Proy Vega B1, Gómez Lluch MT1, Alañón Pardo MM1, Notario Dongil C1
Servicio de Farmacia. Hospital General La Mancha-Centro. Alcázar de San Juan. Ciudad Real (España)
Fecha de recepción: 03/10/2020 – Fecha de aceptación: 21/10/2020
Correspondencia: Beatriz Proy Vega – Avda. de la Constitución, 3 – 13600 Alcázar de San Juan, Ciudad Real (España)
bproyvega@gmail.com
____
RESUMEN
La enfermedad de Behçet es un trastorno inflamatorio multisistémico que se manifiesta de forma muy variada a nivel cutáneo, especialmente en forma de aftas orales frecuentemente refractarias. Los tratamientos con utilidad en la sintomatología de esta patología, resultan poco específicos y poco efectivos; teniendo que recurrir a veces a tratamientos sistémicos, como los biológicos: entre ellos, los anti-TNFα.
Presentamos el caso de una paciente con enfermedad de Behçet, con aftas orales severas, recurrentes y refractarias a múltiples tratamientos. Actualmente, la paciente ha alcanzado la remisión clínica en tratamiento combinado de adalimumab y apremilast.
Palabras clave: Apremilast, adalimumab, Behçet, aftas orales, refractario.
Refractory oral aftas in treatment with adalimumab and apremilast in patient with Behçet syndrome. A case report
SUMMARY
Behçet’s disease is a multisystemic inflammatory disorder that manifests itself in a variety of ways at the cutaneous level, especially in the form of oral thrush, very often very refractory. Treatments that are useful in the symptomatology of this pathology are not very specific and not very effective; sometimes it is necessary to resort to systemic treatments, such as biologi-cal ones: among them, anti-TNFα.
We present the case of a patient diagnosed with Behçet’s disease, with severe oral aphthae, very recurrent and refractory to multiple treatments. Currently, the patient has reached clinical remission in combined treatment of adalimumab and apremilast.
Key words: Apremilast, adalimumab, Behçet, oral thrush, refractary.
____
INTRODUCCIÓN
La enfermedad de Behçet (EB) es una patología inflamatoria crónica multisistémica recurrente de causa desconocida, que presenta alteraciones mucocutáneas, oculares, vasculares, neurológicas y gastrointestinales. Es característica la presencia de aftas orales1, generalmente autolimitadas, que pueden tener un gran impacto negativo en la calidad de vida2. El tratamiento pretende reducir el proceso inflamatorio, mejorar la calidad de vida y prevenir las recaídas. Los tratamientos resultan poco específicos y efectivos, teniendo que recurrir en los casos más graves y refractarios a fármacos como los anti-TNFα. Recientemente, se ha autorizado apremilast para el tratamiento de úlceras bucales asociadas a la EB3.
DESCRIPCIÓN DEL CASO
Mujer de 36 años que requirió ingreso hospitalario tras debut con síndrome de aftas orales, síndrome de Sweet, gingivoestomatitis herpética, fenómeno de patergia, muguet oral, odinofagia intensa, mucosa empedrada en íleon, úlcera perianal, hemorragia digestiva baja autolimitada y anemia asociada. Pruebas complementarias: Hb 10,4 g/dl, L 15.500 cel/µl, PCR 11,5 mg/dl, VSG 37 mm/h, calprotectina >1000 µg/g, Ac anti-DNA 1 UI/ml y ANA negativos. Serologías negativas para VIH, IgM de CMV y RPR, y positivas para IgG de CMV, EBV y difteria. Fue tratada con corticoides, antibióticos, antifúngicos y antivirales. Se realizó un abordaje multidisciplinar entre Medicina Interna, Reumatología, Digestivo, Dermatología y Farmacia. Finalmente fue diagnosticada de EB en abril de 2017.
En noviembre de 2017, tras varios ingresos sucesivos por reagudización de aftas, a pesar de tratamiento corticoideo, azatioprina e inmunoglobulinas, y ante la evolución tórpida, se inició infliximab 5mg/kg/8 semanas (como uso fuera de ficha técnica, UFFT). Posteriormente debido a la falta de respuesta, precisó intensificación a cada 6 semanas (a pesar del incremento de dosis de metotrexato y corticoides).
En septiembre de 2018, se constató fallo secundario a infliximab, y se inició adalimumab 40 mg cada 14 días (también UFFT). Tras ello, vuelve a reingresar por brotes graves de aftosis oral, con desnutrición asociada (precisando nutrición enteral), que mejoraron con dosis altas de corticoides, sin permitir su suspensión.
En octubre de 2019, se solicitó el tratamiento con apremilast añadido a adalimumab. El Servicio de Farmacia autorizó el UFFT del tratamiento combinado, en base a la evidencia disponible y por tratarse de una paciente refractaria a múltiples líneas de tratamiento.
Desde entonces, la paciente no ha precisado ningún ingreso, se mantiene sin brotes y los parámetros analíticos inflamatorios han disminuido (Figuras 1 y 2). El control actual de la enfermedad ha posibilitado el espaciado de adalimumab a 40 mg cada 21 días desde abril de 2020, y desde junio de 2020 a 40 mg mensual. La combinación de ambos fármacos ha sido bien tolerada, sin efectos adversos asociados.
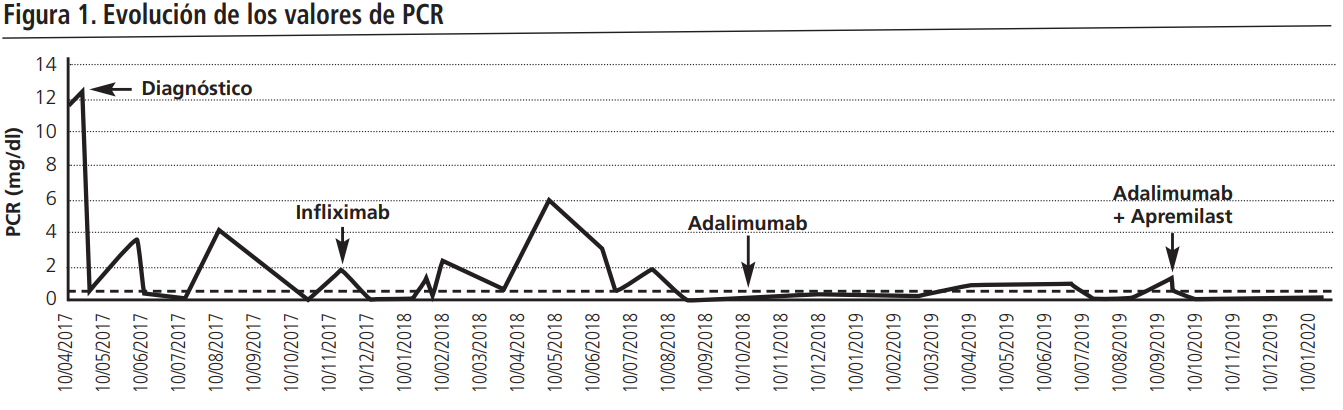
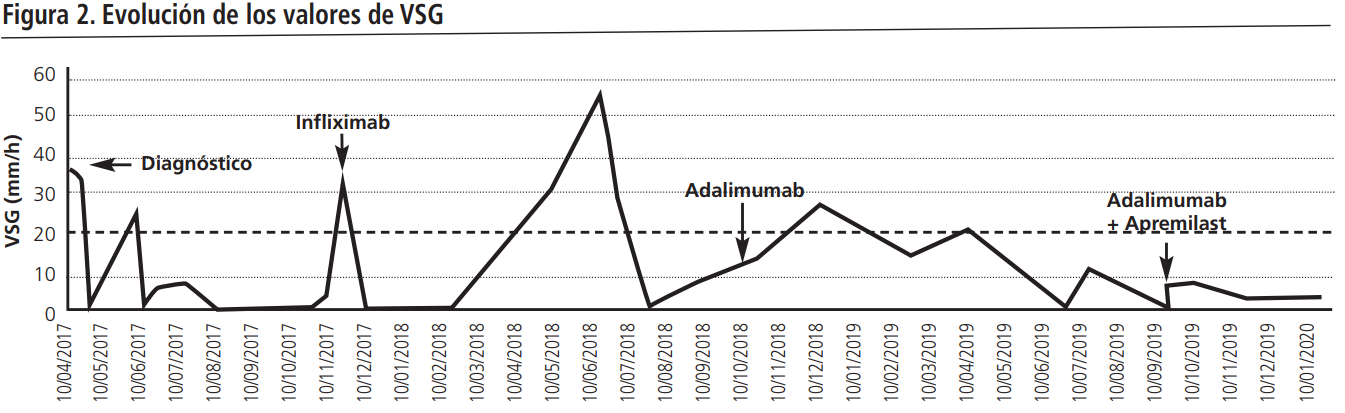
DISCUSIÓN
Se presenta el caso exitoso de una paciente con EB con gran afectación mucocutánea. A pesar de múltiples líneas de tratamiento y corticodependencia, persistían los brotes graves y recurrentes. Con el inicio de la combinación de adalimumab y apremilast ha alcanzado la remisión por primera vez desde el diagnóstico.
En la EB, el control de las manifestaciones cutáneas se realiza habitualmente con colchicina, azatioprina, prednisona y ciclosporina, sin embargo, la eficacia de estos medicamentos no está bien establecida4. En casos más graves y recurrentes se utilizan los anti-TNFα,5,6 (etanercept, infliximab, adalimumab), y aunque las pautas y dosis no están estandarizadas, han demostrado su eficacia en prácticamente todas las manifestaciones clínicas7.
En febrero de 2020, la Agencia Europea del Medicamento aprobó el uso de apremilast en pacientes con EB con aftas orales susceptibles de tratamiento sistémico8. En esta paciente, el tratamiento combinado (apremilast y adalimumab), ha posibilitado la remisión de las aftas orales y otra sintomatología, e incluso la optimización de la terapia, con el espaciado de dosis del anti-TNFα (posibilitando su suspensión futura) y mejorando la calidad de vida de la paciente significativamente.
La utilidad del tratamiento combinado con adalimumab y apremilast ha sido manifestada en varios casos clínicos publicados respecto a otras patologías como psoriasis9 o artritis psoriásica10, sin embargo, no ha sido localizada ninguna publicación sobre EB. Son por tanto necesarios más estudios que evidencien esta utilidad.
Conflicto de intereses: Las autoras declaran no tener conflicto de intereses.
____
BIBLIOGRAFÍA
1. Brote severo de la enfermedad de Behcet con manifestaciones mucocutáneas intensas. Jose M. Martín, Elisabeth Mateo, Carlos Monteagudo y Esperanza Jordá. Reumatol Clin. 2010;6(6):303-305. (Consultado 02/07/2020).
2. What affects the quality of life in patients with Behcet’s disease? M. Melikoglu, M.A. Melikoglu. Acta Reumatol Port. 39 (2014), pp. 46-53.
3. EPAR Otezla. EMA. Disponible en: https://www.ema.europa.eu/en/documents/variation-report/otezla-h-c-003746-ii-0029-epar-assessment-report-variation_.pdf (Consultado 22/06/2020).
4. Taylor J, Glenny A-M, Walsh T, et al. Interventions for the management of oral ulcers in Behçet’s disease. Cochrane Database Syst Rev. 2014;(9):CD011018.
5. Almoznino G, Ben-Chetrit E. Infliximab for the treatment of resistant oral ulcers in Behçet’s disease: a case report and review of the literature. Clin Exp Rheumatol. 2007;25(4 Suppl 45):S99-S102.
6. Sfikakis P, Markomichelakis S, Alpsoy E, Assad-Khalil S, Bodaghi B, Gol A, et al. An-tiTNF therapy in the man agement of Behçet´s disease: review and bas is recommendations. Rheumatology. 2007;46:736-741.
7. Vallet H, Riviere S, Sanna A, et al. Efficacy of anti-TNF alpha in severe and/or refractory Behçet’s disease: Multicenter study of 124 patients. J Autoimmun. 2015 Aug;62:67-74.
8. https://www.ema.europa.eu/en/documents/smop/chmp-post-authorisation-summary-positive-opinion-otezla-ii-29_en.pdf (Consultado el 08/05/2020).
9. Danesh MJ, Beroukhim K, Nguyen C, Levin E, Koo J. Apremilast and adalimumab: a novel combination therapy for recalcitrant psoriasis. Dermatol Online J. 2015 Jun 16;21(6).
10. Abstract ACR 1725: Combination therapy of apremilast and biologic agent as a safe option of Psoriatic Arthritis and Psoriasis.
____
