Calvo-García A, Morell Baladrón A
Departamento de Farmacia. Hospital Universitario de la Princesa. Madrid (España)
Fecha de recepción: 16/08/2022 – Fecha de aceptación: 08/09/2022
Correspondencia: Alberto Calvo-García – Hospital Universitario de la Princesa (Departamento de Farmacia) – Calle de Diego de León, 62 – 28006 Madrid (España)
alberto.calvo@salud.madrid.org
____
RESUMEN
Objetivo: Determinar grado de aceptación e índices de actividad de intervenciones farmacéuticas realizadas en práctica clínica habitual en Unidad COVID de cuidados intensivos.
Método: Análisis retrospectivo de intervenciones registradas durante la actividad clínica diaria de un farmacéutico en Unidad COVID de cuidados intensivos. Se incluyeron pacientes ingresados mínimo 48 horas en la Unidad, entre enero y febrero de 2021. Las variables para determinar el objetivo principal fueron el porcentaje de aceptación de las intervenciones y los siguientes índices de actividad: intervención/paciente, intervención/días e intervención/día-cama de la Unidad de COVID.
Resultados: Se incluyeron 36 pacientes, 21 (56,8%) hombres, y 64,5 (10,8) años de edad media. La media de fármacos prescritos fue 19,1 (7,9). La mediana de estancia en la Unidad fue de 26,5 (15,8-55,3) días. Se realizaron 100 intervenciones y en todos los pacientes se realizó al menos una. La intervención más frecuente fue interacción farmacológica (40,0%). En todos los tipos la aceptación fue del 100%, a excepción del ajuste de dosis (92,0% (IC95%= 94,5-89,5) de aceptación), las interacciones farmacológicas (75,0% (IC95%=77,3-72,7) de aceptación) y la indicación no tratada (50,0% (IC95%=51,8-48,2) de aceptación) (p=0,024). Se registraron un total de 2,8 intervenciones/paciente, 1,7 intervenciones/día y 0,13 intervenciones/día-cama.
Conclusiones: La incorporación del farmacéutico en el equipo de la Unidad COVID de cuidados intensivos y las intervenciones farmacéuticas, obtuvieron un alto grado de aceptación y buenos resultados en los indicadores de actividad. El alto grado de aceptación de las intervenciones indica la relevancia clínica de las mismas; y los indicadores de actividad obtenidos, la alta implicación del farmacéutico.
Palabras clave: Unidad de cuidados intensivos, intervenciones farmacéuticas, COVID-19, atención farmacéutica.
Analysis of the pharmaceutical interventions conducted by a hospital pharmacist in a COVID Intensive Care Unit: acceptance level and activity indexes
SUMMARY
Objective: To determine the acceptance level and activity indexes of pharmaceutical interventions performed in routine clinical practice in a COVID Intensive Care Unit.
Methods: A retrospective analysis of the interventions during the daily clinical activity of a pharmacist in the Intensive Care Covid Unit was performed. Patients admitted to the unit minimum 48 hours, between January and February 2021 were included. The variables to determine the main objective of the study were the percentage of acceptance of the interventions and the following activity indexes: intervention/patient, intervention/day and intervention /day-bed in the COVID Unit.
Results: 36 patients were included, 21 (56.8%) were male, with a mean age of 64.5 (10.8) years. The median number of drugs prescribed was 19.1 (7.9). The median days in the Unit was 26.5 (15.8-55.3). A total of 100 interventions were performed and all patients underwent at least one intervention. The most frequent intervention was drug interaction (40.0%). Acceptance for all intervention types was 100%, with the exception of dose adjustment (92.0% (95%CI=94.5-89.5) acceptance), drug interactions (75.0% (95%CI=77.3-72.7) acceptance) and untreated indication (50.0% (95%CI=51.8-48.2) acceptance) (p=0.024). A total of 2.8 interventions/patient, 1.7 interventions/day and 0.13 interventions/bed-day were recorded.
Conclusions: The incorporation of the pharmacist in the team of a COVID Intensive Care Unit, and the pharmaceutical interventions, obtained a high degree of acceptance and good results in activity indexes. The high degree of acceptance of the interventions indicates the clinical relevance of the interventions; and the activity indexes obtained the high involvement of the pharmacist.
Key words: Intensive Care Unit, pharmaceutical interventions, COVID-19, pharmaceutical care.
____
INTRODUCCIÓN
Las Unidades de cuidados intensivos (UCI) son unas de las Unidades hospitalarias donde los tratamientos farmacológicos presentan una mayor complejidad, por lo que el riesgo de aparición de problemas relacionados con la medicación (PRM) puede ser mayor. Estos PRM pueden afectar a la efectividad de los tratamientos o a la aparición de eventos adversos (EAs) atribuibles a la medicación más severos1. Los PRM se definen como los problemas de salud vinculados con la farmacoterapia que interfieren o pueden interferir con los resultados de salud esperados en el paciente2. A parte de la complejidad de los tratamientos farmacológicos, existen otros factores responsables de su elevada incidencia en la UCI, como la propia complejidad fisiopatológica del paciente crítico, el trabajo bajo presión de los profesionales sanitarios, la rápida toma de decisiones clínica, el frecuente cambio en las prescripciones farmacológicas, el elevado uso de medicamentos de alto riesgo, o las peculiaridades de la farmacocinética y farmacodinamia del paciente crítico1. Los farmacéuticos hospitalarios (FH) pueden contribuir a la revisión de los tratamientos farmacológicos del paciente crítico y prevenir los PRM.
Por otro lado, la emergencia sanitaria producida en el año 2020 por el virus SARS-CoV-2 (Severe acute respiratory syndrome coronavirus 2), nombrada por la Organización Mundial de la Salud como COVID-19 (Coronavirus disease 2019), puso a prueba la capacidad de las UCIs. Según un estudio realizado en China durante los primeros meses de la pandemia, entre el 5-10% de los pacientes que desarrollan neumonía grave por SARS-CoV-2, requirieron ingreso en UCI3. Este aumento de la presión asistencial en las Unidades COVID de las UCI y la limitada experiencia en los tratamientos usados para hacer frente a la enfermedad, puede favorecer la aparición de PRM4. La Society of Critical Care Medicine (SCCM) de Estados Unidos, recomienda, con un nivel de evidencia C, la incorporación de un FH a los equipos multidiciplinares que proporcionan atención a los pacientes COVID-19 ingresados en las Unidades de críticos5.
Entre las funciones del FH durante la crisis sanitaria, estuvieron la evaluación de los nuevos tratamientos para la COVID-19 con el fin de favorecer la rápida disponibilidad de los mismos, monitorizar y ajustar los tratamientos para prevenir EAs atribuibles a la medicación, mantenimiento de los stocks y garantizar el suministro de medicamentos ininterrumpido y adaptarse a la situación de emergencia sanitaria, garantizando la correcta atención a los pacientes por parte del Servicio de Farmacia6.
Las intervenciones farmacéuticas (IF) se define como la actuación dirigida a modificar alguna característica del tratamiento, del paciente que lo utiliza o de las condiciones de uso, y que tiene por objetivo resolver un PRM o un resultado negativo asociado a la medicación7. Existen numerosos estudios que abalan la reducción de PRM con la presencia de un FH en los equipos multidisciplinares de UCI8-19. Por otro lado, existen distintas publicaciones donde se describe el rol del FH en las Unidades COVID de críticos20-24, pero poca bibliografía que analice su actividad en dichas Unidades. Por ello se desarrolló este estudio con el objetivo de determinar el grado de aceptación, los índices de actividad y los patrones de las IF realizadas en práctica clínica habitual durante dos meses en la Unidad COVID de una UCI.
MATERIAL Y MÉTODOS
Se realizó un análisis retrospectivo de las IF registradas durante la actividad clínica diaria de un FH, en la Unidad COVID de la UCI del Hospital Universitario de La Princesa. La UCI no había contado previamente con un FH en su plantilla. El estudio fue aprobado por el Comité de Evaluación de Investigación y Medicamentos del Hospital Universitario de la Princesa, y la Agencia Española de Medicamentos y Productos Sanitarios. Dada la naturaleza de práctica clínica habitual del estudio y el análisis retrospectivo de los datos, no se solicitó consentimiento informado de los pacientes.
Los criterios de inclusión fueron los siguientes: pacientes con infección por SASR-CoV-2 mayores de edad, ingresados un periodo mínimo de 48 horas en la UCI entre los meses de enero y febrero de 2021. Los pacientes con seguimiento y datos incompletos, fueron excluidos del análisis estadístico.
La Unidad COVID de la UCI contaba con trece camas distribuidas en 11 boxes. Entre enero y febrero del 2021, diariamente durante la jornada laboral de 7 horas, se validaron los tratamientos farmacológicos prescritos de todos los pacientes ingresados en la Unidad (dosis, posología, vía de administración, velocidad de administración, concentración y componentes de las perfusiones, posibles alergias e interacciones farmacológicas). Además se revisaron las analíticas y gasometrías, los cultivos de microbiología y otras constantes de los pacientes, con el fin de determinar la adecuación de los tratamientos. También se participó en la sesión clínica multidisciplinar diaria, con los médicos intensivistas, enfermeras y médicos de otras especialidades, cuando así era requerido.
En todos estos procesos se llevaron a cabo las IF, en el programa de prescripción e historia clínica electrónica, y verbalmente en las sesiones clínicas o durante el pase médico. Además se realizó un registro de las IF en una base de datos, donde se recogieron las siguientes variables: sexo, edad, diagnóstico principal de ingreso, ingreso en UCI en las primeras 48h tras ingreso hospitalario, tiempo de estancia en UCI, el índice de comorbilidades de Charlson25, la escala Acute Physiology and Chronic Health Evaluation (APACHE) II26 al ingreso, número de medicamentos prescritos, tipo de IF, medicamento sobre el que se realiza la IF, grupo del medicamento según la Anatomical Therapeutic Chemical (ATC) Classification System y aceptación de la IF.
Las IF se clasificaron en siete grupos: selección correcta de medicamentos, medicamento prescrito no necesario, indicación no tratada, selección correcta de vía de administración, interacciones farmacológicas, reacción adversa al medicamento (RAM) o alergia, y error al recibir el medicamento27. En las interacciones farmacológicas se utilizó la base de datos UpToDate, y solo se consideraron aquellas de categoría C (monitorizar terapia concomitante), D (evitar uso concomitante y considerar alternativas terapéuticas) y X (contraindicado el uso concomitante de los medicamentos)28. Para valorar el cumplimento de las IF realizadas para interacciones categoría C, se comprobó con los médicos del equipo que se realizaba la monitorización correspondiente. Para categorizar las RAM se aplicó el Algoritmo de Naranjo, y se consideraron aquellas que obtuvieron una puntuación entre 5-8 (RAM con probable relación) y mayor de 9 (RAM definida)29.
Las variables para determinar el objetivo principal del estudio fueron el porcentaje de aceptación de las IF y los siguientes índices de actividad: IF por paciente, IF por días del periodo del estudio e IF por día y cama de la Unidad de COVID de la UCI27.
Análisis estadístico
La estadística descriptiva de las variables se expresó en proporciones e intervalos de confianza al 95%. En las variables de distribución normal se utilizaron medias y desviaciones estándar; para las variables de distribución no normal se utilizaron mediana y rangos intercuartílico (RIQ). La prueba Chi Cuadrado se aplicó para analizar la aceptación con los distintas tipos de IF. Los resultados se consideraron estadísticamente significativos si el p valor fue menor de 0,05. El software utilizado fue SPSS versión 22.0.
RESULTADOS
Características sociodemográficas
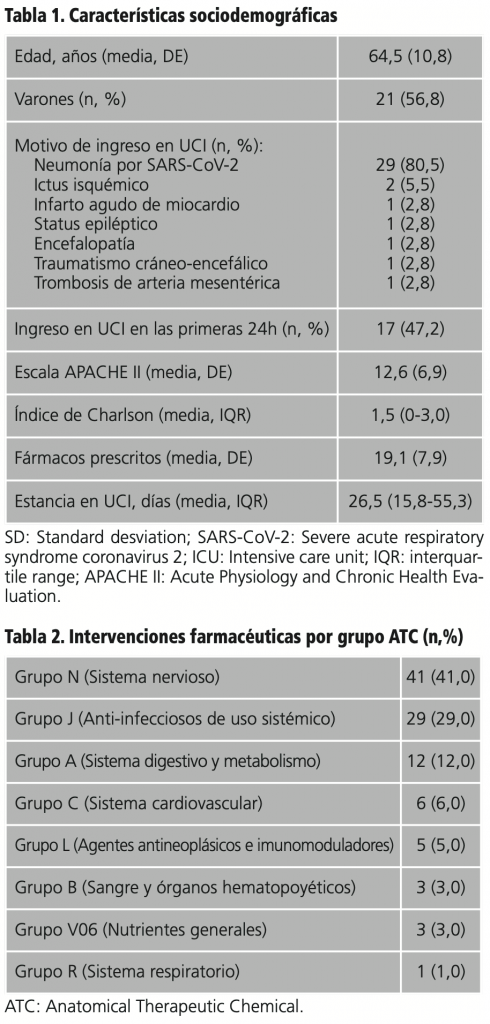
De total de 36 pacientes incluidos en el estudio, 21 (56,8%) fueron hombres, con una media de edad de 64,5 (10,8) años. Todos presentaban infección por SARS-CoV-2, y en 29 (80,6%) pacientes el motivo de ingreso en la UCI fue la neumonía, mientras que en el resto de pacientes el motivo de ingreso fue otra patología no asociada con el virus. Menos de la mitad de los pacientes (47,2%) tuvieron un ingreso en la UCI en las primeras 24h. La media de la escala APACHE II al ingreso fue de 12,6 (6,9) puntos, y la mediana del índice de Charlson 1,5 (0-3,0) puntos. La media de fármacos prescritos fue de 19,1 (7,9). La mediana de estancia en la UCI fue de 26,5 (15,8-55,3) días. El resto de características sociodemográficas se muestran en la tabla 1.
IF, grado de aceptación e índices de actividad
Durante los meses de enero y febrero se llevaron a cabo un total de 100 IF. En todos los pacientes se realizó al menos una IF. El tipo de IF más frecuente fue interacción farmacológica (40,0%), seguida de ajuste de dosis de medicamento (incluyendo el ajuste de dosis por insuficiencia renal (IR)) (25,0%), RAM (14,0%), la selección correcta de medicamentos (9,0%), medicamento no necesario (4,0%), vía de administración incorrecta (3,0%), error al recibir el medicamento (3,0%) e indicación no tratada (2,0%). Los dos grupos ATC predominantes en las IF fueron grupo N o del sistema nervioso, con el 41,0% de las IF y el grupo J o de los anti-infecciosos de uso sistémico, con el 29,0% de las IF. El resto de IF por grupo ATC se recogen en la tabla 2. Un total de 87 IF fueron aceptadas, siendo el grado de aceptación del 87,0% (IC95%= 89,5-84,5). Se registraron un total de 2.8 IF/paciente, 1,7 IF/día y 0,13 IF/día cama.
Análisis del grado de aceptación por tipo de IF
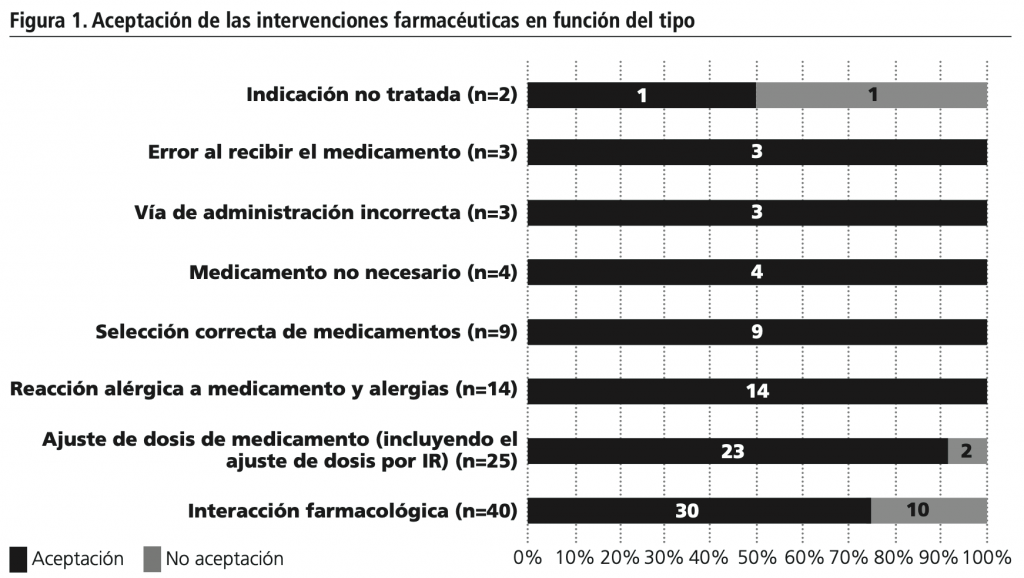
En la figura 1 se muestra el perfil de aceptación por tipo de IF. En todos los tipos de IF la aceptación fue del 100%, a excepción del ajuste de dosis de medicamento (incluyendo ajuste de dosis por IR), que obtuvo un 92,0% (IC95%= 94,5-89,5) de aceptación, las interacciones farmacológicas con un 75,0% (IC95%=77,3-72,7) de aceptación y la indicación no tratada con un 50,0% (IC95%=51,8-48,2) de aceptación. Al aplicar el test de Chi cuadrado se obtuvo una distribución asimétrica estadísticamente significativa (p=0,024).
DISCUSIÓN
Los PRM y las consecuencias derivadas de los mismos, como pérdida de efectividad de los tratamientos o toxicidad relacionada, son frecuentes en las Unidades de críticos1. La pandemia producida por la COVID-19 puso a prueba la capacidad de las UCIs3. La incorporación de un FH a los equipos multidisciplinares que atienden a este tipo de pacientes esta abalado por la SCCM de Estados Unidos5. A nuestro conocimiento, este es el primer estudio que se realiza en España para evaluar la actividad de las IF realizadas por un FH en la Unidad COVID de una UCI, donde tradicionalmente no se contaba con la presencia de un FH en el equipo multidisciplinar.
Las características demográficas muestran la complejidad clínica de los pacientes incluidos en el estudio. Una población envejecida, la larga estancia en UCIs, con 27 días de estancia media o el elevado número de fármacos prescrito por paciente, son factores que puede favorecer estos PRM1.
Durante los dos meses que duró la presencia del FH en la UCI, se participó diariamente no solo en la validación de los tratamientos farmacológicos, también en las sesiones clínicas multidisciplinares y pases clínicos diarios, ayudando a la toma de decisiones en la mejor opción terapéutica para los pacientes mediante una valoración íntegra del mismo. Esta incluía aspectos como la inmunosupresión, función renal o interacciones farmacológicas entre el tratamiento agudo y habitual del paciente. Por esta razón, aunque el periodo solo fue de dos meses y los pacientes en seguimiento 36, se llevaron a cabo 100 IF, y en todos ellos se realizó al menos una IF, indicando la elevada actividad realizada por el FH.
Lo principales fármacos sobre el que se realizaron IF fueron aquellos pertenecientes al grupo del sistema nerviosos. El frecuente cambio de posología que se realiza en este grupo de fármacos para ajustar la sedo-analgesia a las necesidades cambiantes del paciente crítico, justificaría que sean los fármacos donde más IF se realizaron para prevenir PRM. En otros estudios en Unidades de críticos de COVID, el grupo de fármacos con más IF fueron los anti-infecciosos30-33. En nuestro caso, este fue el segundo grupo mayoritario. Es de vital importancia en estos fármacos, debido a que la correcta prescripción de los mismos no solo influye en la resolución del proceso infeccioso que puede ser determinante en el pronóstico del paciente, sino que también va a condicionar la posible aparición de bacterias multirresistente, un problema creciente en nuestro medio en los últimos años, y que se ha visto acentuado por la COVID-1934.
El grado de aceptación fue elevado, llegándose a un 87,0%; similar a otros estudios en Unidades COVID de UCIs, como el llevado a cabo en Francia por Perez et al.30, y en Eslovenia por Cvikl et al.31. Por otro lado, Wang et al.32, en su estudio llevado a cabo en una UCI en China durante la primera ola de la pandemia, obtuvo un porcentaje de aceptación mayor (95,0%). Los indicadores de actividad obtenidos en nuestro estudio, con casi tres IF/pte y dos IF/día, reflejan la alta implicación del FH, participando activamente en las sesiones multidisciplinares, y las rondas de pases de pacientes; así como con la dedicación exclusiva de toda su jornada laboral. A su vez estos factores, pueden contribuir al alto porcentaje de aceptación por parte de los intensivistas, indicando que estas son clínicamente relevantes y que se cubren las necesidades clínicas.
En cuanto al análisis de la aceptación por tipo de IF, solo en dos tipos de interacciones la aceptación fue inferior a la media: las interacciones farmacológicas y las indicaciones no tratadas. En el grupo de las interacciones farmacológicas, a pesar de que fueron el tipo de IF más realizada, solo se obtuvo un 75,0% de aceptación. Esta tendencia desfavorable en el caso de la interacciones farmacológicas también lo describieron Cvikl et al.31. La menor aceptación en este grupo de IF, puede ser debido a que la situación crítica de los pacientes se prioriza en la decisión clínica de mantener tratamientos que a priori pueden producir una interacción farmacológica. Además en nuestras IF, se incluyeron también interacciones de la categorías D, la cual no supone una contraindicación total, sólo la recomendación de buscar alternativas terapéuticas28.
En el caso de las indicaciones no tratadas, solo se realizaron dos IF, aceptándose sólo una de ellas. La IF aceptada por el equipo médico, fue llevada a cabo en un paciente inmunodeprimido que estaba en tratamiento habitual profiláctico para hepatitis B con lamivudina, en el que la recomendación fue su prescripción durante el ingreso. En el caso de la IF no aceptada, se realizó en un paciente con hipertrigliceridemia en contexto de sedación con propofol, donde se propuso el inicio de tratamiento con fibrato.
Nuestro estudio tiene algunas limitaciones. La primera, es que se trata de un análisis retrospectivo de las IF realizadas por un FH. La segunda está relacionada con el corto periodo de tiempo durante el que se llevaron a cabo dichas IF y por tanto pocos pacientes analizados, a pesar del elevado número de IF realizadas. Un estudio prospectivo durante un intervalo de tiempo más largo, implicaría a una mayor cohorte de pacientes. En tercer lugar, no se analizó la relevancia clínica de las IF realizadas, con escalas como la propuesta por Overhage et al.35. Sin embargo, el alto porcentaje de aceptación de las IF, se puede relacionar con la relevancia clínica de las mismas.
Como conclusión, en la incorporación del FH en el equipo médico de la Unidad COVID de una UCI, se obtuvo un alto grado de aceptación de las IF y buenos resultados en los indicadores de actividad de la del FH. A su vez, el alto grado de aceptación de las IF indica la relevancia clínica de las mismas, y los indicadores de actividad obtenidos, la alta implicación del FH. Las interacciones farmacológicas fueron el grupo principal de IF y a su vez obtuvieron menor grado de aceptación que la media, lo que podría deberse a que el equipo médico, prima la situación clínica del paciente y la necesidad de los tratamientos a la propia interacción. A pesar del corto periodo de tiempo del estudio y del análisis retrospectivo, creemos que estos resultados son prometedores y contribuyen a la bibliografía existente para avalar el papel y la calidad de la asistencia sanitaria que los FH puede aportar al equipo multidisciplinar que atiende no solo al paciente crítico con COVID, también a otros pacientes ingresados en Unidades de críticos. Para afianzar estos resultados podría llevarse a cabo un estudio prospectivo más extenso en el que se analizase la relevancia de las IF con escalas validadas.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
BIBLIOGRAFÍA
1. Pilau R, Hegele V, Heineck I. Role of clinical pharmacist in adult intensive care unit: a literature review. Rev Bras Farm Hosp Serv Saude. 2014;1(5): 19-24.
2. Espejo J, Fernández-Llimós F, MAchuca M, Faus MJ. Drug relates problems: Definition and proposal for its inclusion in the International Classification of Primary Care (ICPC) from WONCA. Pharmaceutical Care España. 2002;4 (2):122-127.
3. Wu Z, McGoogan JM. Characteristics of and important lessons from the coronavirus disease 2019 (COVID-19) outbreak in China: summary of a report of 72 314 cases rrom the Chinese center for disease control and prevention. JAMA. 2012;20(323):1239-42.
4. Li H, Zheng S, Liu F, Liu F , Liu W, Zhao R. Fighting against COVID-19: innovative strategies for clinical pharmacists. Res Soc Adm Pharm RSAP. 2021; 7(1):1813-18.
5. Society of Critical Care Medicine. United States Resource Availability for COVID-19 [Página web]. Mount Prospect, US. Society of Critical Care Medicine; 05/12/2020 [05/12/2020; 16/04/2022]. Disponible en: https://www.sccm.org/ Blog/March-2020/United-STates-Resource-Availability-for-COVID-19?utm_source=Email&utm_cmpaign=E-Newsletter&zs=jkSjd1&_zl=Jt7m6.
6. Goff DA, Ashiru-Oredope D, Cairns KA, Eljaaly K, Langford BJ, Messina A, et al. Global contributions of pharmacist during the COVID-19 pandemic. J Am Col Clin Pharm. 2020;2(3):1480-92.
7. Fundacion Pharmaceutical Care. Foro de Atención Farmacéutica Informa: Intervención farmacéutica. Barcelona, España. Fundacion Pharmaceutical Care. 2008 [2018;16/04/2022]. Disponible: https://www.pharmaceutical-care.org/archivos/810/foro_intervencion.pdf.
8. Klopotowska JE, Kuiper R, van Kan HJ, de Pont AC, Dijkgraaf MG, Lie-A-Huen L, et al. On-ward participation of a hospital pharmacist in a Dutch intensive care unit reduces prescribing errors and related patient harm: an intervention study. Critical Care. 2010;14(5):R174.
9. Kessemeier N, Meyn D, Hoeckel M, Reitze J, Culmsee C, Tryba, M. A new approach on assessing clinical pharmacists’ impact on prescribing errors in a surgical intensive care unit. Int J Clin Pharm. 2019;41(5):1184-92.
10. Johansen ET, Haustreis SM, Mowinckel AS,1 Ytrebø LM. Effects of implementing a clinical pharmacist service in a mixed Norwegian ICU. Eur J Hosp Pharm. 2016;23(4):197-202.
11. Jiang S-P, Zheng X, Li X, Lu X-Y. Effectiveness of pharmaceutical care in an intensive care unit from China. A pre- and postintervention study. Saudi Med J. 2012;33(7):756-62.
12. Leape LL, Cullen DJ, Clapp M, Burdick E, Demonaco HJ, Ives Erickson J, et al. Pharmacist participation on physician rounds and adverse drug events in the intensive care unit. JAMA. 1999;282(3):267-70.
13. Montazeri M, Cook DJ. Impact of a clinical pharmacist in a multidisciplinary intensive care unit. Crit Care Med. 1994;22(6):1044-8.
14. Al-Jazairi AS, Al-Agil AA, Asiri YA, Al-Kholi TA, Akhras NS, Horanieh BK. The impact of clinical pharmacist in a cardiacsurgery intensive care unit. Saudi Med J. 2008;29(2):277-81.
15. MacLaren R, Bond CA. Effects of pharmacist participation in intensive care units on clinical and economic outcomes of critically Ill patients with thromboembolic or infarction-related events. Pharmacotherapy. 2009;29(7):761-8.
16. Kucukarslan SN, Corpus K, Mehta N, Mlynarek M, Peters M, Stagner LS, et al. Evaluation of a Dedicated Pharmacist Staffing Model in the Medical Intensive Care Unit. Hosp Pharm. 2013;48(11):922-30.
17. Souza e Silva AC, Carvalho Sousa DS, Carvalho Perraud EO, Almeida Oliveira FR, Cardoso Martins BC. Pharmacotherapeutic follow-up in a respiratory intensive care unit: description and analysis of results. Einstein (Sao Paulo). 2018; 16(2):eAO4112.
18. Fideles GMA, de Alcântara-Neto JM, Peixoto Júnior AA, de Souza-NetoPJ, Luana Tonete T, Gomes da Silva JE, et al. Pharmacist recommendations in an intensive care unit: three-year clinical activities. Rev Bras Ter Intensiva. 2015;27(2):149-54.
19. Ervin JN, Kahn JM, Cohen TR, Weingart LR. Teamwork in the Intensive Care Unit. Am Psychol. 2018;73(4):468-77.
20. García-Gil M, Velayos-Amo A. Hospital Pharmacist experience in the Intensive Care Unit: Plan COVID. Farm Hosp. 2020;44(7):32-5.
21. Lemtiri J, Matusik E, Cousein E, Lambiotte F, Elbekid N. The role of the critical care pharmacist during the COVID-19 pandemic. Ann Pharm Fr. 2020;78(6):464-8.
22. Gil-Navarro MV, Luque-Márquez R. Hospital Pharmacy in the multidisciplinary team of COVID inpatient units. Farm Hosp. 2020;44(7):40-2.
23. Santolaya-Perrin R, García-Martín A, Carrero-Fernández A, Torres-Santos-Olmo R. Hospital pharmacist experience in a multidisciplinary team in special care settings. Farm Hosp. 2020;44(7):36-9.
24. Besson C, Chareyre S, Kirouani N, Jean-Jean S, Bretagnolle C, Henry A, et al. Contribution d’une équipe de pharmacie hospitalière à la prise en charge en réanimation des patients infectés par le SARS-CoV-2. Ann Pharm Fr. 2021;79(4): 473-80.
25. Charlson ME, Pompei P, Ales KL, MacKenzie CR. A new method of classifying prognostic comorbidity in longitudinal studies: development and validation. J Chronic Dis. 1987;40(5):373-83..
26. Knaus WA, Draper EA, Wagner DP, Zimmerman JE. APACHE II: a severity of disease classification system. Crit Care Med. 1985;13(10):818-29.
27. Clopés A. Intervención farmacéutica. En: Gamundi Planas MC. Farmacia Hospitalaria. Tomo 1. Madrid: SEFH; 2002. p. 113-44.
28. Wolters Kluwer. Drug interactions UpToDate. US. Wolters Kluwer. 2022 [2022; 16/04/2022]. Disponible: https://www.uptodate.com/drug-interactions/? source=responsive_home#di-druglist.
29. Naranjo CA, Busto U, Sellars EM, Sandor P, Ruiz I, Roberts EA, et al. A method for estimating the probability of adverse drug reactions. Clin Pharmacol Ther. 1981;30(2):239-45.
30. Perez M, Masse M, Deldicque A, Beuscart JB, De Groote P, Desbordes J, et al. Analysis of clinical pharmacist interventions in the COVID-19 units of a French university hospital. Analysis of clinical pharmacist interventions in the COVID-19 units of a French university hospital.
31. Cvikl M, Sinkovič A. Interventions of a clinical pharmacist in a medical intensive care unit – A retrospective analysis. Bosn J Basic Med Sci. 2020;20(4):495-501.
32. Wang R, Kong L, Xu Q, Yang P, Wang X, Chen N, et al. On-ward participation of clinical pharmacists in a Chinese intensive care unit for patients with COVID-19: A retrospective, observational study. Res Social Adm Pharm. 2021;17(1):1853-8.
33. Alwhaibi A, Alrwaished A, Binobydaan SM, Alawwad S, Wajid S, Bablghaith S, et al. Role of pharmacist during COVID-19 pandemic: A retrospective study focused on critically ill COVID-19 patients. Saudi Pharm J. 2021;29(9):1050-5.
34. Cooke J. Antimicrobial ressitence: a major priority for global focus. Eur J Hosp Pharm. 2022;29(2):63-4.
35. Overhage JM, Lukes A. Practical, reliable, comprehensive method for characterizing pharmacists’ clinical activities. Am J Health Syst Pharm. 1999;56(23): 2444-50.
____