Domínguez Gozalo A1, García Benayas E2, Hidalgo Correas FJ2, García Díaz B3
1 Licenciada en Farmacia y Bioquímica. Residente de 4º año de Farmacia Hospitalaria
2 Licenciada/o en Farmacia. Facultativo Especialista de Farmacia Hospitalaria
3 Jefe de Servicio de Farmacia Hospitalaria
Introducción
La infección por virus de la hepatitis C (VHC) genotipo 1 tradicionalmente se trataba con Peg-Interferon (P-INF) α2a ó α2b y ribavirina (RBV), consiguiéndose tasas de respuesta viral sostenida (RVS) del 50%. La adición de telaprevir o boceprevir (inhibidores de la proteasa (IPs) del VHC genotipo 1 ha conseguido tasas de RVS del 75%1. La mayor complejidad de la triple terapia genera o agrava los efectos adversos asociados, entre ellos anemia más frecuente con boceprevir (49%) que con telaprevir (32%)2. Su origen es multifactorial, mientras que RBV produce hemolisis, IPs y P-INF inhiben los mecanismos estimulantes de eritropoyesis3. La anemia es más grave en pacientes pretratados y con insuficiencia renal (IR)1, y es un factor predictor positivo de eliminación del VHC2-4. En pacientes tratados con boceprevir se observó mayor porcentaje de RVS en los que desarrollaron anemia (72%) frente a los que no (58%)4.
El objetivo del trabajo es describir el caso de una paciente con VHC tratada con triple terapia que desarrolló anemia refractaria y prolongada, originando su ingreso hospitalario.
____
Descargue aquí el artículo en PDF: Anemia refractaria y prolongada en paciente VHC en tratamiento con triple terapia
Artículo dentro del número: VOL. 25 – Nº2 – 2015
____
DESCRIPCIÓN DEL CASO
Mujer de 54 años diagnosticada de hepatopatía crónica (febrero de 2008) por VHC (genotipo 1b, IL-B28 CT), naive, fibrosis grado F4 (Fibroscan 26 KPa), carga viral (CV) 6,3 log, albumina sérica 45 g/L, plaquetas 113.000/μl, crioglobulinemia mixta tipo III (crioglobulinas positivas), IR moderada (Aclaramiento creatinina (ClCr)=46 ml/min) y proteinuria, diabetes mellitus tipo II (DM II) en tratamiento con metformina y glimepirida, HTA controlada con torasemida y amlodipino, hipotiroidismo y ansiedad.
Inició tratamiento en marzo de 2012 con RBV oral 1.000 mg/día, P-ING α2b subcutáneo 100 mcg/semana y eritropoyetina (EPO) subcutánea 40.000 UI/semana por anemia leve (Hemoglobina (Hb)=11 g/dl).
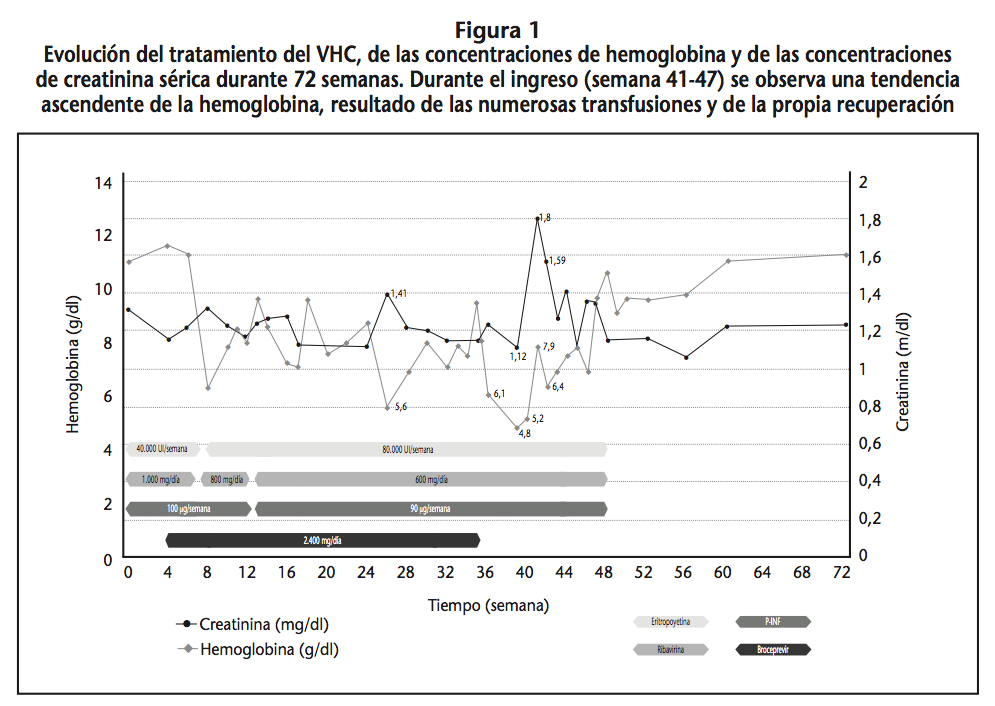
A las 4 semanas inició tratamiento con boceprevir oral 2.400 mg/día por reducción de la CV a 3,3 log y con valores de Hb basales (11,6 g/dl). Desde la 8ª semana la CV fue indetectable, pero se observó un importante descenso de Hb (6,3 g/dl), incrementándose la dosis de EPO a 80.000 UI/semana, administrándose hierro oral, transfundiéndose concentrados de hematíes (CH) (1-2 veces/semana) y ajustándose dosis de RBV a 600 mg/día (9 mg/kg) y P-INF a 90 mcg/semana en la semana 12 (Figura 1).
La paciente manifestó cansancio, fatiga grave (necesitó silla de ruedas), pérdida de peso (15 Kg), neutropenia, rash, alopecia, disgeusia, infecciones urinarias recurrentes y candidiasis orofaringea.
En la semana 26 presentó un valor de Hb de 5,6 g/dl (primer valor más bajo) coincidiendo con el empeoramiento de la función renal (Creatinina sérica (Cr)=1,41 mg/dl; ClCr=41 ml/min) (Figura 1). Por decisión de la paciente no se suspendió boceprevir hasta la semana 36, continuando con P-INF y RBV hasta la semana 48.
En la semana 39 la Hb disminuyó a 4,8 g/dl, requiriendo repetidas transfusiones de CH e ingresando por anemia grave (Hb=5,2 g/dl), dolor por múltiples caídas, desnutrición y hepato y esplenomegalia en la semana 40. La función renal siguió empeorando (Cr=1,8 mg/dl; ClCr=33 ml/min) así como la anemia (Figura 1), necesitando transfusiones de 2 CH cada 2-3 días. En total la paciente fue transfundida 22 veces (55 CH y 1 pool de plaquetas) desde la semana 8 de tratamiento hasta el final.
El ingreso se complicó con acidosis láctica por metformina e hiperpotasemia por laxantes osmóticos. La paciente fue dada de alta la semana 47 con CV indetectable y Hb de 9,7 g/dl.
Finalizado el tratamiento en la semana 48 la función renal se recuperó (ClCr=50 ml/min). En la semana 72 la paciente presentó RVS, crioglobulinas negativas, hemoglobinemias normales y recuperación física.
DISCUSIÓN
Son varios los factores que predisponen a desarrollar anemia en pacientes tratados con boceprevir: sexo femenino, edad (>40 años), fibrosis avanzada, ClCr<80 ml/min, polimorfismo del gen inosina trifosfato (ITPA), anemia previa, uso de estatinas y grado de reducción de Hb durante la fase lead in5. En nuestro caso desconocemos el polimorfismo del gen ITPA, y el descenso de Hb durante el lead in no se puede valorar por la administración de EPO. Respecto al resto, la paciente cumple todos excepto el uso de estatinas, por lo que la anemia es un efecto adverso esperable y por lo tanto se inició tratamiento con EPO desde la semana 1.
En el 95% de los pacientes con biterapia, la Hb disminuye ligeramente durante las primeras 4 semanas6. En general se observa una disminución de Hb de aproximadamente 3 g/dl durante los 3 primeros meses de tratamiento y al añadir boceprevir una disminución extra de 1 g/dl5.
En el estudio SPRINT-2, con la adición de boceprevir en la semana 4 se observo una disminución de 1,3 g/dl en la Hb en la semana 84, y durante todo el tratamiento hasta 5,3 g/dl (valor máximo observado)4. En nuestro caso observamos una disminución mucho mayor, de 5,3 g/dl (semana 8) y de 6,2 g/dl (valor máximo). La reducción de Hb en pacientes tratados con boceprevir se mantiene hasta el final del tratamiento (semana 48) y tras la suspensión del mismo la Hb vuelve a niveles basales5. Nuestra paciente tardó 12 semanas en recuperarlos.
Cuando Hb es <10 g/dl se recomienda disminuir progresivamente dosis de RBV hasta un mínimo de 600 mg (en dosis escalonada de 200 mg) y suspender cuando Hb es <8,5 g/dl2,4,6. Algunos clínicos prefieren mantener el tratamiento hasta Hb<7,5 g/dl administrando EPO y/o transfundiendo CH3. La triple terapia se debe suspender cuando Hb<7 g/dl, si hay compromiso hemodinámico o si no se consigue estabilizar Hb>8,5 g/dl a pesar de transfundir CH5. Este sería el caso de nuestra paciente, que a pesar de la recomendación médica de abandonar el tratamiento decidió finalizarlo. Otra sugerencia recogida en la bibliografía es suspender RBV durante 3 días, y en el caso de no controlarse la anemia y por lo tanto no poder reintroducir RBV, suspender la terapia triple5.
RBV se elimina principalmente vía renal (semivida de eliminación=79 horas)5,7 y se debe usar con precaución cuando Cr es >2 mg/dl y/ó ClCr es <50 ml/min5,7. En estos casos se recomienda monitorizar estrechamente las concentraciones de Hb, adoptando las medidas correctoras que se consideren oportunas a lo largo del tratamiento (ajustar dosis de RBV, administrar EPO y/o transfundir CH)5. Algunos autores opinan que en casos de IR o anemia grave controlada (Hb<7,5 g/dl) es preferible administrar RBV 400 mg/día o 200 mg/3veces/semana antes de suspender tratamiento3, ya que durante la anemia la disminución de dosis de RBV no afecta a la eficacia del tratamiento porque aumenta el área bajo la curva (AUC) de RBV4. En nuestra paciente influyó de forma decisiva tanto para el desarrollo de la anemia4 como para la RVS5, que la dosis de RBV se mantuviera en 600 mg/día a pesar de la afectación renal (ClCr=33 ml/min). Por otra parte, como se ha visto en el estudio PAN, la frecuencia de reducción del filtrado glomerular (FG) por debajo de 60 ml/min es mayor con la triterapia que con la biterapia y además el IP se establece como factor de riesgo de sufrir reducción del FG<60 ml/min y con ello el aumento de la acumulación de RBV7.
En general, se recomienda administrar EPO cuando no es suficiente la disminución de dosis de RBV o según criterio clínico cuando Hb es <10 g/dl2-5,8. Habitualmente, se inicia con 40.000 UI/semana, ajustándose la dosis y el intervalo de administración en función de los valores de Hb y la clínica, y suspendiéndose cuando Hb>12 g/dl2-5,8. En los pacientes tratados con boceprevir, no se observan diferencias en la RVS en función de la estrategia elegida para controlar la anemia8. En general se prefiere disminuir la dosis de RBV antes de administrar EPO, aunque las 2 opciones son igual de eficaces y seguras5,8.
Aunque nuestra paciente recibió EPO 80.000 UI/semana durante 40 semanas, no fue suficiente ya que tuvo que recibir 55 CH durante el tratamiento. Las causas pueden haber sido falta de tiempo de actuación, anemia de origen central, déficit de hierro o resistencia a EPO (eritropoyetina endógena <500 IU/L)5. La causa más habitual es la deficiencia de hierro. Por eso cuando los niveles de ferritina son <100 mg/dl y la saturación de transferrina <20%, se recomienda administrar hierro intravenoso para que la EPO sea efectiva5.
En los estudios solo el 3% de pacientes requiere transfusiones y no en tal cantidad2. El valor más bajo de Hb en nuestra paciente fue 4,8 g/dl, que encaja dentro del 7% de pacientes que presentó anemia grave (Hb<8,5 g/dl) en los estudios4.
En resumen, presentamos un caso de anemia refractaria y prolongada como consecuencia de triple terapia para VHC. La paciente cumplía con la mayoría de factores de riesgo de anemia asociados a boceprevir5, pero por otro lado no cumplía con los 2 parámetros predictores de complicaciones graves observados en el estudio CUPIC (Albumina sérica < 3,5 g/dl y plaquetas ≤100.000/μl)9. La anemia perduró hasta 12 semanas después de finalizar el tratamiento a pesar de suspender boceprevir (12 semanas antes de lo indicado), ajustar la dosis de RBV, administrar EPO y transfundir CH. La paciente alcanzó RVS gracias a mantener la triple terapia y a pesar de suspender boceprevir antes de lo indicado.
Esta reacción fue notificada online a través del sistema de notificación espontánea al Centro de Farmacovigilancia de la Comunidad Autónoma de Madrid.
Conflicto de intereses: Los autores declaran no tener conflictos de intereses.
Bibliografía
- Crespo G, Lens S. Uso de boceprevir y telaprevir en pacientes con VHC (aspectos prácticos). Gastroenterol Hepatol. 2012 May;35(5):337-43.
- Hézode C. Management of anaemia and other treatment complications. Dig Liver Dis. 2013 Sep 30;45 Suppl 5:S337-42.
- Jacobson IM, Kowdley KV, Kwo PY. Anemia management in the era of triple combination therapy for chronic HCV. Gastroenterol Hepatol (N Y). 2012 Sep;8(9 Suppl 6):1-16.
- Sulkowski MS, Poordad F, Manns MP, Bronowicki JP, Rajender Reddy K, Harrison SA, et al. Anemia During Treatment With Peginterferon Alfa-2b/Ribavirin and Boceprevir: Analysis From the Serine Protease Inhibitor Therapy 2 (SPRINT-2) Trial. Hepatology. 2013 Mar; 57(3):974-84.
- Romero-Gómez M, Berenguer M, Molina E, Calleja JL. Management of anemia induced by triple therapy in patients with chronic hepatitis C: challenges, opportunities and recommendations. J Hepatol. 2013 Dec; 59(6):1323-30.
- Ficha Técnica de ribavirina. Disponible en: http://www. aemps.gob.es/cima/pdfs/es/ft/73658/FT_73658.pdf.
- Mauss S, Hueppe D, Alshuth U. Renal impairment is frequent in chronic hepatitis C patients under triple therapy with telaprevir or boceprevir. Hepatology. 2014 Jan;59(1):46-8.
- Poordad FF, Lawitz EJ, Reddy KR, Nelson DR, Strader D, Thomas DL, et al. A randomized trial comparing ribavirin dose reduction vs. erythropoietin for anemia management in previously untreated patients with chronic hepatitis C receiving boceprevir plus peginterferon/ribavirin. J Hepatol. 2012;56:S559.
- Hézode C, Fontaine H, Dorival C, Larrey D, Zoulim F, Canva V, et al. Triple therapy in treatment-experienced patients with HCV-cirrhosis in a multicentre cohort of the French Early Access Programme (ANRS CO20-CUPIC)-NCT01514890. J Hepatol. 2013 Sep;59(3):434-41.