Alonso-Fito L1, Hernández-López A2
1 Unidad de dispensación a pacientes externos. Servicio de Farmacia. Complejo Asistencial de Segovia, Salud Castilla y León (SACYL). Segovia (España)
2 Unidad de dispensación a pacientes ingresados. Servicio de Farmacia. Complejo Asistencial de Segovia. SACYL. Segovia (España)
Fecha de recepción: 24/09/2018 – Fecha de aceptación: 27/12/2018
Correspondencia: Luisa Alonso Fito – Servicio de Farmacia DA Norte – C/Alfonso Rodríguez Castelao, 17 – 28035 Madrid (España)
Luisa.a.fito@gmail.com
____
Resumen
Introducción: Los antihistamínicos son uno de los grupos de medicamentos más usados en alergología, a pesar de ser medicamentos seguros y ser de los más utilizados no están exentos de reacciones adversas (RAM).
Descripción del caso: Mujer con vasculitis leucocitoclástica y déficit de diamino oxidasa (DAO) a la que se prescribe rupatadina para habones en piernas y glúteos y urticaria generalizada. Tras 15 días de administración discontinua consulta por angioedema localizado en manos que desaparece con la suspensión y reaparece al reintroducir la medicación.
Discusión: La RAM de angioedema no se encontraba descrita en la ficha técnica de la rupatadina en el momento del caso, pero si en su metabolito principal, la desloratadina1. En los últimos años esta RAM se ha añadido a la ficha de varios antihistamínicos de nueva generación (bilastina, rupatadina, desloratadina), por lo que a pesar de su la baja frecuencia, parece razonable valorar la posibilidad de que el riesgo de angioedema sea una RAM de clase en antihistamínicos de nueva generación.
Palabras clave: Rupatadina, antihistamínicos, reacción adversa, angioedema, histaminasa.
Rupatadine related angioedema in an histaminase deficient patient
Summary
Background: Antihistamines are one of the most used medications in allergology, despite being safe medications are not exempt from adverse drug reactions (ADR).
Case report: Woman with leukocytoclastic vasculitis and a deficit of diamine oxidase enzyme (DAO) who was prescribed rupatadine for hives in the legs and gluteus and generalized urticaria. After 15 days of discontinuous administration, consulted for localized angioedema in the hands that disappears with the suspension and reappears when the medication is reintroduced.
Discussion: The ADR of angioedema was not described in product characteristics of rupatadine at the time of the case, evaluating the metabolites of rupatadine it was observed that its main metabolite, desloratadine1, presented this reaction. In recent years this ADR has been added to the summary of several new generation antihistamines (bilastine, rupatadine, desloratadine), so despite its low frequency, it seems reasonable to assess the possibility that the risk of angioedema is a ADR of class in new generation antihistamines.
Key Words: Rupatadine, antihistamine, angioedema, drug adverse reaction, histaminasa.
Introducción
Los antihistamínicos antih1 se han convertido en uno de los grupos farmacoterapéuticos de uso más común, especialmente de forma estacional bien sea por prescripción médica como por recomendación farmacéutica o incluso a través de la automedicación.
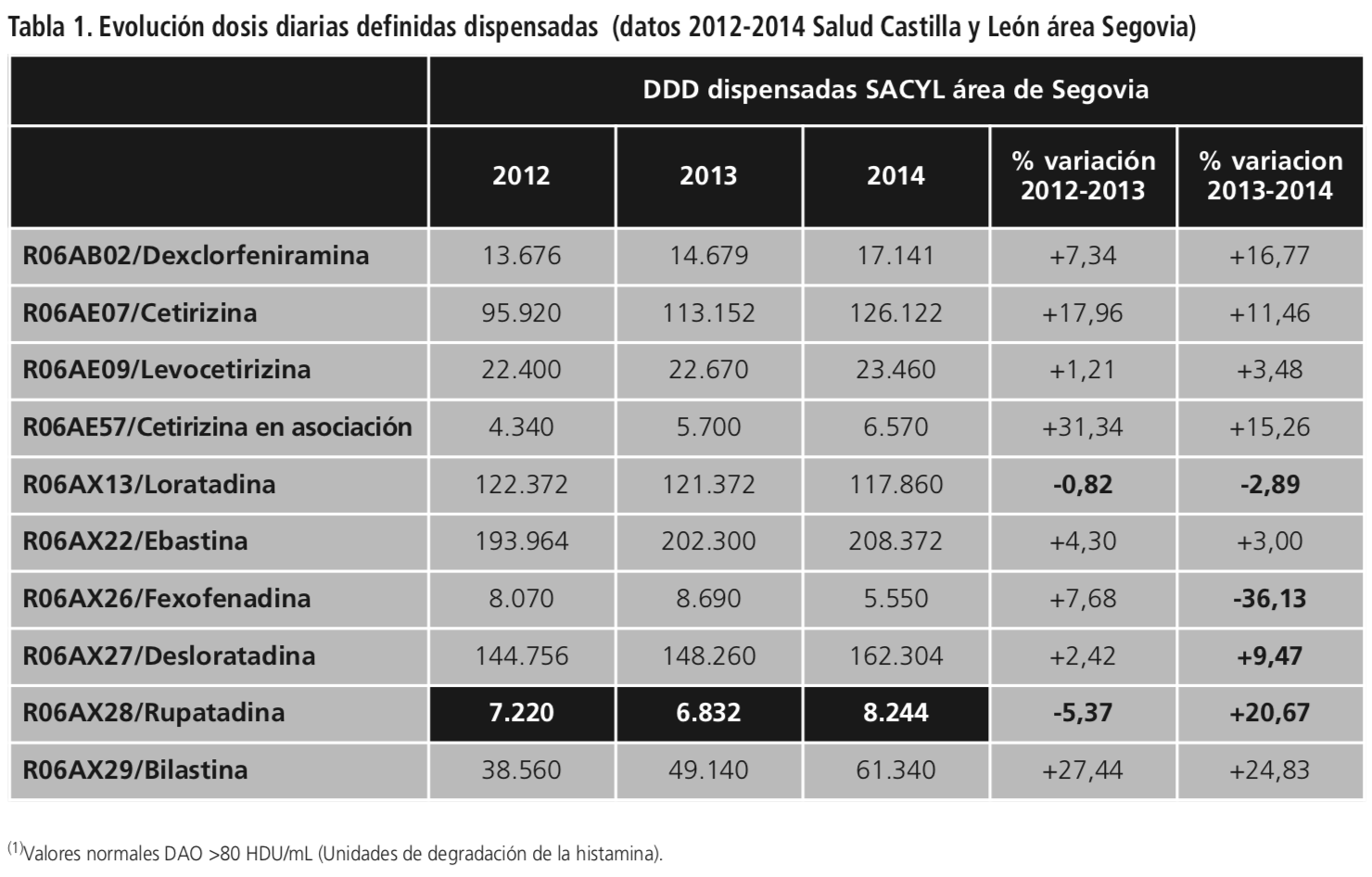
En los últimos 10 años en España se ha autorizado la comercialización de varias moléculas antih1 de nueva generación como rupatadina, bilastina, desloratadina… y pasados los primeros 5 años post-autorización ya no se encuentran sometidos a vigilancia adicional. La tendencia al aumento de la prescripción de estas moléculas en estos últimos años (Tabla 1), facilita que sigan apareciendo reacciones adversas poco frecuentes o nuevas que son de obligada declaración y que pueden dar lugar a la modificación de la ficha técnica.
La ficha técnica de rupatadina incluía como RAM poco frecuentes influenza, nasofaringitis, infecciones de tracto respiratorio superior, eosinofilia, neutropenia, mareo, náuseas, eczema, sudores nocturnos, fatiga y como efectos frecuentes cefalea y somnolencia4.
El cuadro de angioedema localizado que desaparece y reaparece con la suspensión y reintroducción de la rupatadina hace pensar en la aparición de un efecto adverso que no se encuentra incluido en la ficha técnica.
Informe del caso
Mujer, de 32 años y 65 kg de peso y 1,55 cm, con presencia de habones localizados en piernas y glúteos, urticaria, migrañas, congestión nasal, alteraciones intestinales hinchazón y saciedad precoz, historial de TDAH y diagnóstico de vasculitis leucocitoclástica en tratamiento con levoceritizina 10 mg comprimidos v.o. cada 12h durante 15 días para la reacción de urticaria y la aparición de los habones.
Debido a la persistencia de estos síntomas alérgicos, que no ceden con el antihistaminico prescrito, su alergóloga sustituye la levocetirizina por rupatadina 10 mg comprimidos cada 12h. Ante la sospecha de déficit de Diamino oxidasa (EC1.4.3.22; DAO) se solicitó para la paciente análisis de sangre para determinación de actividad de DAO que dio como resultado, 28 HDU/ml. (1)Una vez obtenido este resultado, para la confirmación, se realizó una determinación del genotipo2 y una biopsia intestinal en la que se confirmó el diagnóstico siendo la paciente poseedora del alelo, que dentro de los 7 polimorfismos encontrados para este gen, ha demostrado déficit de actividad (rs1049793). Se descartó en el mismo proceso condición celiaca, resultando HLA-DQ2/DQ8 negativa.
La paciente inicia, por prescripción, tratamiento con Migrasín® comprimidos v.o. 1/12h, un complemento alimenticio que incluye DAO encapsulada, más rupatadina 10 mg comprimidos v.o. (1/12h). A los 5 días de iniciar el tratamiento tomando un total de 10 dosis (100 mg), observa un importante angioedema localizado en ambas manos que relaciona con su patología basal y continúa tomando la medicación (Figuras 1 y 2). Por circunstancias la paciente no puede adquirir un nuevo envase y retoma la prescripción inicial de levocetirizina 10 mg comprimidos manteniendo la pauta inicialmente prescrita (1/12h), a las 48h el angioedema localizado desaparece.
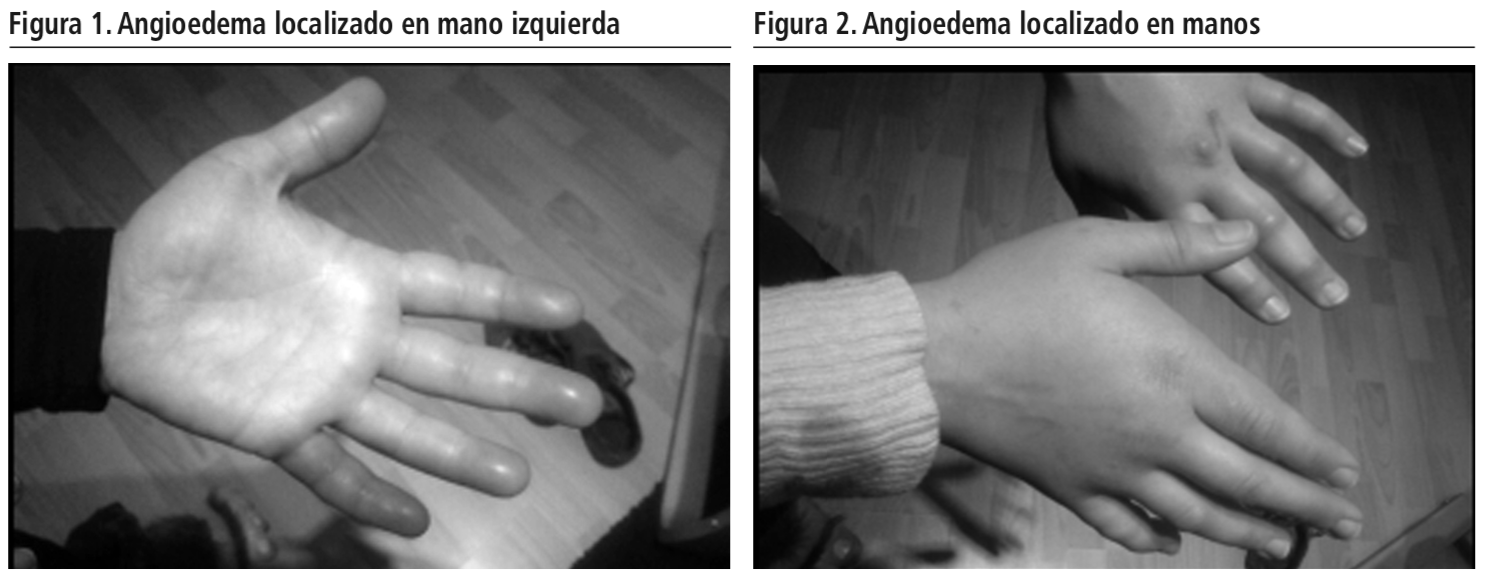
Cuando reintroduce la rupatadina 10 mg a los 3 días (tras 6 dosis), reaparece el angioedema con mayor intensidad, y la paciente acude al personal de nuestro Servicio de Farmacia a pedir consejo. Durante la consulta se establece la conveniencia de la suspensión de la rupatadina ante la posible relación causal (algoritmo de Naranjo “probable”) y el aumento de la intensidad de los síntomas con la reintroducción. Se realizó una búsqueda exhaustiva y se comprobó que, la aparición de angioedema, a pesar de no estar descrita en ficha técnica de rupatadina sí lo está en la de su metabolito mayoritario, la desloratadina, por lo que se emite un informe de recomendación para valoración por su alergóloga que una vez analizada la relación clínicamente contraindica la toma de rupatadina, desloratadina y loratadina. La reacción adversa desaparece tras 5 días de suspensión del tratamiento.
Se le pide su consentimiento para emplear las fotos, y la información facilitada para el caso.
Discusión
La ficha técnica de rupatadina, indica que se metaboliza casi por completo a nivel intestinal, dando lugar a varios metabolitos activos, en un 85% desloratadina, en cuyo caso sí se ha descrito angioedema como efecto adverso de frecuencia rara. Esta reacción adversa fue añadida a la sección 4.8 de la ficha técnica en una modificación de 2004 tras un informe de la Agencia Europea del Medicamento (EMA)3,5. La aparición de alergias medicamentosas y reacciones adversas relacionadas con los metabolitos medicamentosos es de sobra conocida, por lo que valorar las reacciones adversas aparecidas en los principales metabolitos de un medicamento cuando están comercializados como tales es una práctica habitual. En los últimos años esta RAM se ha añadido a la ficha de varios antihistamínicos de nueva generación bilastina (2018)6, rupatadina (2017), desloratadina (2004), ebastina (2014), por lo que pesar de su la baja frecuencia de aparición, parece razonable valorar la posibilidad de que el riesgo de angioedema sea una RAM de clase en antihistamínicos de nueva generación.
Se valoró la posible causalidad de Migrasin® (diaminoxidasa encapsulada) quedando descartada ya que la paciente continuó tomando el complejo alimenticio sin presentar sintomatología durante meses después de la reacción adversa.
Esta reacción adversa fue notificada al centro de farmacovigilancia correspondiente.
Agradecimiento: Las autoras agradecen su colaboración a Rafael Aguileña Vizcaíno por su colaboración.
Conflicto de intereses: Las autoras declaran no tener conflicto de intereses.
BIBLIOGRAFÍA
1. Sun C, Li Q, Pan L, Liu B, Gu P, Zhang J, et al. Development of a highly sensitive LC-MS/MS method for simultaneous determination of rupatadine and its two active metabolites in human plasma: Application to a clinical pharmacokinetic study. J Pharm Biomed Anal. 2015;111:163-8.
2. Schwelberger HG. Histamine intolerance: a metabolic disease? Inflamm Res. 2010;59:219-221.
3. Informe EPAR (EMEA) Aerius® consultado el 04/4/2018 disponible en http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Product_Information/human/000313/WC500025540.pdf.
4. FICHA TÉCNICA RUPATADINA (AEMPs) [citada 08 de agosto 2018], disponible en http://www.aemps.gob.es/cima/pdfs/es/ft/75990/FT_75990.pdf.
5. FICHA TÉCNICA DESLORATADINA (AEMPs) [citada el 08 de julio 2018], disponible en http://www.ema.europa.eu/docs/es_ES/document_library/ EPAR_-_Product_Information/human/000313/WC500025540.pdf.
6. FICHA TÉCNICA DE BILASTINA (AEMPs) [citada el 08 de julio 2018] disponible en: https://www.aemps.gob.es/cima/dochtml/ft/73027/FichaTecnica_73027.html.
____
