Rev. OFIL 2018, 28;1:37-42
Fecha de recepción: 10/01/2018 – Fecha de aceptación: 15/01/2018
González-Haba Peña E1, Gaspar Carreño M2
1 Farmacéutica Especialista en Farmacia Hospitalaria. Grupo de Farmacia Oncológica de la Sociedad Española
de Farmacia Hospitalaria (SEFH). Hospital General Universitario Gregorio Marañón. Madrid (España)
2 Farmacéutica Especialista en Farmacia Hospitalaria. Grupo de Productos Sanitarios (GPS) de la Sociedad Española de Farmacia Hospitalaria (SEFH). Hospital Intermutual de Levante. Valencia (España)
____
Correspondencia:
Eva González-Haba Peña
Hospital General Universitario Gregorio Marañón
(Servicio de Farmacia)
C/Dr. Esquerdo, 46
28007 Madrid
Correo electrónico: eva.gonzalezhaba@salud.madrid.org
____
Resumen
La exposición laboral a medicamentos y productos peligrosos (MPP) con propiedades carcinogénicas, mutagénicas, teratogénicas y/o tóxicas para la reproducción, debe ser una preocupación para los responsables del correcto uso de los medicamentos en el ámbito sanitario.
A pesar de que los fármacos antineoplásicos constituyen el grupo más importante de MPP, hay un gran número de medicamentos de otros grupos terapéuticos que presentan una toxicidad y unos riesgos similares a los medicamentos antitumorales. Por tanto el número de profesionales y áreas clínicas afectados por el problema es mucho mayor de lo considerado de forma habitual.
En este sentido, una de las causas más habituales de contaminación por MPP, es la utilización de agujas y sistemas de transferencia de medicamentos convencionales que favorecen la formación de aerosoles, la liberación de vapores o el goteo del medicamento, o la punción accidental, en las distintas fases de la preparación y administración.
Es por ello, que para garantizar la reducción en el nivel de exposición de los manipuladores hasta el nivel técnicamente más bajo posible se recomienda, además del uso de salas blancas con cabinas de seguridad biológica (CSB) y equipos de protección individual (EPI), el empleo de sistemas cerrados de transferencia de medicamentos (SCTM) tanto en la preparación como en la administración.
En España, así como en el resto de Europa no existe regulación específica sobre los SCTM. En nuestro país estos equipos son considerados productos sanitarios, regulados por el RD 1591/2009, y clasificados en la clase IIa. Por ello es necesario avanzar en la evaluación y recomendaciones de uso de estos dispositivos.
Palabras clave: Medicamento peligroso, sistema cerrado de transferencia de medicamentos, agentes antineoplásicos, preparación de medicamentos, administración, exposición ocupacional.
____
Introducción
A pesar de que los fármacos antineoplásicos constituyen el grupo más importante de medicamentos y productos peligrosos (MPP), hay un gran número de medicamentos de otros grupos terapéuticos que presentan una toxicidad y unos riesgos similares a los medicamentos antitumorales, y por tanto el número de profesionales y áreas clínicas afectados por el problema es mucho mayor al considerado de forma habitual.
Una de las causas más habituales de contaminación por MPP, es la utilización de agujas y sistemas de transferencia de medicamentos convencionales que favorecen la formación de aerosoles, la liberación de vapores, el goteo del medicamento, o los accidentes por punción, en las distintas fases de la preparación y administración.
Es por ello, que para intentar reducir el nivel de exposición de los manipuladores se recomienda el empleo de sistemas cerrados de transferencia de medicamentos (SCTM) tanto en la preparación como en la administración de MPP.
Los SCTM son dispositivos en los que el MPP no entra en contacto con el medio externo, ni en la fase de preparación, ni en la fase de administración y son los sistemas recomendados y promovidos por diversos organismos internacionales de reconocido prestigio, organizaciones científicas y fabricantes para la preparación y administración de los MPP1.
Exposición ocupacional a medicamentos y productos peligrosos (MPP)
En términos de exposición ocupacional, un MPP, se entiende como un agente que contiene algún principio activo cuya toxicidad inherente representa un cierto tipo de riesgo para la salud del personal sanitario que va a manipularlo.
La peligrosidad de estos medicamentos se comprende según el riesgo químico, en concreto relacionado con la actividad carcinogénica, teratogénica, genotóxica y tóxica sobre el proceso reproductivo o sobre un órgano concreto a dosis bajas, o por tratarse de un nuevo fármaco similar a otros con este tipo de riesgos (criterios peligrosidad NIOSH)2.
En este sentido, a los MPP les son de aplicación las normas referentes a la protección de los trabajadores relacionadas con la exposición a agentes químicos (RD 374/2001)3, agentes cancerígenos (RD 665/1997)4 y los riesgos de exposición a agentes carcinogénicos o mutágenos durante el trabajo (Directiva 2004/37/CE)5.
En España, la protección de los trabajadores frente a riesgos relacionados con la exposición a agentes cancerígenos o mutágenos está legislada por el RD 665/19974 y su posterior modificación por el RD 1124/20006 y el RD 349/20037. En él, se recoge algunos aspectos citados en las normas internacionales como que “… en la medida en que sea técnicamente posible, el empresario evitará la utilización en el trabajo de agentes cancerígenos, en particular mediante su sustitución por una sustancia, un preparado o un procedimiento que, en condiciones normales de utilización, no sea peligroso ….” (Artículo 4) o “En caso de que no sea técnicamente posible sustituir el agente cancerígeno. El empresario garantizará que la producción y utilización del mismo se lleven a cabo en un sistema cerrado” (Artículo 5, pto 2) y “Cuando la aplicación de un sistema cerrado no sea técnicamente posible, el empresario garantizará que el nivel de exposición de los trabajadores se reduzca a un valor tan bajo como sea técnicamente posible.” (Artículo 5, pto 3).
Con posterioridad al RD 665/1997, el Instituto Nacional de Seguridad e Higiene en el Trabajo, ha publicado dos Notas Técnica de Prevención relacionadas con el tema –la NTP 7408 y NTP 10519– y el Documento Técnico sobre Medicamentos Peligrosos donde se presenta la relación de medicamentos clasificados como peligrosos de uso habitual en España, recomendaciones sobre su manipulación, las medidas de prevención asociadas y, en su caso, equipos de protección individual que se deben utilizar10.
Dado que no han podido establecerse de forma clara los efectos tóxicos a largo plazo de la exposición a estos fármacos, el posible riesgo laboral que supone su manipulación y las consecuencias derivadas, resulta imprescindible adoptar medidas que ayuden a reducir esta exposición y a garantizar unas condiciones óptimas de trabajo. En este sentido, la actividad más adecuada es la preventiva. Tal como queda establecido en el artículo 15 de la Ley de Protección de Riesgos Laborales LPRL11 referente a los principios de la acción preventiva, la adopción de medidas de protección colectiva, tanto técnica como organizativa, debe anteponerse a la protección individual.
Además de la estructura de recursos humanos, con competencias y capacitación acreditadas, el manejo seguro de MPP requiere una estructura física apropiada. Es necesario disponer no solo de las principales medidas técnicas de prevención primaria, tales como instalaciones, salas blancas y cabinas de seguridad biológica (CSB) y SCTM, sino también de medidas de prevención secundaria como los equipos de protección individual (EPI)12. No obstante, para prevenir los posibles efectos nocivos de una manipulación inadecuada de MPP, se considera clave aplicar las medidas organizativas de prevención primaria colectiva que deben incluir, como mínimo, la aplicación de una sistemática de trabajo apropiada, la validación de técnicas de manipulación específicas, el establecimiento de procedimientos normalizados de trabajo que contemplen todas las fases de la manipulación de los MPP y limpieza de las instalaciones, así como las medidas de actuación frente a cualquier situación de riesgo excepcional.
Sistemas cerrados de transferencia de medicamentos
Para garantizar la reducción de la exposición a los MPP de los manipuladores hasta el nivel técnicamente más bajo posible se recomienda, el empleo de sistemas cerrados tanto en la preparación como en la administración. Se trata de dispositivos en los que el MPP no entra en contacto con el medio externo, desempeñando un papel fundamental en la protección del personal manipulador frente a los efectos nocivos, no solo de los fármacos antineoplásicos, sino de todos los fármacos que por su toxicidad representan un posible peligro para la salud del personal sanitario.
A su vez, el uso de estos sistemas se encuentra íntimamente relacionado con la práctica de seguridad promovida desde la Unión Europea para evitar pinchazos accidentales por utilización de dispositivos punzantes, tanto en la preparación como en la administración de los medicamentos (Directiva Europea 2010/32/UE)13.
NIOSH, en la alerta del año 20042, define un dispositivo cerrado de transferencia de fármacos (closed-system drug-transfer device, CSTD) como un sistema que mecánicamente no permite la transferencia de contaminantes ambientales dentro del dispositivo, ni el escape de fármacos de alto riesgo o sus vapores fuera del mismo. La definición del NIOSH es la única que contempla la posibilidad de formación de vapores de un determinado fármaco. La definición de un CSTD también se aplica a la administración de tratamientos peligrosos.
La International Society of Oncology Pharmacy Practitioners (ISOPP) recomienda el uso de SCTM durante la preparación y dispositivos de contención (antigoteo y herméticos) para la administración de fármacos citotóxicos, y distingue entre un sistema cerrado en el contexto de contaminación microbiológica y un sistema cerrado en el contexto de contaminación química y exposición laboral. Los estándares ISOPP para el manejo seguro de antineoplásicos coinciden en que la definición NIOSH es la más amplia y concreta, ya que en la reconstitución de MPP preocupa tanto la contaminación microbiológica como la exposición a fármacos de alto riesgo14.
La NTP 10519, adaptando las definiciones que dan NIOSH2 y la ISOPP14 denominan SCTM a los dispositivos que impiden el intercambio de aire no filtrado o de contaminantes con el aire ambiente. Los SCTM comprenden tres partes necesarias para la elaboración de MPP: el punzón o protector que se acopla en el vial; el inyector o conector de jeringa que permite extraer la medicación del vial y el dispositivo de transferencia que permite la transferencia a la bolsa de infusión15.
Con el uso de los SCTM durante el proceso de elaboración se evita la formación de aerosoles e idealmente vapores mediante diferentes sistemas que permiten igualar las presiones dentro y fuera del vial. Hay dos tipos de sistemas, los de filtración, que disponen de un filtro de aire hidrófobo que evita el incremento de la presión interna del vial, permitiendo el intercambio adecuado de aire durante el proceso de extracción de la medicación y los de barrera, que disponen de diferentes mecanismos (cámara de ecualización, doble aguja) que permiten igualar las presiones dentro y fuera del vial.
Es necesario que los SCTM se usen correctamente, y se cumplan los procedimientos de asepsia, para poder garantizar la estabilidad microbiológica del medicamento que se está manipulando.
La farmacopea de los Estados Unidos en su normativa de manipulación de fármacos peligrosos (USP 800), obliga a utilizar sistemas cerrados en la administración de fármacos peligrosos, y lo recomienda en la elaboración siempre que las formas farmacéuticas lo permitan16.
Diversos estudios han demostrado la eficacia de los SCTM en la minimización de la contaminación ambiental. No obstante, no se han establecido test específicos para evaluar los criterios que tienen que cumplir los sistemas cerrados17-23.
El tipo de SCTM seleccionado es un elemento muy importante en la contaminación que se genera en la preparación. No obstante, no hay que olvidar que hay un conjunto de factores que también van a influir de manera muy importante: las instalaciones donde se realizan las preparaciones de MPP (salas limpias y CSB), el mantenimiento adecuado de las instalaciones, el entrenamiento del personal, el EPI, los protocolos de manipulación y los protocolos de descontaminación24. Por tanto, si queremos asegurar el nivel técnicamente más bajo posible, no podemos descuidar ninguno de estos aspectos25.
La USP 800 reconoce la importancia de la realización de estudios de SCTM y no considerarlos simplemente como sistemas intercambiables16. En reconocimiento de esas diferencias NIOSH está actualmente desarrollando un protocolo con un marcador que le permita evaluar tanto a los sistemas cerrados de filtración como a los de barrera, sin que hasta la fecha esté disponible26. Por tanto, aunque en la NTP 1051 se cuestiona la utilidad de los SCTM que utilizan filtros de venteo por la posibilidad de no retener vapores, NIOSH está interesado en encontrar un marcador que presente características físico-químicas similares a los MPP. Afortunadamente, la mayor parte de los MPP no están en estado de vapor a la temperatura ambiente.
En Estados Unidos, la FDA tiene establecido el código de producto ONB (optimal normal basis) para los SCTM destinados a su aplicación intravascular y que define como los que en el ámbito sanitario permiten la reconstitución y transferencia de antineoplásicos y medicamentos peligrosos reduciendo la exposición del personal sanitario. Puede que un equipo sea ONB solamente para alguna de las fases de trabajo o para todas. En cuanto a la administración, no hay establecido específicamente un código que nos permita conocer el nivel de seguridad.
La FDA requiere que los dispositivos cumplan los siguientes criterios: hermético, antigoteo y que prevenga la contaminación microbiológica. Por el momento no se han establecido test específicos para evaluar dichos criterios, si bien se les pueden solicitar datos que avalen que su uso reduce la exposición del personal expuesto a los MPP.
En España estos equipos son considerados productos sanitarios, regulados por el RD 1591/200923, y clasificados en la clase IIa.
A diferencia de lo que sucede en Estados Unidos, en nuestro país, como en el resto de la Comunidad Europea, no existe regulación específica sobre los sistemas cerrados, y por tanto, en el caso de dispositivos que exclusivamente se comercializan y distribuyen en Europa desconocemos si se deberían utilizar en la manipulación y manejo de MPP.
Es importante comprender que no todos los sistemas de preparación y administración son igualmente capaces de proteger a los trabajadores de la exposición a MPP, de ahí la importancia de seleccionarlos de forma adecuada.
Contaminación ambiental por medicamentos peligrosos: de la preparación a la administración
A pesar de que varios estudios de contaminación de superficies han confirmado que la mayor exposición a MPP, como son por ejemplo los fármacos citostáticos, se produce durante la preparación de las mezclas en la cabina de seguridad biológica (CSB) y/o en las salas limpias27,28, se ha puesto de manifiesto que en las zonas de administración también se pueden detectar concentraciones de estos fármacos. Es de esperar que el riesgo de exposición sea mayor durante la preparación, ya que, para conseguir las dosis individualizadas por paciente, se reconstituyen y/o diluyen los fármacos concentrados. No obstante, en la zona de administración la manipulación es menor, ya que habitualmente los fármacos llegan diluidos, pero también existe un potencial riesgo de exposición, además el nivel de protección es inferior que en las zonas de preparación.
Los profesionales sanitarios que trabajan elaborando estas mezclas tienen un alto nivel de protección tanto en relación a las medidas colectivas como son las instalaciones que utilizan durante la elaboración, como las medidas de protección individuales, como EPIs y los SCTM de preparación y administración de MPP. Dichos sistemas son críticos tanto para que los tratamientos lleguen a las zonas de administración libre de contaminantes, como para garantizar una administración segura.
Por tanto, es también necesario que durante la administración de los MPP se establezcan procedimientos que aseguren la menor exposición posible. Para ello es fundamental aplicar una sistemática de trabajo apropiada, que la preparación de la mezcla se realice de tal manera que quede lista para su administración sin requerir manipulación posterior y garantizando, además de la composición y estabilidad, la seguridad del personal que los prepara y que posteriormente los administra, así como la prevención de la contaminación ambiental.
Durante la administración existe riesgo de exposición accidental a estos medicamentos al purgar y desconectar las vías de infusión. En este sentido, la utilización de sistemas de contención para administración, evita de forma mecánica, tanto la transferencia de contaminación ambiental dentro del sistema, como la salida del medicamento de alto riesgo o concentraciones de vapor fuera del mismo.
En la fase de administración se debe asegurar que las conexiones entre las mezclas con MPP y la vía del paciente son estancas, reduciendo al máximo el riesgo de desconexiones accidentales, salpicaduras o eliminación de vapores al ambiente.
Aunque cada dispositivo tiene un diseño distinto, todos ellos se basan en proporcionar conexiones herméticas entre los componentes del sistema y en retener los posibles aerosoles o derrames en cámaras estancas diseñadas al efecto. En general se ofrecen como sistemas de varios componentes para las distintas operaciones, compatibles entre sí pero no siempre compatibles con dispositivos de otros sistemas o proveedores.
Administración de medicamentos peligrosos
1. Consideraciones generales
La evaluación de la seguridad durante la administración es un aspecto mucho menos estudiado que la seguridad en la preparación de MPP. Sería necesario realizar estudios que garanticen la seguridad con los diferentes tipos de sistemas cerrados de administración disponibles.
Habitualmente cuando se administra un esquema de quimioterapia se empieza con una pre-medicación que en ocasiones incluye hidratación, a continuación, los fármacos antineoplásicos y posteriormente suero limpio tras cada uno de los fármacos para asegurar que se administra la dosis completa de cada fármaco, para lavar la vía y proceder a una desconexión de seguridad al finalizarlo. El purgado de la línea de infusión del paciente también se debe realizar con suero limpio para minimizar el contacto directo con estos fármacos.
Aunque todos estos sistemas se han diseñado y se vienen específicamente utilizando para la quimioterapia, su uso se debería extender para la administración de MPP que, aunque se administren de forma única, debería procederse también por seguridad, a un purgado de la línea previa y posterior a la infusión del fármaco.
Independientemente del sistema de administración cerrado que se vaya a utilizar, la administración de estos fármacos se debería realizar con bombas de perfusión de flujo controlado, para que, tras la desconexión de la vía del paciente, no se produzcan goteos. Estos sistemas se conectan a la vía de paciente mediante conexiones luer-lock.
En cuanto a las características de los materiales de los sistemas de administración deben cumplir entre otros, el no contener látex ni DEHP (Di2-etilhexilftalato) en todo el dispositivo que está en contacto con la medicación, además debe asegurarse la compatibilidad de los materiales que lo componen con la medicación que va a ser administrada.
También debemos tener en cuenta que en el mercado hay bolsas y frascos de infusión que disponen de conexiones convencionales, y bolsas de infusión con conexiones luer que condicionan los diferentes sistemas cerrados de preparación y administración de MPP.
2. Modalidades de administración de medicamentos peligrosos.
En nuestro país tenemos disponible dos sistemas diferentes de administración de MPP: el sistema tipo árbol (Figura 1), y el sistema valvular, que consta de una única línea de infusión (Figura 2).
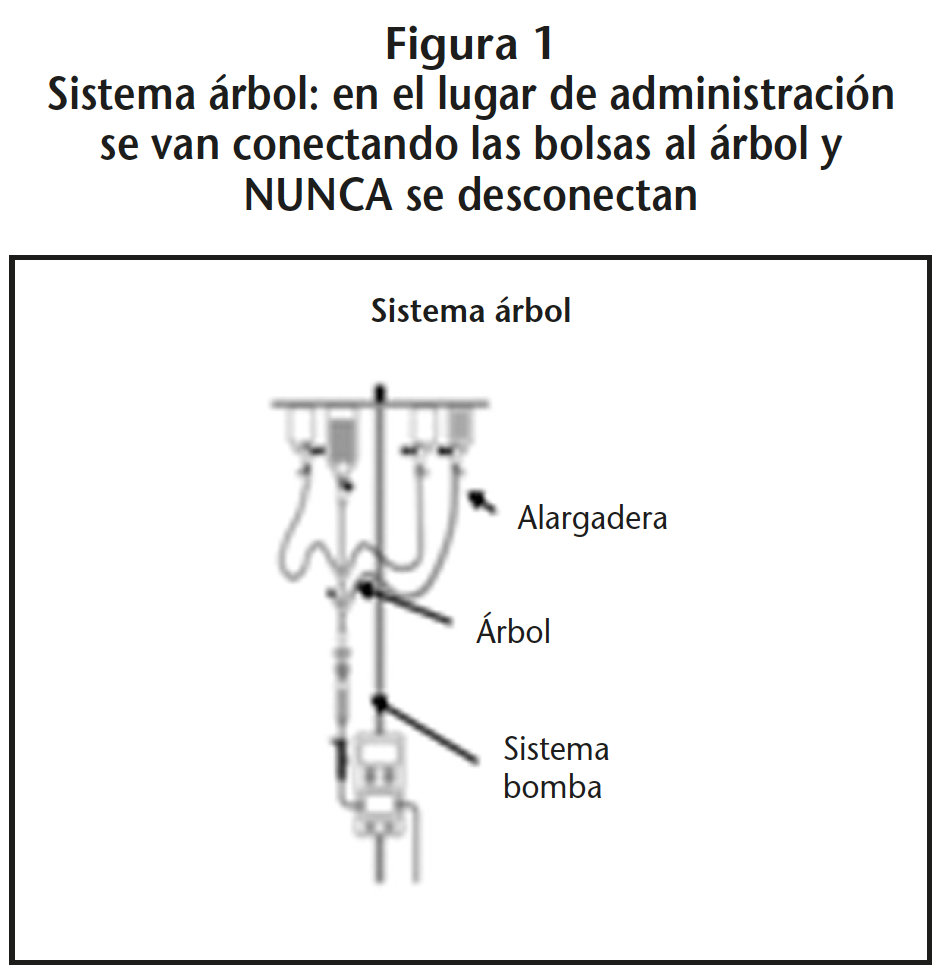
2.2. Sistemas tipo árbol
La elección de una arquitectura tipo “árbol” implica utilizar un dispositivo que tiene un trocar o punzón proximal para conectar una solución de mantenimiento y lavado y que dispone de varias conexiones valvulares en “Y”, entre 2 y 4, donde se insertan las preparaciones. El punzón de la línea principal se conecta a un suero de lavado que permite limpiar la línea de infusión entre la administración de diferentes mezclas. Algunos de estos sistemas disponen de un adaptador para incorporar el sistema de infusión, y otros tienen el sistema de infusión ya incorporado.
Las premedicaciones o las soluciones de hidratación se conectan al punzón del árbol previo a la administración del tratamiento. Las distintas bolsas o frascos de infusión de MPP se conectan en las válvulas de seguridad del árbol. Es imprescindible que se dispensen desde el Servicio de Farmacia (SF) con una alargadera denominada línea secundaria, purgada con un suero limpio. Esta línea secundaria debe reunir una serie de características para que se pueda considerar segura:
– Punzón que garantice la no salida de fluidos del interior de la bolsa hacia el exterior.
– Puerto para transferencia de fármaco con válvula bidireccional de seguridad, que garantice que no hay goteos del interior del contenedor hacia el exterior al desconectar la jeringa.
– Luer macho giratorio con válvula antirreflujo incorporada (evita efecto vasos comunicantes) y tapón hidrófobo que facilita el purgado, eliminando el aire y evitando el goteo. En el caso de que la válvula antirreflujo esté incorporada en el equipo o sistema de infusión, no será exigible que también lo esté en este luer macho
– Pinza (clamp) de seguridad para evitar la transferencia del fármaco hacia la zona de conexión con el árbol. Es muy importante que este sistema secundario salga pinzado, para minimizar que el fármaco pueda llegar a la zona de conexión.
Una vez están preparados todos los contenedores de los fármacos (frascos o bolsas de infusión) para un tratamiento, estas líneas se conectarán para ser administrados a través los puertos de conexión. Previo a la administración se abrirá la pinza (clamp) de la alargadera para permitir la infusión en el orden establecido de los diferentes fármacos.
A través del trocar proximal, donde está conectado el contenedor del suero limpio, se podrá realizar el lavado del sistema después de la administración de cada fármaco.
Ninguna de las bolsas o frascos de fármacos peligrosos debe ser desconectado de las válvulas de seguridad (a menos que se trate de árboles con conexiones secas), de modo que una vez finalizada la sesión se desecharán las bolsas o frascos vacíos con sus alargaderas, el sistema de árbol y el de infusión.
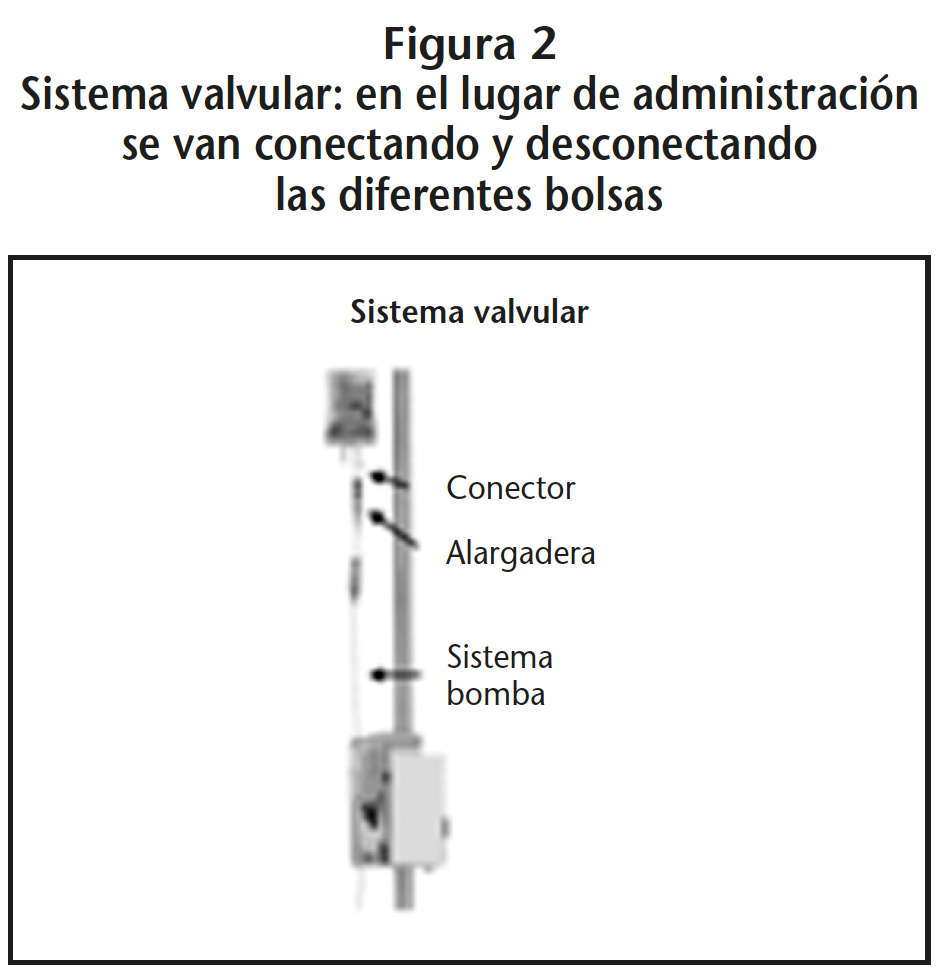
2.3. Sistemas valvulares
Los sistemas valvulares consisten en un sistema de administración de una única línea de infusión con un dispositivo que permite conectar una a una las diferentes mezclas que conforman el tratamiento del paciente mediante conexiones y desconexiones que deben ser seguras.
El MPP se envía elaborado desde el SF en una bolsa o frasco con un dispositivo que dispone de una válvula de seguridad, que no requiere alargadera, y por tanto que no es necesario purgar con suero.
Previo a la administración se conecta la bolsa o frasco al sistema de infusión que dispondrá de otro dispositivo con una válvula, con la que se podrá realizar la conexión macho-hembra. Habitualmente este dispositivo va unido a una alargadera, que se ha conectado previamente a un sistema de administración de bomba mediante su ajuste irreversible al punzón del sistema de infusión.
Dado que teóricamente este sistema permite hacer conexiones y desconexiones en un ámbito cerrado, una vez infundida la medicación de una bolsa o frasco, se desconecta y se desecha. A continuación, se conecta a través del dispositivo la siguiente medicación. De esta forma se administra tanto la pre-medicación, hidratación, los MPP y las soluciones de lavado.
Tanto la pre-medicación como los sueros de hidratación/lavado requerirán por tanto disponer del dispositivo que permite la conexión con el sistema de infusión.
2.4. Comparativa de sistemas árboles versus valvulares
Los sistemas de administración de árbol presentan como ventaja la seguridad en el proceso de administración, ya que no hay desconexiones que incrementen el riesgo de exposición a fármacos peligrosos como ocurre con los sistemas valvulares. No obstante, los árboles presentan como inconveniente el riesgo de derrames accidentales en caso de olvidos al pinzar el sistema secundario. Los que utilizan en la preparación sistemas diseñados para minimizar la contaminación química es más probable que lleguen a la zona de administración con menor nivel de contaminación. Los sistemas valvulares son más sencillos e intuitivos, pero hay pocos estudios que evalúen su seguridad. Sabemos que los que utilizan válvulas de seguridad que no están diseñadas para contener la contaminación química (sistema valvular Texium®, ChemoCLAVE®)29, producen contaminación en los puntos críticos en la desconexión.
Conclusiones
Para garantizar la reducción en el nivel de exposición de los manipuladores de MPP hasta el nivel técnicamente más bajo posible es necesario el empleo de SCTM tanto en la preparación como en la administración, de ahí la importancia de seleccionarlos de forma adecuada.
En España, así como en el resto de Europa no existe regulación específica sobre los SCTM, por lo que es necesario avanzar en la evaluación y recomendaciones de estos dispositivos, así como en el establecimiento de los test específicos que permitan evaluar los criterios que tienen que cumplir dichos SCTM.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
Bibliografía
- Alonso Herreros JM, Cercós Lletí AC, Gaspar Carreño ML, González-Haba Peña E, Márquez Peiró J, Pernía López MS. Estructura para la manipulación segura de Medicamentos Peligrosos: recomendaciones sobre instalaciones, sistemas cerrados y equipos de protección individual. En: Medicamentos Peligrosos. Monografías de Farmacia Hospitalaria y Atención Primaria. Sociedad Española de Farmacia Hospitalaria SEFH. 2016.
- Howard J. Preventing occupational exposure to antineoplastic and other hazardous drugs in health care settings. Publication Number 2004-165. Cincinnati: The National Institute for Occupational Safety and Health (NIOSH); 2004.
- Real Decreto 374/2001, sobre la protección de la salud y seguridad de los trabajadores contra los riesgos relacionados con los agentes químicos durante el trabajo. (BOE núm. 104, de 1-05-2001).
- Real Decreto 665/1997, sobre la protección de los trabajadores contra los riesgos relacionados con la exposición a agentes cancerígenos durante el trabajo. (BOE núm. 124, 24/05/1997).
- Directiva 2004/37/CE del parlamento europeo y del consejo relativa a la protección de los trabajadores contra los riesgos relacionados con la exposición a agentes carcinógenos o mutágenos durante el trabajo. (DOUE núm. 158, de 30-04-2004).
- Real Decreto 1124/2000, de 16 de junio, por el que se modifica el Real Decreto 665/1997, de 12 de mayo, sobre la protección de los trabajadores contra los riesgos relacionados con la exposición a agentes cancerígenos durante el trabajo. (BOE núm. 145, 17/06/2000).
- Real Decreto 349/2003, de 21 de marzo, por el que se modifica el Real Decreto 665/1997, de 12 de mayo, sobre la protección de los trabajadores contra los riesgos relacionados con la exposición a agentes cancerígenos durante el trabajo. (BOE núm. 82 de 5 de abril de 2003).
- Guardino Solá X, Rosell Farrás MG, Galisteo Manzanares M. NTP 740: Exposición laboral a citostáticos en el ámbito sanitario. Instituto Nacional de Higiene y Seguridad en el Trabajo. 2006.
- Guardino Solá, X. NTP 1051 Exposición laboral a compuestos citostáticos: sistemas seguros para su preparación. Instituto Nacional de Higiene y Seguridad en el Trabajo. 2015.
- Medicamentos peligrosos. Medidas de prevención para su preparación y administración. Instituto Nacional de Seguridad e Higiene en el Trabajo (INSHT). Barcelona, septiembre 2016.
- Ley 31/1995, de 8 de noviembre, de Prevención de Riesgos Laborales. BOE de 10 de noviembre de 1995.
- Real Decreto 1407/1992, de 20 de noviembre, por el que se regulan las condiciones para la comercialización y libre circulación intracomunitaria de los equipos de protección individual. (BOE núm. 311, de 28 de diciembre de 1992).
- Directiva 2010/32/UE del Consejo, que aplica el acuerdo marco para la prevención de las lesiones causadas por instrumentos cortantes y punzantes en el sector hospitalario y sanitario. (DOUE núm. 134, 1-06-2010).
- International Society of Oncology Pharmacy Practicioners Standards Committee. ISOPP standards of practice. Safe handling of cytotoxics. J Oncol Pharm Pract Off Publ Int Soc Oncol Pharm Pract. 2007;13 Suppl:1-81.
- González-Haba E, Manrique-Rodríguez S, Herranz A, Casado C, Sánchez MN, Sanjurjo M. Evaluation and selection of closed-systems for safe cytostatics handling. Eur J Clin Pharm. 17(4):279-88.
- General Chapter 800 Hazardous Drugs: Handling in Healthcare Settings [Internet]. 2016 [accedido 5 Enero 2018]. Disponible en: http://www.usp.org/compounding/general-chapter-hazardous-drugs-handling-healthcare.
- Wick C, Slawson MH, Jorgenson JA, Tyler LS. Using a closed-system protective device to reduce personnel exposure to antineoplastic agents. Am J Health Syst Pharm. 2003;60:2314-20.
- Spivey S, Connor T. Determining sources of workplace contamination with antineoplastic drugs and comparing conventional IV drug preparation with a closed system. Hosp Pharm. 2003;38:135-9.
- Harrison BR, Peters BG, Bing MR. Comparison of surface contamination with cyclophosphamide and fluorouracil using a closed-system drug transfer device versus standard preparation techniques. Am J Health Syst Pharm. 2006;63:1736-44.
- Nygren O, Olofsson E, Johansson L. Spill and leakage using a drug preparation system based on double-filter technology. Ann Occup Hyg. 2008;52:95-8.
- Siderov J, Kirsa S, McLauchlan R. Reducing workplace cytotoxic surface contamination using a closed-system drug transfer device. J Oncol Pharm Pract. 2010;16:19-25.
- Sessink PJ, Connor TH, Jorgenson JA, Tyler TG. Reduction in surface contamination with antineoplastic drugs in 22 hospital pharmacies in the US following implementation of a closed-system drug transfer device. J Oncol Pharm Pract. 2011;17:39-48.
- Clark BA, Sessink PJM. Use of a closed system drug-transfer device eliminates surface contamination with antineoplastic agents. J Oncol Pharm Pract. 2013; 19:99-104.
- Yoshida J, Koda S, Nishida S, Nakano H, Tei G, Kumagai S. Association between occupational exposure and control measures for antineoplastic drugs in a pharmacy of a hospital. Ann Occup Hyg. 2013;57(2):251-60.
- Fleury-Souverain S, Mattiuzzo M, Mehl F, Nussbaumer S, Bouchoud L, Falaschi L, et al. Evaluation of chemical contamination of surfaces during the preparation of chemotherapies in 24 hospital pharmacies. Eur J Hosp Pharm. 2015;22(6):333-41.
- NIOSH. A Performance Test Protocol for Closed System Transfer Devices Used During Pharmacy Compounding and Administration of Hazardous Drugs [Internet]. 2017 [accedido último acceso 5 Enero 2018]. Disponible en: https://www.cdc.gov/niosh/topics/hazdrug/pdfs/performancetestprotocolclosedsystemtransferdevices.pdf.
- Fransman W, Vermeulen R, Kromhout H. Dermal exposure to cyclophosphamide in hospitals during preparation, nursing and cleaning activities. Int Arch Occup Environ Health. 2005;78(5):403-12.
- González Álvarez A, López-Montenegro Soria MA, Albert Marí A, Martínez Gómez MA, Porta Oltra B, Jiménez Torres NV. [Exposure to cytotoxic drugs among health care professionals]. Farm Hosp. 2012; 36(5):368-73.
- González-Haba Peña E, Manrique Rodríguez S, Herranz Alonso AM, Pérez Castán P, Moreno Gálvez M, Iglesias Peinado I, et al. Comparative study of preparation of hazardous drugs with different closed-system drug transfer devices by means of simulation with fluorescein. Farm Hosp. 2016;40(6):496-503.
____
Descargar artículo en PDF: Sistemas cerrados desde la preparación hasta la administración de medicamentos peligrosos
