Medrado e Silva PB¹, da Silva AL¹, Figueiredo Modesto AC², Almeida Matteucci Ferreira TX²
1 Farmacêutica residente
2 Farmacêutica hospitalar
Hospital das Clínicas UFG/EBSERH (Brasil)
Fecha de recepción: 15/03/2019 – Fecha de aceptación: 12/04/2019
Correspondencia: Paula Beatriz Medrado e Silva – Hospital das Clínicas UFG/EBSERH (Residência Multiprofissional em Saúde) – Avenida Primeira Avenida, s/n – Setor Leste Universitário, Goiânia – GO, 74605-020 (Brasil)
pbmedrado@gmail.com
____
RESUMO
As reações adversas a medicamentos são uma das maiores causas de morbimortalidade no mundo. Dentre essas, encontramos a neuropatia periférica, que muitas vezes está relacionada à própria doença, como o mieloma múltiplo, e em decorrência do uso de alguns medicamentos, como a talidomida. Este trabalho é referente à identificação de um possível caso de neuropatia periférica induzida por quimioterápico do tipo autonômica que foi identificado pelo farmacêutico durante uma consulta. O paciente apresentava um quadro de impotência sexual e constipação intestinal severas, com necessidade de retirada manual do conteúdo fecal. Após a suspensão do tratamento com a talidomida, o paciente apresentou remissão completa dos sintomas. A atuação do farmacêutico foi essencial para a identificação precoce, monitoramento e resolução do caso de modo a garantir a melhora na qualidade de vida do paciente.
Palavras-chave: Efeitos colaterais e reações adversas relacionados a medicamentos, assistência farmacêutica, doenças do sistema nervoso periférico.
The role of the pharmacist in the identification of adverse drug reactions: study case of an autonomic neuropathy resulting from treatment with thalidomide in a patient with multiple mieloma
SUMMARY
Adverse drug reactions are one of the major causes of morbidity and mortality in the world. Among these, peripheral neuropathy are often related to the disease itself, such as multiple myeloma, and due to the use of some medications, such as a thalidomide. This work is based on the identification of a possible case of autonomic-type chemotherapy-induced peripheral neuropathy indicated by a pharmacist during a pharmaceutical consultation. The patient presented sexual dysfunction and severe intestinal constipation, with manual withdrawal of fecal content. After suspending the treatment with thalidomide, the patient had a completely remission of symptoms. The performance of the pharmacist was essential for an early evaluation, monitoring and resolution of the case in order to guarantee an improvement in the quality of the patient’s life.
Key Words: Drug-related side effects and adverse reactions, pharmaceutical services, peripheral nervous system diseases.
____
INTRODUÇÃO
As reações adversas a medicamentos (RAM) são uma das maiores causas de morbimortalidade no mundo. Na Europa, estima-se que aproximadamente 5% de todas as internações estejam relacionadas a uma RAM, e que 5% dos pacientes internados experienciarão uma RAM durante sua estadia1.
A neuropatia periférica induzida por quimioterápico (NPIQ) é uma das RAM mais comuns em pacientes com mieloma múltiplo (MM), com incidência de 1 e 20%, dependendo da natureza da população e do histórico de tratamento. Além disso, a frequência da reação adversa aumenta com a idade do paciente e é decorrente do acúmulo de dose, com pior prognóstico para os pacientes idosos. Esse fato é importante, pois aproximadamente 63% dos pacientes portadores de MM possuem mais de 65 anos ao diagnóstico da doença2,3.
Nos pacientes em tratamento de MM, a ocorrência de NPIQ é frequentemente associada ao uso de talidomida, bortezomibe e a alguns outros agentes quimioterápicos4. A NPIQ ocorre em 20 a 40% dos pacientes em tratamento com talidomida e apresenta-se frequentemente como polineuropatia sensitiva com parestesia, que pode ser acompanhada de dor e simetria nas mãos e pés (forma de “luva e meia”). Sintomas autonômicos podem estar presentes, resultando em problemas gastrointestinais, como íleo paralítico e atonia de bexiga, impotência, hipotensão ortostática e problemas cardíacos2,5,6. A NPIQ associada à talidomida pode ser irreversível mesmo após a suspensão do tratamento e ainda não existe documentado na literatura o manejo adequado para a prevenção de NPIQ, restando apenas a modificação de dose ou cessação do tratamento2,4,7. As diretrizes para manejo e modificação de dose da quimioterapia em pacientes com MM que desenvolvam NPIQ são baseadas nos graus da RAM definidos nos Critérios de Terminologia Comum para Eventos Adversos – CTCAE do National Cancer Institute4,8.
Diante da possível gravidade do quadro de NPIQ durante o tratamento de MM com talidomida, os profissionais que prestam assistência a esses pacientes devem monitorá-los de perto quanto ao aparecimento dessa condição, uma vez que ainda não existem maneiras eficazes de preveni-la7. Neste sentido, o farmacêutico pode atuar em conjunto com a equipe multiprofissional de saúde para garantir que a farmacoterapia seja segura e apropriada. O presente estudo de caso teve por objetivo demonstrar a importância da contribuição do farmacêutico na identificação e manejo precoce das RAM, a partir da exposição de um caso de NPIQ identificado pelo farmacêutico.
CASO CLÍNICO
Homem de 55 anos foi diagnosticado com MM em outubro de 2017, e passou a ser acompanhado pela equipe multiprofissional de saúde do Ambulatório de Hematologia de um hospital universitário, no estado de Goiás, Brasil. A equipe multiprofissional de saúde do hospital é composta por médicos, farmacêuticos, enfermeiros, assistentes sociais, nutricionistas, psicólogos e biomédicos.
Ao diagnóstico, o paciente apresentava hipercelularidade medular de 60 a 70% da série linfoplasmocitária, anemia, alteração renal, hipercalcemia e lesões líticas nos corpos vertebrais e na base do crânio. O tratamento foi iniciado em novembro de 2017 com doses orais de 50 mg diárias de ciclofosfamida, 100 mg de talidomida em noites alternadas e 40 mg semanais de dexametasona.
Em janeiro de 2018, o farmacêutico iniciou o acompanhamento do paciente, monitorando o desenvolvimento de RAM associada ao tratamento com talidomida. Esse monitoramento era realizado por meio de consulta farmacêutica, com periodicidade mensal, em que o farmacêutico aplicava um questionário ao paciente para identificar os sintomas de NPIQ. Neste mesmo mês, o farmacêutico identificou que o paciente apresentava os sintomas que poderiam estar relacionados a manifestações autonômicas graves de NIPQ. Essas manifestações incluíam disfunção sexual e constipação intestinal, sendo que o paciente já estava há 8 dias sem evacuar e tinha um histórico recente de 21 dias e ressecamento anal. A constipação intestinal não cedeu com uso de laxantes, e necessitou de retirada manual de fecaloma com piora de qualidade de vida do paciente. Ao farmacêutico, o paciente relatou ainda outros sintomas característicos de neuropatia periférica sensorial e motora, como sensação de dormência nas mãos e dor em pontadas esporádicas nas pernas, e alguns tremores, respectivamente.
Para determinar se existia relação causal entre os sintomas de neuropatia apresentados pelo paciente e o uso de talidomida, o algoritmo de Naranjo foi utilizado pelo farmacêutico, visto que esse instrumento possibilita a categorização da relação de causalidade a partir da identificação de problemas de acordo com algumas perguntas, conforme o Quadro 1. A partir da soma dos resultados foi obtido um score 8, que significa que há uma “provável” correlação do uso de talidomida com os sintomas, e consequentemente, com a NPIQ. A pontuação deste algoritmo é classificada como “Definida” quando apresenta 9 ou mais pontos, “Provável”, de 5 a 8, “Possível” de 1 a 4 e “Duvidosa” com 0 ou menos.
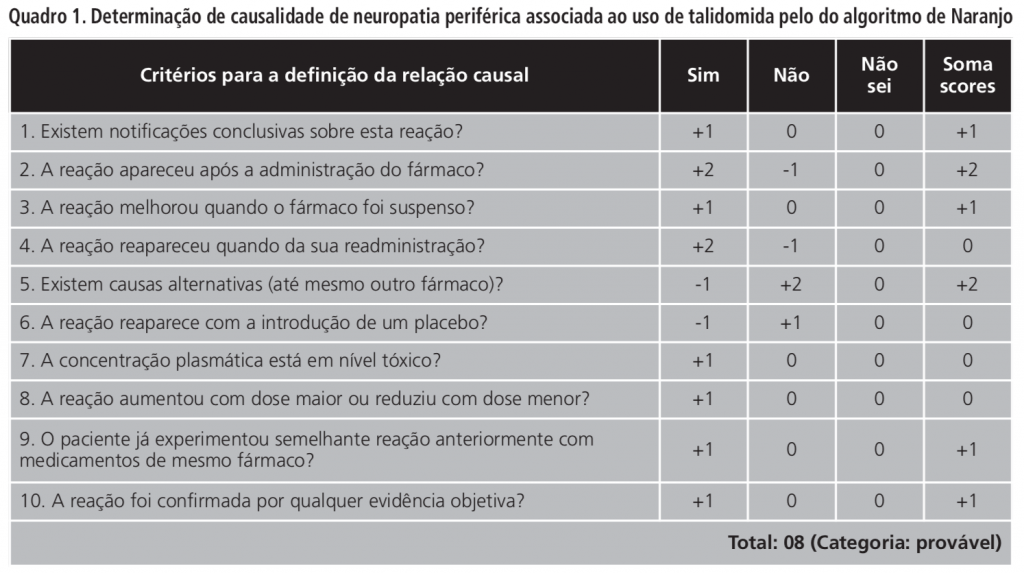
A partir dos achados, o farmacêutico concluiu que os sintomas apresentados pelo paciente poderiam caracterizar a NPIQ e classificou a RAM nos graus definidos no CTCAE: constipação intestinal grau 03, impotência sexual grau 03, já que os sintomas foram severos e precisaram de intervenção médica, como a retirada manual; neuropatia sensitiva grau 01 e neuropatia motora grau 01, pois os sintomas foram leves e não havia indicação de intervenção. Diante do quadro do paciente, o farmacêutico reportou-se à equipe médica, que optou pela suspensão da talidomida devido à gravidade da constipação intestinal apresentada. O bortezomibe foi então adicionado ao esquema quimioterápico do paciente. Em avaliações mensais posteriores realizadas pelo farmacêutico durante as consultas de rotina com o paciente foi observada remissão completa dos sintomas de NPIQ. Este caso foi relatado ao Sistema de Nacional de Farmacovigilância correspondente.
DISCUSSÃO
A busca por terapias e processos que promovam ou melhorem a qualidade de vida dos pacientes com câncer tem sido cada vez mais importante. Para isso, é necessário que as terapias apresentem a melhor efetividade, segurança e conveniência para o paciente9. O uso de questionários pode ser interessante para o monitoramento da NPIQ por possibilitar a avaliação e identificação precoce do desenvolvimento da NPIQ, já que o uso de aparelhos de medidas objetivas como eletromiografia pode não ser sensível o suficiente, além de ser caro e demandar bastante tempo para sua realização4.
A importância da detecção precoce e monitorização dos sintomas de NPIQ está diretamente relacionada à qualidade de vida dos pacientes envolvidos, por prevenir desconfortos e dores desnecessárias, lesões por perda de propriocepção e arreflexia, além de permitir a manutenção das atividades diárias6,8.
Uma das NPIQ que ocorre mais frequentemente e rapidamente com o uso da talidomida é a constipação intestinal, que está potencialmente associada a danos nas fibras nervosas autonômicas6. A constipação intestinal é classificada pelo CTCAE como grau 2 assim que começa a limitar as atividades de vida diária, na qual o paciente apresenta sintomas persistentes com uso regular de laxantes. O farmacêutico pode colaborar no manejo deste problema de saúde autolimitado e melhorar o resultado do tratamento aplicando seu conhecimento farmacoterapêutico10.
Ademais, o farmacêutico pode atuar junto à equipe de saúde de modo a complementar as ações multiprofissionais, promover o uso racional dos medicamentos, otimizar os resultados e promover qualidade, segurança e eficiência no cuidado9,10. Além de detectar RAM e reduzir custos associados, pode também realizar entrevistas com os pacientes, conciliação medicamentosa e orientação de alta9,10. Todas essas atividades podem resultar em melhorias para o tratamento dos pacientes10. Estes serviços são relevantes, especialmente a nível ambulatorial, já que muitas vezes o paciente é tratado de forma fragmentada nos diversos setores em que é atendido e a descoberta de RAM ou de qualquer problema relacionado a medicamento (PRM) ou resultado negativo associado a medicamentos (RNM) pode demorar ou nem ser identificada9.
CONCLUSÃO
O cuidado farmacêutico aos pacientes que fazem uso crônico de medicamentos e possuem diversos problemas de saúde permite a otimização do tratamento e a melhora na qualidade de vida. O farmacêutico tem se integrado cada vez mais as equipes de saúde de modo a contribuir para que o paciente possa ser tratado integralmente e da melhor forma possível. Neste caso, a intervenção farmacêutica proporcionou a identificação precoce e cessação do problema de saúde antes que consequências mais graves ocorressem.
Conflito de interesses: Os autores declaram não haver conflitos de interesse.
BIBLIOGRAFÍA
1. Bouvy JC, De Bruin ML, Koopmanschap MA. Epidemiology of adverse drug reactions in Europe: A review of recent observational studies. Drug Saf. 2015;38:437-53.
2. Grisold W, Cavaletti G, Windebank AJ. Peripheral neuropathies from chemotherapeutics and targeted agents: Diagnosis, treatment, and prevention. Neuro Oncol. 2012;14:iv45-iv54.
3. Palumbo A, Bringhen S, Ludwig H, Dimopoulos MA, Bladé J, Maria V, et al. Personalized therapy in multiple myeloma according to patient age and vulnerability : a report of the European Myeloma Network (EMN). Blood. 2011;118 (17):4519-29.
4. Beijers AJM, Vreugdenhil G, Oerlemans S, Eurelings M, Minnema MC, Eeltink CM, et al. Chemotherapy-induced neuropathy in multiple myeloma: influence on quality of life and development of a questionnaire to compose common toxicity criteria grading for use in daily clinical practice. Support Care Cancer. 2016;24(6):2411-20.
5. Seretny M, Currie GL, Sena ES, Ramnarine S, Grant R, Macleod MR, et al. Incidence, prevalence, and predictors of chemotherapy-induced peripheral neuropathy: A systematic review and meta-analysis. Pain. 2014;155(12):2461-70.
6. Delforge M, Bladé J, Dimopoulos MA, Facon T, Kropff M, Ludwig H, et al. Treatment-related peripheral neuropathy in multiple myeloma: the challenge continues. Lancet Oncol. 2010;11:1086-95.
7. Hershman DL, Lacchetti C, Dworkin RH, Lavoie Smith EM, Bleeker J, Cavaletti G, et al. Prevention and management of chemotherapy-induced peripheral neuropathy in survivors of adult cancers: American society of clinical oncology clinical practice guideline. J Clin Oncol. 2014;32(18):1941-67.
8. Tariman JD, Love G, McCullagh E, Sandifer S. Peripheral neuropathy associated with novel therapies in patients with multiple myeloma: Consensus Statement of the IMF Nurse Leadership Board. Clin J Oncol Nurs. 2008;12(3 Suppl):29-36.
9. Liekweg A, Westfeld M, Jaehde U. From oncology pharmacy to pharmaceutical care: New contributions to multidisciplinary cancer care. Support Care Cancer. 2004;12(2):73-9.
10. Gallagher J, McCarthy S, Byrne S. Economic evaluations of clinical pharmacist interventions on hospital inpatients: a systematic review of recent literature. Int J Clin Pharm. 2014;36(6):1101-14.
____
