Taberner Bonastre P, Aragonés Eroles A, Martínez Castro B, Schoenenberger Arnaiz JA
Hospital Universitario Arnau de Vilanova. Lleida (España)
Correspondencia: Pilar Taberner Bonastre – Hospital Universitario Arnau de Vilanova – Av. Alcalde Rovira Roure, 80 – 25198 Lleida (España)
ptaberner.lleida.ics@gencat.cat
____
RESUMEN
La infección fúngica peritoneal es poco frecuente pero supone una elevada mortalidad. A pesar de que la principal recomendación es la retirada de catéter cuando se sospecha que es éste el foco de infección, hay ocasiones en las se requiere considerar otras opciones.
La administración de anidulafungina intraperitoneal es una técnica sobre la que hay pocos estudios. Presentamos un caso clínico en el que administramos anidulafungina intraperitoneal y analizamos mediante técnica cualitativa la presencia del antifúngico en distintas muestras. Además, calculamos el porcentaje de reducción de anidulafungina entre el líquido de diálisis en el que la diluimos y este mismo tras permanecer 8 horas en la cavidad peritoneal.
Palabras clave: Anidulafungina, peritoneal, Candida glabrata, diálisis.
Qualitative determination of anidulafungin in dialysis fluids with intraperitoneal administration
SUMMARY
Peritoneal fungal infection is rare but involves high mortality. Although the main recommendation is catheter removal when it is suspected that this is the focus of infection, there are occasions when other options are required.
There are few references about administration of intraperitoneal anidulafungin. We present a clinical case in which we administer intraperitoneal anidulafungin and analyze the presence of this antifungal in different samples using a qualitative technique. In addition, we calculate the percentage reduction of anidulafungin between the dialysis fluid in which we diluted it and this fluid after remain 8 hours in the peritoneal cavity.
Key words: Anidulafungin, peritoneal, Candida glabrata, dialyses.
____
INTRODUCCIÓN
La infección peritoneal es una complicación común en pacientes con diálisis peritoneal (DP) siendo más frecuente por bacterias que por hongos. Para esta última se estima una incidencia entre 2-13% y una mortalidad del 15-45%1. El riesgo de infección peritoneal se incrementa cuando hay factores de riesgo, los cuales no han sido establecidos con claridad, pero entre los que se sospecha: episodios previos de peritonitis bacteriana y administración reciente de antibióticos2. La primera recomendación en casos de infección peritoneal es la retirada del catéter cuando este se considera la principal fuente de infección1. Como alternativa, hay algunos casos en los que se ha descrito la administración de anidulafungina intraperitoneal. Existe poca bibliografía en la que se describa la técnica y los resultados obtenidos de su uso3-5.
En relación con la técnica de administración de la anidulafungina intraperitoneal, Tobudic y col. en 2014 publicaron un estudio de estabilidad y compatibilidad de la anidulafungina en los fluidos de DP (Extraneal® y DianealPD4®) en el que observaron que la pérdida de concentración fue inferior al 10% a los 14 días a 3 temperaturas diferentes (4º, 25º y 36ºC). Concluyeron que se observaba lenta degradación química a temperatura y pH fisiológico3.
CASO CLÍNICO
Mujer de 75 años con insuficiencia renal grado IV y cardiopatía, motivo por el cual se aconsejó la DP. El inició de la DP fue tórpido con un primer catéter disfuncional, hematomas, dehiscencia de la herida quirúrgica de la inserción del catéter e infarto agudo de miocardio consecuencia de la hemodiálisis llevada a cabo durante el reposo peritoneal. Posteriormente se aisló en un cultivo rutinario Candida glabrata con sensibilidad a equinocandinas. En este momento, considerando las complicaciones que había tenido la paciente para conseguir usar el catéter peritoneal y por su cardiopatía, se decidió evitar la retirada del catéter y tratamiento con anidulafungina. La paciente recibió una dosis inicial de 200 miligramos de anidulafungina intravenosa seguido de 100 miligramos intraperitoneal diluida en Extraneal® durante 1 semana. Se optó por esta vía de administración por el mal acceso venoso del que disponía la paciente.
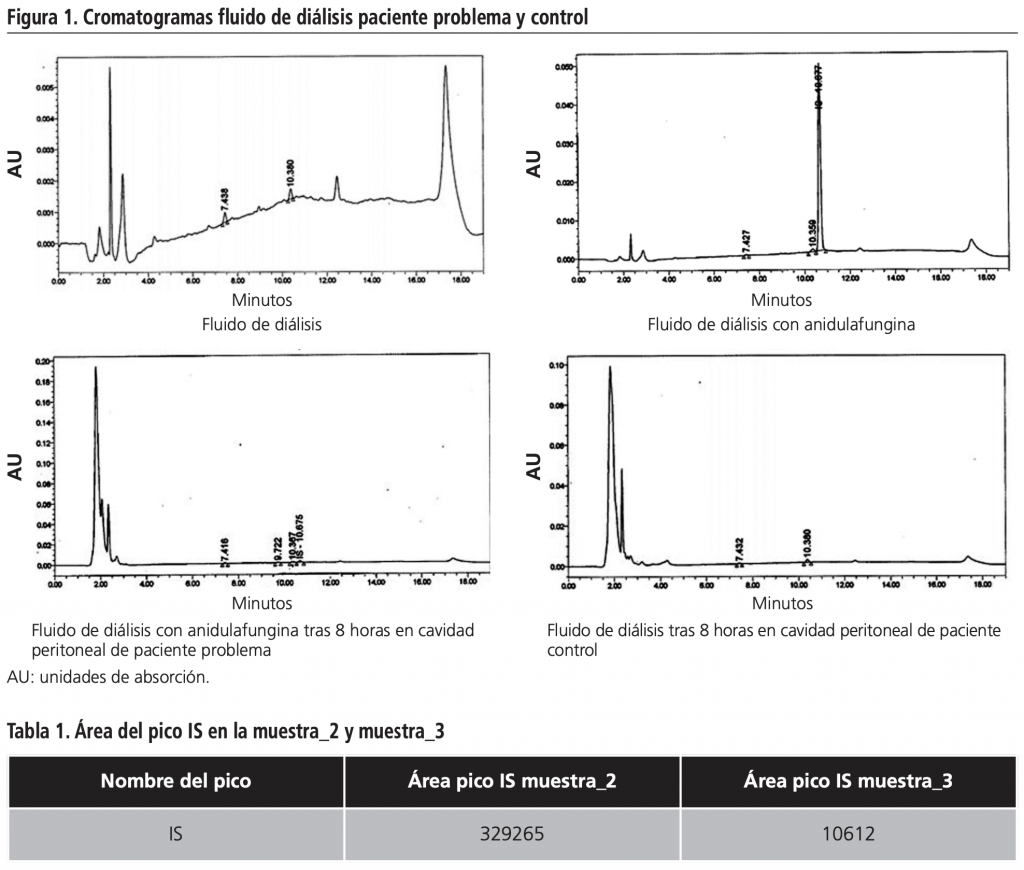
Se llevó a cabo análisis cualitativo de anidulafungina en distintas muestras de líquido peritoneal aprovechando una técnica desarrollada para la cuantificación de micafungina en plasma, en la que se usa anidulafungina como control interno (HPLC con detección ultravioleta). Se solicitaron consentimientos informados aceptando la participación en la técnica experimental de la paciente que recibió el tratamiento y de la que sirvió de control. Las muestras en las que se determinó presencia de anidulafungina fueron: Extraneal® sin manipular (muestra_1), dilución de anidulafungina en Extraneal® que se utilizó como fluido de diálisis (muestra_2), líquido peritoneal (LP) extraído tras la diálisis (muestra_3) y LP-Extraneal® de una paciente control tras realizar DP (muestra_4). La muestra_1 y la muestra_4 sirvieron para confirmar la ausencia de interferencias en el tiempo de elución de anidulafungina.
La extracción aplicada al LP fue la misma que la que se usa para plasma (precipitado de proteínas en placa con extracción de fosfolípidos) cuando se determinan concentraciones de micafungina en plasma. Se usó como contenedor de la muestra un tubo con heparina de litio como anticoagulante previamente validado en el método para análisis en plasma.
Se observó presencia de un pico en la muestra_2 en el tiempo 10.677, correspondiente a la elución de anidulafungina en el método inicial, y un pico de menor tamaño en la muestra_3 en el mismo tiempo de elución. Se comparó el espectro ultravioleta de la sustancia eluida, con el espectro de anidulafungina almacenado en la base de datos del cromatógrafo, coincidiendo (Figura 1). El porcentaje residual de anidulafungina en la muestra_3 frente a la muestra_2 fue de 3,22% (Tabla 1). No se observó ningún pico en el tiempo de elución de anidulafungina ni en la muestra_1 ni en la muestra_4.
La paciente presentó cierta mejoría con el tratamiento de anidulafungina intraperitoneal. Ingresó al finalizar el tratamiento antifúngico por síndrome tóxico agravado de causa no filiada. A los 20 días del ingreso y tras cobertura antibiótica de amplio espectro para lo cual la paciente requirió instauración de vía central ya que las vías periféricas tenían un complicado acceso, se retiró el catéter peritoneal. Desde la retirada del catéter peritoneal, se realizó hemodiálisis solo en situaciones de necesidad imperiosa por su cardiopatía. Finalmente la paciente falleció a los dos meses del inicio de la anidulafungina intraperitoneal.
DISCUSIÓN
A pesar de que la paciente no presentaba factores de riesgo para sospechar de infección fúngica, se aisló cultivo positivo en control rutinario demostrándose la importancia de realizar estos controles.
El bajo porcentaje de anidulafungina en la muestra_3 respecto al de la muestra_2 hace pensar en una buena difusión a través del peritoneo del antifúngico. El análisis presenta limitaciones ya que la técnica estaba validada para plasma, no para LP y que se trata de un método cualitativo. El análisis podría haberse hecho de forma cuantitativa si se hibiera administrado micafungina intravenosa a la paciente ya que se dispone de la técnica validada.
CONCLUSIÓN
Se trata de una técnica experimental con la que se comprobó la reducción de anidulafungina en una muestra de fluido de diálisis tras haber estado en peritoneo durante un periodo de 8 horas en las cuales gracias al estudio de Tobudic y col. podemos saber que no se degradó por lo que intuimos que se absorbió a través de peritoneo. Este análisis sirve como precedente para futuros casos dado el número reducido de ocasiones en los que se utiliza esta técnica.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
BIBLIOGRAFÍA
1. UpToDate. Fungal peritonitis in peritoneal dialysis. Joel D Glickman, Gary M Cox, Carol A Kauffman. [Jul 25, 2019 ; Nov 11, 2019]. Disponible en: https://bit.ly/2RHx6XO.
2. R. García-Agudo, P. García-Martos. Aspectos clínicos y microbiológicos de la peritonitis fúngica en diálisis peritoneal. Nefrología. 2009;29(6):506-517.
3. Tobudic S, Donath O, Vychytil A, Forstner C, Poeppl W, Burgmann H. Stability of anidulafungin in two standar peritoneal dialysis fluids. Perit Dial Int. 2014;34(7):798-802. DOI: 10.3747/pdi.2012.00326.
4. Tobudic S, Harrison N, Forstner C, Kussman M, Burgmann H. Effect of peritoneal dialysis fluids on activity of echinocandins against Candida Spp. Biofilm. Med Mycol. 2017; 55(7):790-793. DOI: 10.1093/mmy/myw145.
5. Agencia Española del Medicamento y Productos Sanitarios. CIMA (entro de información de medicamentos). Ficha técnica de Ecalta 100 mg. [Base de datos en Internet]. España: Agencia Española de Medicamentos y Productos Sanitarios [consultado el 05/12/2019]. Disponible en: https://cima.aemps. es/cima/dochtml/ft/07416002/FT_07416002.html.
____
