Rev. OFIL 2018, 28;1:23-27
Fecha de recepción: 17/01/2018 – Fecha de aceptación: 28/01/2018
Alonso Pérez L, Gomis Muñoz P, Ferrari Piquero JM
Hospital Universitario 12 de Octubre. Servicio de Farmacia. Madrid (España)
Este trabajo se presentó parcialmente en formato póster con el título de “Disgregación de comprimidos de medicamentos peligrosos” en el Congreso Nacional de Farmacia Hospitalaria que se celebró en Madrid en 2017
____
Correspondencia:
Lucía Alonso Pérez
Hospital Universitario 12 de Octubre
(Servicio de Farmacia)
Avda. Córdoba, s/n
28041 Madrid
Correo electrónico: lalonsoperez@salud.madrid.org
____
Resumen
Introducción: Recientemente el Instituto Nacional de Seguridad e Higiene en el Trabajo ha elaborado un documento técnico sobre medidas de prevención para la preparación y administración de medicamentos peligrosos. Entre los medicamentos que hay que preparar en cabina de seguridad biológica están los comprimidos que deban machacarse para administrarse en forma líquida. Una alternativa a su preparación centralizada sería la disgregación del comprimido en una jeringa.
Objetivo: Conocer si el tiempo de disgregación de los comprimidos de los medicamentos peligrosos incluidos en la Guía de nuestro hospital es menor de 5 minutos, y por tanto podría utilizarse este método para su administración segura.
Material y métodos: Cada comprimido se introdujo en una jeringa con 10 ml de agua. Se agitó varias veces y se dejó en reposo 5 minutos. Posteriormente se volvió a agitar y se valoró si se había disgregado.
Resultados: Aproximadamente un 50% de los comprimidos se disgregaron en 5 minutos. En algunos de ellos quedaba una parte importante del polvo en la jeringa después de vaciarla, por lo que fue necesario volverla a cargar de agua y agitar para no perder parte del medicamento.
Conclusión: Un alto porcentaje de los comprimidos de medicamentos peligrosos que necesitan ser administrados en forma líquida pueden disgregarse en una jeringa y ser manipulados con las debidas precauciones, lo que podría ser una alternativa a la preparación centralizada en un Servicio de Farmacia.
Palabras clave: Medicamentos, peligrosos, disgregación, jeringa.
____
Introducción
La definición de medicamento peligroso (MP) fue introducido por la ASHP en 19901 y adoptado por la OSHA2 para aquellos medicamentos que presentan en humanos al menos una o más de una de las siguientes características de peligrosidad: carcinogenicidad, teratogenicidad u otra toxicidad para el desarrollo, toxicidad reproductiva, toxicidad en órganos a dosis bajas, genotoxicidad, estructura o perfil de toxicidad similares a otros medicamentos peligrosos.
En el año 2004 The National Institute for Occupational Safety and Health (NIOSH) publicó una lista de medicamentos peligrosos3, que se actualizó en 20104, 20125 y 20166.
NIOSH en la publicación del 2014 agrupó los medicamentos peligrosos en tres grupos:
- Grupo 1: Medicamentos antineoplásicos.
- Grupo 2: Medicamentos no antineoplásicos que cumplen al menos un criterio de peligrosidad de los aceptados por OSHA o ASHP.
- Grupo 3: Medicamentos que presentan riesgo para el proceso reproductivo y que puedan afectar a hombres y mujeres que están intentando concebir de forma activa, y mujeres embarazadas o en período de lactancia, pero que no comportan riesgo para el resto del personal.
En septiembre de 2016, sale a la luz el documento técnico “Medicamentos peligrosos, Medidas de prevención para su administración” publicado por el Instituto Nacional de Seguridad e Higiene en el Trabajo (INSHT) en el que se establece una relación de medicamentos clasificados como “peligrosos” de uso en España y recomendaciones para la protección de los profesionales durante su manejo.
Este documento se basa en la lista de medicamentos peligrosos publicados por NIOSH en 2014. Adicionalmente el INSHT revisó la disponibilidad de estos medicamentos en España y la presencia de otros medicamentos peligrosos que no estuvieran en las listas de Revisión del grupo ATC L (Antineoplásicos) disponibles en la Agencia Española del Medicamento y Productos Sanitarios o inclusión de algunos medicamentos por similitud en la estructura y toxicidad con medicamentos de la lista NIOSH. El cumplimiento de las recomendaciones incluidas en dicho documento supone nuevas responsabilidades de trabajo para el Servicio de Farmacia requiriendo aumentar el número de recursos humanos con competencia y capacitación en el manejo de medicamentos peligrosos y por otra parte, de los recursos materiales, tanto de las instalaciones (cabinas de seguridad biológica y salas blancas) como de sistemas cerrados de transferencia de medicamentos. No obstante, para prevenir los posibles efectos perjudiciales de una manipulación inadecuada de MP, se considera clave aplicar las medidas organizativas de prevención primaria colectiva que deben incluir: La aplicación sistemática de trabajo, la validación y el establecimiento de procedimientos normalizados de trabajo que contemplen todas las fases de la manipulación de los medicamentos peligrosos y las medidas de actuación frente a cualquier situación7. Mientras se produce esa adaptación de recursos y organización, es preciso plantearse medidas alternativas de manejo de MP que garanticen la seguridad del personal manipulador.
Entre los MP que según el documento citado hay que preparar en cabina de seguridad biológica se encuentran medicamentos cuya forma farmacéutica es de comprimido que deba triturarse para administrarse diluido. Una alternativa a su preparación centralizada sería la dispersión del comprimido en una jeringa.
El objetivo de este estudio es conocer si el tiempo de disgregación de los comprimidos de los medicamentos peligrosos incluidos en la Guía Farmacoterapéutica de nuestro hospital es menor de 5 minutos, con lo que este método podría ser una alternativa a su preparación centralizada en el Servicio de Farmacia.
MATERIAL Y MÉTODOS
Se revisó el documento técnico sobre medidas de prevención para la preparación y administración de medicamentos peligrosos del Instituto Nacional de Seguridad e Higiene en el Trabajo, se seleccionaron los principios activos orales sólidos y se eligieron aquellos cuya forma farmacéutica se comercializa como comprimido y que se encuentran incluidos en la Guía Farmacoterapéutica de nuestro hospital en el momento de realizar el estudio (Tabla 1).
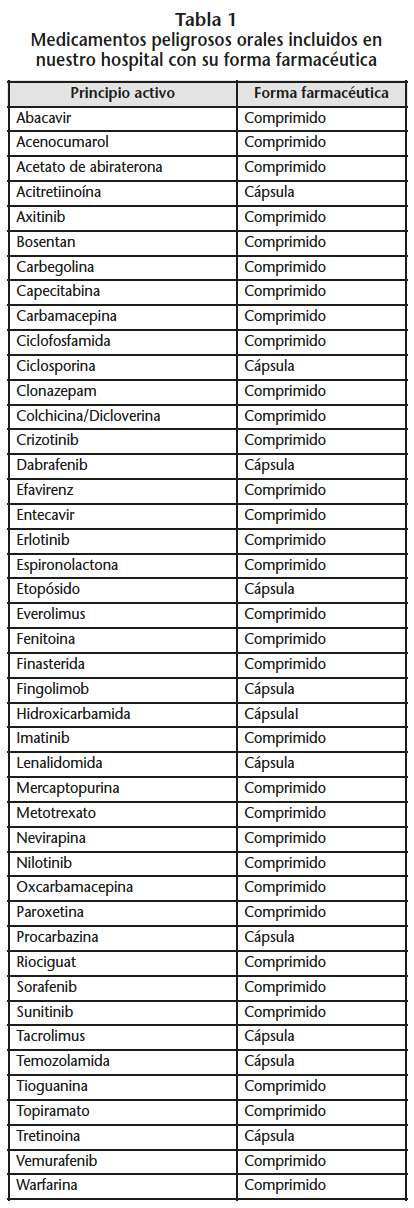
Una vez seleccionados los medicamentos peligrosos cuya forma farmacéutica es comprimido, se procedió a realizar la dispersión con los siguientes pasos:
- Quitar el émbolo de una jeringa de 20 mL.
- Introducir el comprimido sin triturar en la jeringa y colocar de nuevo el émbolo.
- Aspirar unos 10 mL de agua templada.
- Tapar la jeringa y agitar periódicamente.
- Comprobar si se disuelve en menos de 5 minutos.
La manipulación de medicamentos peligrosos se realizó protegiéndose con batas, mascarillas y guantes.
La solución generada se depositó en el contenedor de residuos de citotóxicos.
RESULTADOS
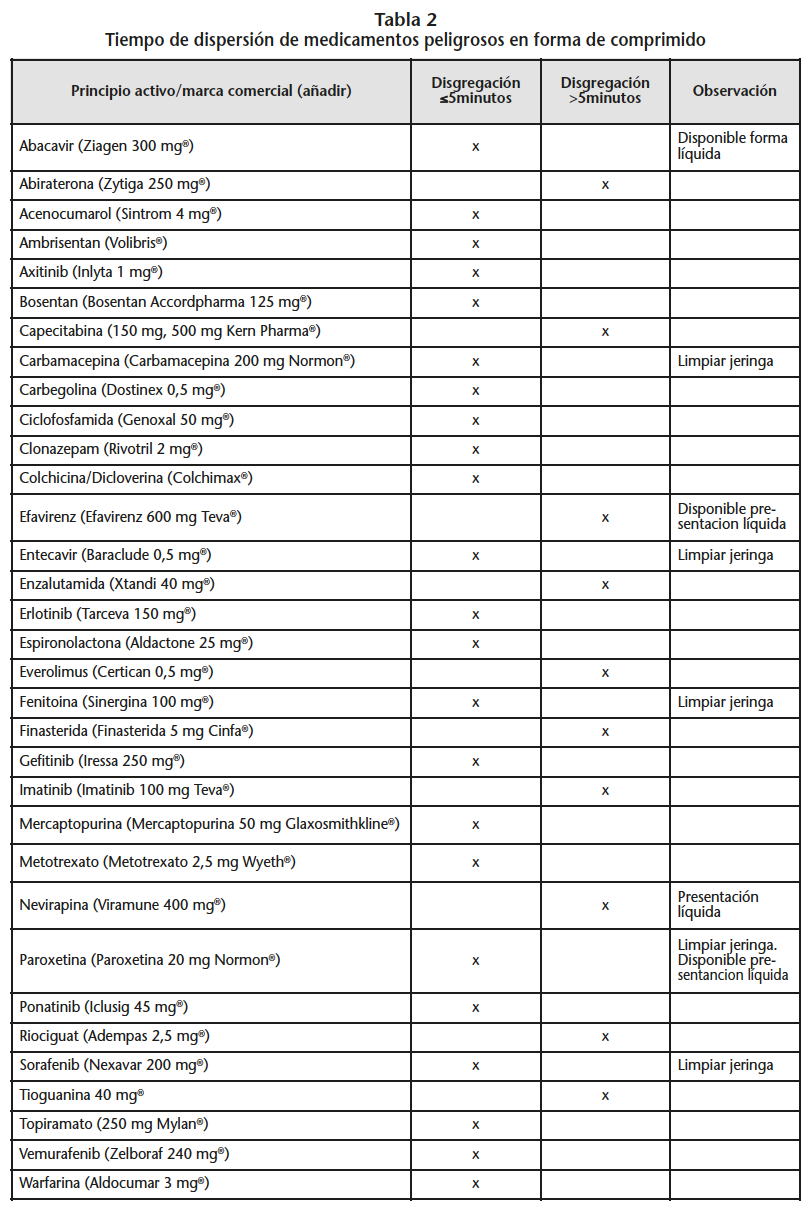
Más del 50% de los comprimidos se disgregaron en menos de 5 minutos (Tabla 2). En algunos de ellos (entecavir paroxetina, fenitoina, carbamacepina y sorafenib) quedaba una parte importante del polvo en la jeringa después de vaciarla, por lo que fue necesario volverla a cargar de agua y agitar para no perder parte del medicamento. En estos casos se podría utilizar la dispersión en jeringa siempre y cuando quisiéramos administrar toda la dosis al paciente. De los fármacos en los que hemos realizado el estudio hay en varios que existen también en la presentación líquida como son abacavir, clonacepam, paroxetina y efavirenz. De los MP en forma de comprimidos que aparecen en el documento técnico en el 28% de ellos se podría utilizar este procedimiento.
DISCUSIÓN
La definición de medicamento peligroso engloba una gran variedad de fármacos, desde antineoplásicos cuyos riesgos para toda persona implicada están claramente definidos hasta medicamentos que podrían afectar sólo a personas en edad fértil en menor grado. No existe un único enfoque que pueda cubrir todas las posibles exposiciones ocupacionales a medicamentos peligrosos debido a esta variabilidad6.
Hay que evaluar en cada situación el riesgo para la salud que supone para el profesional la manipulación de estos fármacos. En cada centro es necesario elaborar una lista con medicamentos peligrosos con las recomendaciones óptimas para la protección de la salud del trabajador.
Entre los factores que afectan a la exposición de los trabajadores se puede citar la forma farmacéutica. En el proceso de selección de medicamentos deben considerarse aspectos específicos que puedan repercutir en la seguridad y salud de trabajadores, pacientes y medio ambiente8.
Respecto a los medicamentos peligrosos orales se recomienda que la presentación comercial se adapte lo mejor posible a las dosis habituales, con el objeto de minimizar la manipulación. En las formas líquidas se debe elegir la concentración más apropiada y de más fácil manejo y todas las dosis disponibles de los medicamentos peligrosos cuya forma farmacéutica sea comprimidos para evitar fraccionamiento.
Hay casos en los que es inevitable fraccionar o triturar el medicamento como es en la población pediátrica o en pacientes que poseen sonda nasogástrica. La administración de medicamentos por sonda nasogástrica es una práctica habitual en los hospitales. Habitualmente, los fármacos no disponibles en la forma farmacéutica líquida, son triturados por el personal de enfermería en las unidades de hospitalización. Este método aparte de consumir mucho tiempo en enfermería, puede dar lugar a que el paciente reciba menos dosis9. En nuestro hospital, según un estudio de la dispersión de los medicamentos en agua para su administración por sonda, un alto porcentaje de ellos se dispersaban en menos de 5 minutos10.
Otros autores también han descrito la facilidad de dispersión de los comprimidos en agua, sobre todo en guía de administración por sondas enterales11.
En el presente estudio se ha observado que existen algunos medicamentos peligrosos orales que se dispersan fácilmente en una jeringa con agua templada en un tiempo adecuado. Este método podría ser una alternativa a la centralización del proceso de trituración de los fármacos en la cabina de flujo laminar de los Servicios de Farmacia. Existe bibliografía publicada para la adaptación a formulación magistral de medicamentos peligrosos orales que son necesarios fraccionar porque no está disponible la presentación comercial adecuada para cada caso. Para la elaboración de formulación magistral de medicamentos peligrosos se deben preparar en una sala separada de la zona de preparación de medicamentos peligrosos estériles para evitar el riesgo de contaminación de la sala y de la cabina con partículas sólidas. En las operaciones de mezclado de polvos, elaboración de cápsulas, pesada o trituración de formas sólidas de medicamentos peligrosos, se debe utilizar una cabina de seguridad biológica tipo I o las CVE (containment ventilated enclosure) en las condiciones descritas por la USP. En caso de utilizar una cabina de flujo laminar vertical tipo IIB2 no debe ser la misma en la que se manipulen los medicamentos peligrosos estériles, aunque en caso excepcional sería admisible si se procede a una limpieza y desinfección de la cabina tras la manipulación del no estéril.
El material de laboratorio para la elaboración de las fórmulas magistrales debe ser desechable o de uso único para medicamentos peligrosos, o esterilizable. El material de uso único para medicamentos peligrosos no desechable debe ser identificado como tal y ser lavado inmediatamente después de su uso con agua, jabón y un último enjuagado con agua11. Tanto el agua como la esponja en caso de utilizarse, deben tratarse como residuos contaminados12.
Para un manejo seguro de medicamentos peligrosos orales en las plantas de hospitalización es recomendable realizar información y formación a los profesionales, implementar medidas de identificación así como un desarrollo informático en el que señalice el medicamento peligroso y las recomendaciones generales de actuación13,14.
CONCLUSIONES
La dispersión de comprimidos en jeringas podría ser una alternativa a la preparación centralizada en los Servicios de Farmacia del proceso de trituración de los medicamentos orales peligrosos en la cabina de flujo laminar, mientras se produce la adaptación de la organización al documento técnico, siempre que se lleve a cabo por profesionales informados y formados para realizar la técnica y se utilicen equipos de protección individual (EPIs) adecuados que garanticen la protección del manipulador.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
Bibliografía
- ASHP tecchical assistance bulletin on handling cytotoxic and hazardous drugs. Am J Hosp Pharm. 1990;47(5):1033-49.
- Occupational Safety and Health Administracion (OSHA). OSHA Techical Manual. [Consultado: 9/12/2017]. Disponible en: https://www.osha. gov/dts/osta/otm/otm_ vi/otm_vi_2.html.
- National Institute for Occupational Safety and Health (NIOSH). NIOSH alert: Preventing Occupational Exposures To Antineoplastic and Other Hazardous Drugs in Healthcare Setting (Monografía en internet); 2004. 2004-165. [Consultado 9/12/2017]. Disponible en: http://www.cdc.gov/niosh/docs/2004-165/pdfs/ 2004-165.pdf.
- National Institute for Occupational Safety and Health (NIOSH). NIOSH List Of Antineoplastic and Other Hazardous Drugs in Healthcare setting 2010 ( Monografía en internet); 2010.2010-167. Disponible en internet; 2010.2010-167. [Consultado 10/12/2017]. Disponible en https://cdc.gov/niosh/docs/2010-167/pdfs/2010-167.pdf
- National Institute for Occupational Safety and Health (NIOSH). NIOSH List Of Antineoplastic and Other Hazardous Drugs in Healthcare setting 2012. (Monografía de internet); 2012.2012-150. [Consultado 10/12/2017]. Disponible en https://www.cdc.gov/niosh/docs/2012-150/pdfs/2012-150.pdf.
- National Institute for Occupational Safety and Health (NIOSH). NIOSH List Of Antineoplastic and Other Hazardous Drugs in Healthcare setting 2014. (Monografía en internet); 2014.2014-138. [Consultado 10/12/2017]. Disponible en http://www.cdc.gov/niosh/docs/2014-138/pdfs/2014-138.pdf.
- Monografías de farmacia hospitalaria y atención primaria: medicamentos peligrosos (Nº 6). Barcelona: Bayer Hispania SL, 2016.
- Canadian Standards Association (CSA). Handling of waste material in health care facilities and veterinary health care facilities. 2002 [Consultado 10/12/2017]. Disponible en: http://www.scc.ca/en/standardsdb/standards/7607.
- Beales Jetat Administracion of medication via nasogastric tube. Can J Hosp Pharm. 1991;44:107-8.
- Luna Vega T, Sorni Pérez I, Goyache Goñi MP, Marfagón Sanz N, Herreros de Tejada A. Técnica para la administración de medicamentos por sonda nasogástrica. Farm Hosp. 1998;22(5):257-260.
- Guía de administración de medicamentos por sondas de alimentación de alimentación enteral Hospital Clínico San Carlos 2012.
- Connor T, McLauchlan R, Vandenbroucke J. ISOPP Standards of Practice. Section 9: Non sterile preparation. J Oncol Pharm Pract. 2007;13:43. [Consultado 12/12/2017]. Disponible online en: http://opp.sagepub.com/content/13/3_suppl/43.citation.
- Compounding with hazardous drugs. Secundum Artem, vol. 15, nº 2. [Consultado 12/12/2017]. Disponible en: http://www.perrigo.com/business/education.aspx.
- Gaspar Carreño M, Achau Muñoz R, Torrico Martín F, Agún González, Sánchez Santos JC, Cercos LLeti AC, Ramos Orozco P. Safe procedure development to manage hazardous drugs in the workplace. Farm Hosp. 2017;41(2):222-256.
____
Descargar articulo completo en PDF: Dispersión de comprimidos de medicamentos peligrosos como forma segura de administración en unidades de hospitalización
