Sangrador Pelluz C1, Maiques Llácer FJ1, Soler Company E1, Flores Cid J2
1 Servicio de Farmacia
2 Unidad de Enfermedades Infecciosas
Hospital Arnau de Vilanova. Valencia (España)
Resumen
Objetivo: Evaluar la efectividad del tratamiento con ribavirina, peginterferon alfa y boceprevir en pacientes con hepatitis C crónica en la semana 24 tras la finalización del tratamiento.
Material y método: Estudio observacional retrospectivo (enero 2012-julio 2014). Se incluyeron todos los pacientes con VHC genotipo 1 que hubieran finalizado el tratamiento con boceprevir.
Evaluación efectividad: Carga viral <15 UI/ml en la semana 24 post-tratamiento.
Resultados: Se incluyeron 57 pacientes: 63,2% curaciones, 24,6% fracasos de tratamiento, 10,5% suspensiones por toxicidad y 1,8% de abandono del tratamiento. Pacientes que completaron el tratamiento (n=50), efectividad global del 72%. Mayor efectividad en pacientes no cirróticos (86,4% vs. 60,7% p=0,044). No se evidenciaron diferencias en efectividad entre pacientes monoinfectados y coinfectados por VIH.
Conclusiones: Nuestros resultados de efectividad se sitúan dentro del intervalo establecido por los principales trabajos publicados tanto de eficacia como efectividad, resultando la cirrosis hepática como el principal factor que condiciona la efectividad.
Palabras clave: Boceprevir, hepatitis C crónica, efectividad.
Effectiveness of triple therapy with boceprevir in chronic hepatitis C patients
Summary
Objective: To evaluate the effectiveness of treatment with ribavirin, boceprevir and peginterferon alfa in patients with chronic hepatitis C at week 24 after completion of treatment.
Methods: Retrospective observational study (January 2012-July 2014). Were included all patients with HCV genotype 1 who had completed treatment with boceprevir.
Effectiveness evaluation: Viral load <15 IU/ml at week 24 post-treatment.
Results: 57 patients were included: 63.2% cures, 24.6% treatment failures, 10.5% suspensions toxicity and 1.8% discontinuing treatment. Patients who completed treatment (n=50), overall effectiveness of 72%. Greater effectiveness in non-cirrhotic patients (86.4% vs 60.7% p=0.044). No differences about effectiveness were apparent between patients monoinfected and coinfected with HIV.
Conclusions: Our effectiveness results are within the range established by the major works published of efficacy and effectiveness, resulting in liver cirrhosis as the primary factor that determines the effectiveness.
Key Words: Boceprevir, hepatitis C chronic, effectiveness.
____
Descargar PDF: Efectividad de la triple terapia con boceprevir en pacientes con hepatitis C crónica
Artículo dentro del número: VOL. 25 – Nº2 – 2015
____
Introducción
La infección por el virus de la hepatitis C (VHC) es un problema de salud grave que afecta aproximadamente al 3% de la población mundial1,2 y que en el 85% de los casos se establece como una infección crónica3.
La incorporación de los antivirales de acción directa sobre el VHC, telaprevir y boceprevir, ha permitido superar el techo de la eficacia de la terapia convencional basada en la combinación de interferón pegilado y ribavirina4,5. El tratamiento con boceprevir ha sido evaluado en los ensayos clínicos fase III SPRINT-26 y RESPOND-27, en los que se describe respuesta viral sostenida (RVS) del 75% en los pacientes naive y del 50% en pacientes que habían fracasado a terapias previas. Sin embargo, en la actualidad ya se dispone de estudios observacionales de práctica clínica8,9 que ponen de manifiesto unas tasas de RVS inferiores a las señaladas en los ensayos clínicos6,7.
Dado que la población coinfectada por VHC-VIH y los pacientes respondedores nulos a terapias previas no han sido incluidos en los ensayos clínicos que llevaron a la aprobación del boceprevir y que la población cirrótica estaba menos representada en los mismos, en la actualidad se disponen de pocos datos en este contexto. Es por ello que la evaluación del éxito del tratamiento en estos grupos de pacientes así como en pacientes cirróticos, población poco representada en los ensayos pivotales, resulta de especial interés en la actualidad.
El objetivo del estudio es evaluar la efectividad del tratamiento combinado con ribavirina, peginterferon alfa y boceprevir para el tratamiento de la hepatitis C en pacientes monoinfectados y coinfectados a la semana 24 tras la finalización del tratamiento.
Material y método
Estudio observacional retrospectivo de dos años y siete meses de duración (enero 2012-julio 2014) realizado en nuestro Departamento de Salud que cubre a una población aproximada de 311.000 habitantes.
Los criterios de inclusión fueron todos los pacientes adultos infectados por VHC genotipo 1, tanto monoinfectados como coinfectados por VIH, que:
– hubieran finalizado el tratamiento completo con boceprevir, peginterferon y ribavirina y dispusieran de resultado de carga viral a la semana 24 post-finalización de tratamiento, o
– aquellos en los que se hubiera suspendido la triple terapia durante el periodo de estudio bien por toxicidad grave o por fracaso del tratamiento a lo largo del mismo.
A partir del programa informático Farmasyst® y de la revisión de las historias clínicas a través de Orion Clinic® se recogieron las variables necesarias para caracterizar a los pacientes, y aquellas referentes al tratamiento recibido.
Se recogieron las siguientes variables relacionadas con los pacientes: edad, sexo, genotipo del VHC, grado de fibrosis, tipo de paciente (naive o pretratados) y coinfección con VIH.
Respecto al tratamiento se recogieron: carga viral inicial (CV) previa al inicio de la triple terapia, CV en la semana 24 post-tratamiento, suspensiones de tratamiento y causas (toxicidad o fracaso durante la biterapia) y fracasos tras la finalización del tratamiento.
La efectividad se evaluó como respuesta viral sostenida (resultado de carga viral RNA-VHC inferior a 15 UI/ml) evaluada a la semana 24 tras finalizar de forma completa el tratamiento de triple terapia con boceprevir. En cuanto a los casos de fracaso del tratamiento, se analizó tanto la causa como el momento del tratamiento donde tuvo lugar.
Los datos se analizaron mediante el programa estadístico SPSS® versión 15.0. Se realizó un análisis estadístico descriptivo, incluyendo medidas de tendencia central y dispersión, y frecuencias absolutas y relativas. En cuanto al análisis comparativo, se empleó el test Chi-cuadrado para comparar en función de una variable categórica.
Resultados
Se incluyeron un total de 57 pacientes. Por intención de tratar los resultados de efectividad evaluados como RVS a las 24 semanas fueron: 63,2% (36/57) curaciones, 24,6% (14/57) fracasos de tratamiento, 10,5% (6/57) suspensiones de tratamiento por toxicidad y 1,8% (1/57) de abandono voluntario del tratamiento. Respecto a los fracasos de tratamiento, en el 17,5% (10/57) el fracaso tuvo lugar durante la triple terapia y en el 7,0% (4/57) durante las 12 semanas posteriores a la finalización del tratamiento.
Para el análisis más detallado de la efectividad del tratamiento se excluyeron siete pacientes: seis por suspensión del tratamiento por toxicidad y uno por incumplimiento voluntario del tratamiento.
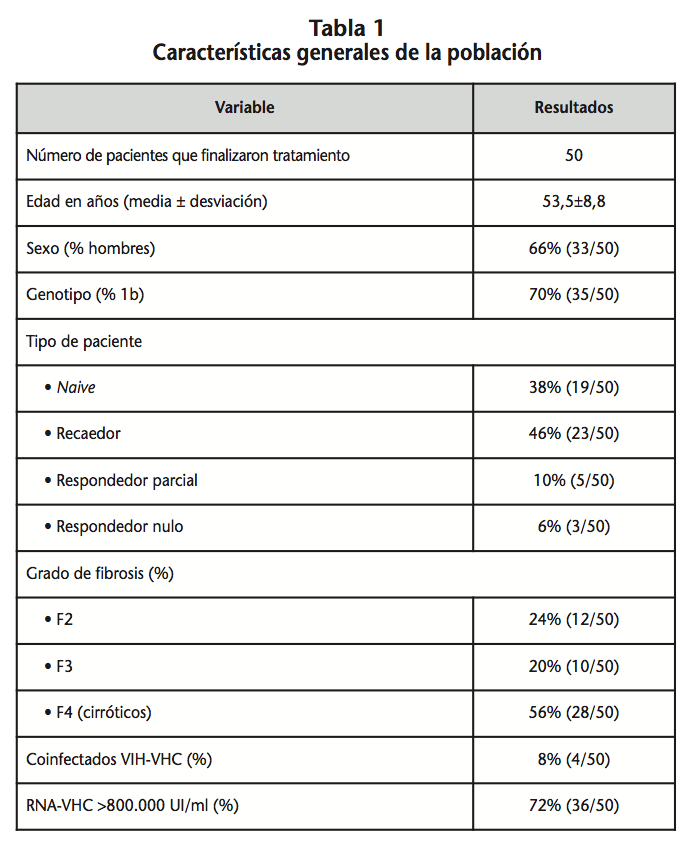
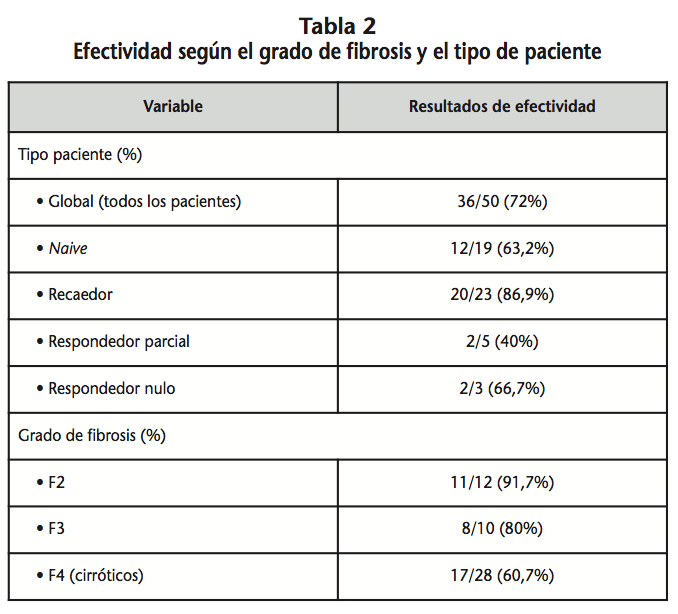
Respecto a los 50 pacientes restantes que finalizaron el tratamiento, sus características generales se detallan en la tabla 1. Los resultados de efectividad en función del grado de fibrosis o tipo de paciente se recogen en la tabla 2.
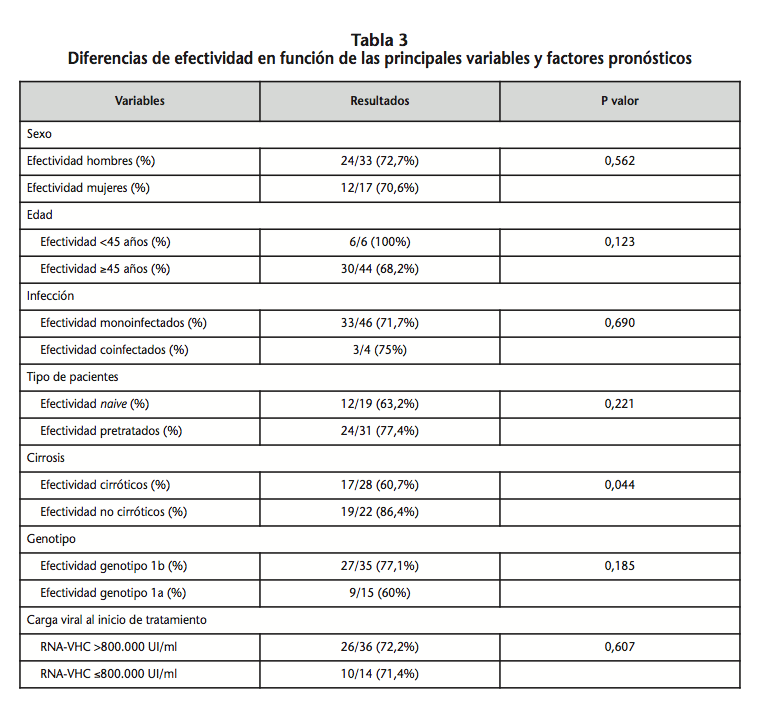
La diferencia de efectividad en función de las principales variables y factores pronósticos se detallan en la tabla 3.
Discusión
En cuanto a la efectividad según el tipo de paciente nuestros resultados son inferiores a los publicados para pacientes naive (63,2% vs. 66%) y respondedores parciales (40% vs. 40-52%), sin embargo se observan mejores tasas de respuesta en pacientes recaedores (86,9% vs. 69-75%). Estas diferencias podrían explicarse debido al menor tamaño muestral, el mayor porcentaje de pacientes con grado de fibrosis avanzada F3-F4 (76%) y la inclusión de pacientes coinfectados con VIH.
En cuanto al estudio CUPIC de práctica clínica realizado en pacientes cirróticos8 nuestros resultados de efectividad son similares para pacientes respondedores parciales (40%) y superiores para recaedores (86,9% vs. 51%) y respondedores nulos (66% vs. 11%).
De manera global, incluyendo pacientes naive y pretratados, la tasa de efectividad obtenida en nuestro estudio fue del 63,2%, dato que se sitúa dentro del intervalo presentado por los ensayos clínicos (59-75%)6,7 y superior al resultado obtenido en pacientes cirróticos en el estudio CUPIC (41%)8 y otros estudios de práctica clínica (50%)9.
Respecto a las diferencias de efectividad en función de características de los pacientes se observó una mayor efectividad en pacientes no cirróticos frente a pacientes con cirrosis de manera estadísticamente significativa (86,4% vs. 60,7% p=0,044), al igual que se señala en los ensayos clínicos6,7. Sin embargo, los resultados de efectividad para pacientes cirróticos en este estudio fueron superiores a los observados en el estudio CUPIC (60,7% vs. 41%)8.
En cuanto al resto de variables comparadas no se demostraron diferencias estadísticamente significativas, sin embargo, al igual que se señala en los ensayos clínicos, se observa una tendencia de mayor efectividad para pacientes menores de 45 años, hombres y con genotipo 1-b6,7.
En cuanto al análisis de los fracasos de tratamiento, la prevalencia de suspensiones por toxicidad (10,5%) resultó similar a la indicada en el ensayo clínico RESPOND-2 (10%)7 e inferior a la señalada en el estudio CUPIC (14,2%)8. Los fracasos de tratamiento durante las 12 semanas posteriores a la finalización del tratamiento (7,0%) fueron inferiores en nuestro estudio respecto a las señaladas en los ensayos clínicos (9-15%)6,7 y en el estudio CUPIC (27%)8.
Al comparar nuestros resultados con los obtenidos por otros autores, hay que tener en cuenta que nuestra población difiere principalmente de las de los ensayos clínicos u otros estudios observacionales en que no es homogénea, ya que incluye a diferente tipo de pacientes (naive y pretratados) con un mayor porcentaje de cirrosis, y que incluye a pacientes que no fueron analizados en los ensayos clínicos como son los respondedores nulos o los coinfectados con VIH. Además, la comparación de nuestros resultados con estudios de práctica clínica presenta la diferencia de que la efectividad en dichos estudios se evaluó en la semana 12 post-tratamiento mientras que en nuestro caso fue en la semana 24. No obstante, diversos autores señalan que existe una concordancia entre la RVS de la semana 12 y la 24 igual o superior al 98%10,11.
En conclusión, los resultados de efectividad obtenidos se sitúan dentro del intervalo establecido por los principales trabajos publicados tanto de eficacia como efectividad, resultando la cirrosis hepática como el principal factor que condiciona la efectividad.
Conflicto de intereses: Los autores declaran no tener conflictos de intereses.
Bibliografía
- World Health Organization Hepatitis C Fact Sheet 2012. (Consulta 1/10/2014). Disponible en: http://www.who. int/mediacentre/factsheets/fs164/en/.
- World Health Organization Hepatitis C. Weekly Epidemiological Record 1997;72:65-9.
- Marrero-Álvarez P, Gil-Gómez I, Monte-Boquet E, Lorente-Fernández L, Poveda-Andrés JL. Estudio de utilización de boceprevir y telaprevir para el tratamiento de la hepatitis C crónica. Farm Hosp. 2014;38:30-7.
- Manns MP, McHutchison JG, Gordon SC, Rustgi VK, Shiffman M, Reindollar R, et al. Peginterferon alfa-2b plus ribavirin compared with interferon alfa-2b plus ribavirin for initial treatment of chronic hepatitis C: a randomised trial. Lancet 2001;358:958-65.
- Fried MW, Shiffman ML, Reddy KR, Smith C, Marinos G, Goncales FL Jr, et al. Peginterferon alfa-2a plus ribavirin for chronic hepatitis C virus infection. N Engl J Med. 2002;347:975-82.
- Fred Poordad MD, Jonathan McCone Jr MD, Bruce R Bacon MD, Savino Bruno MD, Michael P Manns MD, Mark S, et al. Boceprevir for untreated chronic HCV genotype 1 infection. N Engl J Med. 2011;364:1195-206.
- Bruce R Bacon MD, Stuart C Gordon MD, Eric Lawitz, MD, Patrick Marcellin MD, John M Vierling MD, Stefan Zeuzem MD, et al. Boceprevir for previously treated chronic HCV genotype 1 infection. N Engl J Med. 2011;364:1207-17.
- Fontaine H, Hezode C, Dorival C, Larrey D, Zoulim F, de Ledinghen F, et al. SVR12 rates and safety of triple therapy including telaprevir or boceprevir in 485 cirrhotic non responders treated in the French Early Access Program (ANRS CO20-CUPIC). EASL 48th Annual Meeting (Consulta 1/10/2014). Disponible en: http://www.natap.org/2013/EASL/EASL_16.htm.
- Belpeiro PS, Hwang EW, Thomas IC, Mole LA, Cheung RC, Backus LI. Early virologic responses and hematologic safety of direct-acting antiviral therapies in veterans with chronic hepatitis C. Clin Gastroenterol and Hepatol. 2013;11:1021-7.
- Chen J, Florian J, Carter W, Fleischer RD, Hammerstom TS, Jadhav PR, et al. Earlier sustained virologic response end points for regulatory approval and dose selection of hepatitis C therapies. Gastroenterology. 2013;144: 1450-5.
- Martinot-Peignoux M, Stern C, Maylin S, Ripault MP, Boyer N, Leclere L, et al. Twelve weeks post-treatment follow-up is as relevant as 24 weeks to determine the sustained virologic response in patients with hepatitis C virus receiving pegylated interferon and ribavirin. Hepatology. 2010;51:1122-6.