Agüero-Rojas ME1, Venegas-Campos AC1,2,3, Pereira-Céspedes A3,4
- Caja Costarricense de Seguro Social. Hospital San Juan de Dios. Servicio de Farmacia. San José, Costa Rica.
- Caja Costarricense de Seguro Social. Hospital San Juan de Dios. Unidad de Atención Farmacéutica. San José, Costa Rica.
- Univ. de Costa Rica. Fac. de Farmacia. Departamento de Atención Farmacéutica y Farmacia Clínica. San José, Costa Rica.
- Univ. de Costa Rica. Fac. de Farmacia. Instituto de Investigaciones Farmacéuticas. Centro Nacional de Información de Medicamentos. San José, CR.
Fecha de recepción: 10/05/2023 – Fecha de aceptación: 14/06/2023
Correspondencia: Alfonso Pereira-Céspedes · Cuidad Universitaria Rodrigo Facio. Facultad de Farmacia, CIMED Montes de Oca, San José, Costa Rica CP: 11501-2060 · Email: alfonso.pereiracespedes@ucr.ac.cr
____
Objetivo: Caracterizar los niveles séricos de fósforo, calcio, hormona paratiroidea y aluminio, para evaluar la efectividad y seguridad del hidróxido de aluminio en hemodiálisis y promover intervenciones, desde el programa de Atención Farmacéutica, que permitan mejorar la toma de decisiones farmacoterapéuticas.
Método: Estudio exploratorio, descriptivo, retrospectivo, unicéntrico y de resultados de práctica clínica en pacientes en hemodiálisis pertenecientes al programa de Atención Farmacéutica de un hospital.
Resultado: Una población de 15 pacientes fueron incluidos en el estudio. Las medias ± desviaciones típicas de los parámetros analíticos fueron: 6.60 ± 2.45 mg/dl para fósforo, 9.09 ± 0.80 mg/dl para calcio, 127.24± 193.80 pg/ml para hormona paratiroidea intacta y 31.72 ± 9.74 μg/l para aluminio. El 73% presentaron hiperfosfatemia, 86% reportaron niveles de aluminio dentro de la zona gris (20 – 60 μg/l), 93% presentaron niveles normales de calcio sérico conformes a las recomendaciones y 73% reportaron niveles de hormona paratiroidea intacta por debajo del nivel normal recomendado (menor a 150 pg/ml). En cuanto al tratamiento prescrito con hidróxido de aluminio (tabletas de 200 mg y/o frascos de suspensión de 5,5% p/p) se tuvo que la dosis media fue 990.79 mg al día, con una desviación típica de 558.34 mg.
Conclusión: Se evidencian los parámetros séricos de interés, la efectividad y seguridad del hidróxido de aluminio en el grupo de pacientes estudiado. Además, se destaca la importancia del Programa de Atención Farmacéutica para la toma de decisiones farmacoterapéuticas en la práctica clínica. Otros estudios son necesarios
Palabras clave: Diálisis renal, hidróxido de aluminio, trastorno mineral y óseo asociado a la enfermedad renal crónica, atención farmacéutica
Effectiveness and safety of aluminium hydroxide in haemodialysis and pharmaceutical care. Clinical practice results
Objective: To characterise serum levels of phosphorus, calcium, parathyroid hormone and aluminium, in order to evaluate the effectiveness and safety of aluminium hydroxide in haemodialysis and to promote interventions, from the Pharmaceutical Care programme, to improve pharmacotherapeutic decision-making.
Methods: Exploratory, descriptive, retrospective, single-centre, retrospective, single-centre study of clinical practice outcomes in haemodialysis patients belonging to the Pharmaceutical Care programme of a hospital.
Results: A patient population of 15 patients was included in the study. The means ± standard deviations of the analytical parameters were: 6.60 ± 2.45 mg/dl for phosphorus, 9.09 ± 0.80 mg/dl for calcium, 127.24± 193.80 pg/ml for intact parathyroid hormone and 31.72 ± 9.74 μg/l for aluminium. Seventy-three per cent had hyperphosphataemia, 86% reported aluminium levels within the grey zone (20 – 60 μg/l), 93% had normal serum calcium levels according to recommendations and 73% reported intact parathyroid hormone levels below the recommended normal level (less than 150 pg/ml). Regarding the prescribed treatment with aluminium hydroxide (200 mg tablets and/or 5.5% w/w suspension bottles) the mean dose was 990.79 mg per day, with a standard deviation of 558.34 mg.
Conclusion: The serum parameters of interest, effectiveness and safety of aluminium hydroxide in the studied group of patients are evidenced. In addition, the importance of the Pharmaceutical Care Programme for pharmacotherapeutic decision-making in clinical practice is highlighted. Further studies are needed
Keywords: Renal Dialysis, aluminum hydroxide, chronic kidney disease-Mineral and Bone Disorder, pharmaceutical care
____
Introducción
Los pacientes en hemodiálisis, como tratamiento renal sustitutivo1, presentan alteraciones del metabolismo óseo y mineral (MOM), las cuales pueden manifestarse como anormalidades del calcio, el fósforo, la hormona paratiroidea (PTH) y la vitamina D2-5.
Como parte de las alternativas terapéuticas destacan: dieta, calcifediol, calcio, metabolitos activos de vitamina D, calcimiméticos y captores de fósforo2, 3.
Entre los captores o quelantes de fósforo, como parte del tratamiento de la hiperfosfatemia asociada, se incluye al hidróxido de aluminio, medicamento cada día más en desuso en la práctica clínica5, 6 por sus potenciales efectos tóxicos6, 7.
La toxicidad por aluminio ha sido implicada en: demencia o encefalopatía de diálisis, anemia microcítica sin déficit de hierro, osteomalacia y fracturas en diálisis5-7; es por esto que se recomienda administrar la dosis mínima terapéutica y que la duración del tratamiento se limite a unos pocos meses 2.
Las presentaciones de hidróxido de aluminio, disponibles en el Hospital San Juan de Dios (Caja Costarricense de Seguro Social) son: tabletas de 200 mg y suspensión oral al 5.5% p/p8. Otros quelantes disponibles son: carbonato de calcio y carbonato de sevelamer, los cuales están fuera del alcance de esta investigación.
Este estudio se justifica en el hallazgo previo de la Unidad de Atención Farmacéutica del hospital sobre la prescripción de dosis de hidróxido de aluminio superiores a las establecidas en ficha técnica. Además, desde setiembre del año 2011 hasta enero del año 2012, 35 pacientes del Servicio de Nefrología, mostraron concentraciones séricas de aluminio mayores a 60 μg/ml, es decir, presentaban concentraciones tóxicas; por tanto, se empezaron a ajustar las dosis de hidróxido de aluminio, reduciéndolas sustancialmente, según las concentraciones séricas de aluminio reportadas para cada paciente (datos propios no publicados del Servicio de Nefrología).
A partir de estos antecedentes, como parte de la práctica clínica, se realizaron analíticas de fósforo, aluminio, calcio y PTH a los pacientes de hemodiálisis, en tratamiento con hidróxido de aluminio, pero se desconocía la periodicidad de esos análisis clínicos y el estado general de salud de los pacientes en relación con los parámetros antes mencionados.
Dentro de este panorama el paciente en hemodiálisis puede sufrir un problema de salud asociado a una infectividad (cuantitativa o no) y/o a una inseguridad (cuantitativa o no) del hidróxido de aluminio, es decir resultados negativos asociados a la medicación (RNM)9. Estos RNM pueden ser causados por problemas relacionados con medicamentos9-12.
El presente estudio pretende caracterizar los niveles séricos de fósforo, calcio, hormona paratiroidea y aluminio, para evaluar la efectividad y seguridad del hidróxido de aluminio en hemodiálisis y promover intervenciones, desde el programa de Atención Farmacéutica, que permitan mejorar la toma de decisiones farmacoterapéuticas.
Material y Métodos
Tipo de estudio y ámbito
Estudio exploratorio, descriptivo, retrospectivo, unicéntrico y de resultados de práctica clínica (vida real) en pacientes en hemodiálisis del programa de Atención Farmacéutica en Nefrología del Hospital San Juan de Dios (perteneciente a la Caja Costarricense de Seguro Social) en tratamiento con hidróxido de aluminio como quelante del fósforo. El periodo de estudio fue de agosto del 2013 hasta marzo del 2014.
Población y selección de los participantes
Se trabajó con toda la población de pacientes (15 pacientes). No se trabajó con muestra. Se incluyeron pacientes (hombres y mujeres) en hemodiálisis (modalidades disponibles) del programa de Atención Farmacéutica, de todas las etnias y mayores de 18 años en tratamiento con hidróxido de aluminio como quelante del fósforo. Además, se excluyeron los pacientes que hubiesen fallecido durante el periodo de estudio (debido a que no fue posible recuperar esta información).
Variables de interés
Se analizaron las siguientes variables:
Demográficas (edad, sexo, lugar de domicilio).
Sobre el hidróxido de aluminio: dosis, pauta y duración del tratamiento, parámetros clínicos de efectividad (determinaciones séricas de fósforo, calcio y PTH intacta) y de seguridad (determinación sérica de aluminio). Es importante aclarar que el nivel sérico de aluminio fue el único parámetro de seguridad de interés para el estudio. Otras posibles sospechas de reacciones adversas no fueron analizadas.
Los valores séricos (bioquímicos) establecidos como normales (referentes o recomendados), para efectos de este estudio, fueron los establecidos según las guías Kidney Disease Outcomes Quality Initiative (KDOQI), Kidney Disease Improving Global Outcomes (KDIGO) y la Sociedad Española de Nefrología1,2.
Procedimientos de trabajo y recolección de información
Para la recolección de información se utilizaron como fuentes de información: las bases de datos, aplicaciones informáticas y registros disponibles en el hospital, a saber: base de datos del Programa de Atención Farmacéutica en Nefrología (selección de los pacientes), Sistema Integrado de Farmacias (SIFA) (dosis, pauta y duración del tratamiento con hidróxido de aluminio), historias clínicas de la Unidad de Hemodiálisis (variables demográficas), aplicación informática LabCore® de análisis clínicos y reportes de aluminio sérico del Laboratorio de Nefrología e Investigación Clínica (parámetros bioquímicos séricos de interés).
Los parámetros bioquímicos analizados fueron recuperados, a través de bases de datos e historia clínica del hospital, en el marco de la parte de la práctica clínica habitual. No se solicitaron analíticas adicionales como parte de este estudio.
Los datos se recolectaron, de manera confidencial y se registraron en una base de datos diseñada para fines de investigación (Hoja de Cálculo Microsoft® Excel para Windows®) codificada de manera anónima para las variables de interés.
Análisis estadístico
El análisis de normalidad fue realizado mediante análisis gráfico y prueba de Shapiro-Wilk.
Las variables categóricas y nominales se analizaron mediante las frecuencias relativas de sus categorías, expresadas en porcentajes, como parte del análisis descriptivo.
Las variables cuantitativas de razón proporcional se presentaron como mediana si su distribución no se acerca, de manera suficiente, a una normal y como moda, media ± desviación típica en caso contrario.
Para este análisis se empleó la aplicación informática Statistical Package for the Social Science ( IBM® SPSS®, Chicago, IL, Estados Unidos) (versión 19 para Windows®).
Consideraciones éticas
Se contó con la autorización del Comité de Ética del Hospital San Juan de Dios. En todo momento se garantizó la protección de datos personales, el cumplimiento de la normativa bioética para la investigación en Costa Rica y los principios éticos (respeto de la dignidad de las personas, principio de beneficencia, principio de no maleficencia, principio de autonomía y principio de justicia retributiva). Debido a las características de este estudio se autorizó la excepción del consentimiento informado conforme con la normativa del país.
Resultados
Características socio demográficas
Del total de 15 pacientes, 9 eran hombres (60%) y 6 eran mujeres (40%), teniéndose una relación hombres: mujeres de 1.5:1.
La media de las edades fue de 45.73 ± 11.81 años (edad máxima de 72 años y edad mínima de 23 años).
En cuanto al lugar de domicilio: el 73.3% (11 pacientes) habitaba en la provincia de San José, el 13.3% (2 pacientes) en la provincia de Puntarenas y el 13.3% (2 pacientes) se desconoce.
Parámetros séricos
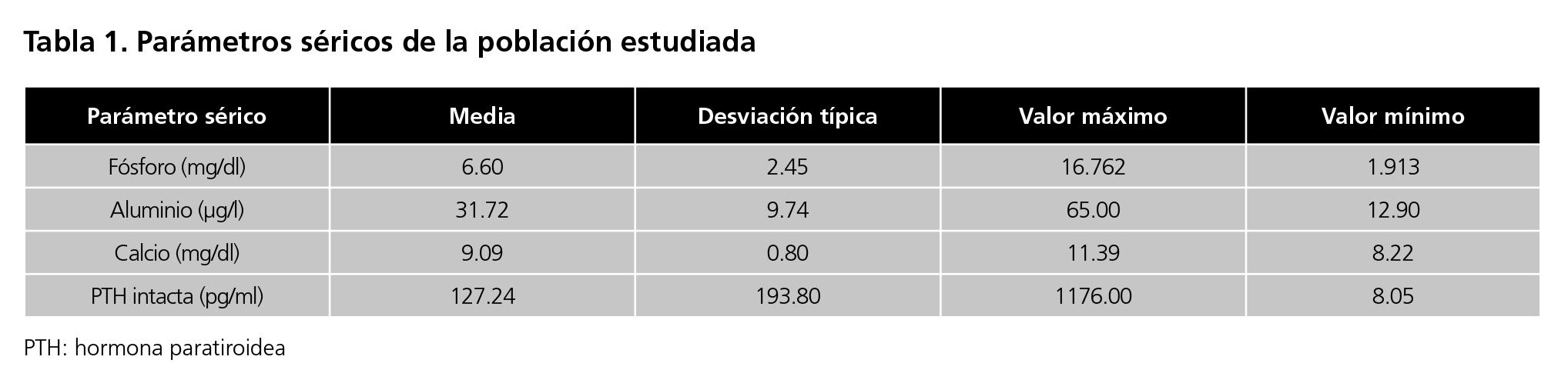
La tabla 1 resume los parámetros séricos analizados. La periodicidad de las analíticas de fósforo y calcio séricos fue de cada dos meses, de PTH intacta sérica aproximadamente cada dos meses y medio y de aluminio sérico cada 6 meses. Cuatro de los pacientes tenían registros solamente de un valor de aluminio sérico (pacientes de ingreso reciente a la unidad de hemodiálisis).
Tratamiento con hidróxido de aluminio.
Dosis diaria: En cuanto al tratamiento prescrito con hidróxido de aluminio (tabletas de 200 mg y/o frascos de suspensión de 5.5% p/p) se tiene que la dosis media fue 990.79 mg al día, con una desviación estándar de 558.34 mg (dosis menor de 400 mg y la dosis mayor de 2565 mg) y la moda de 1200 mg diarios.
Parámetros clínicos de efectividad: En cuanto a la relación de la efectividad del hidróxido de aluminio para el control de las alteraciones del MOM se destaca:
Fósforo: El 73 % (11 pacientes) presentó hiperfosfatemia (mayor a 5 mg/dl) y el 27% (4 pacientes) reportó niveles normales de fosforo séricos conformes con lo recomendado (2.5 – 5.0 mg/dl).
Calcio:El 93% (14 pacientes), registró niveles normales de calcio sérico conformes con las recomendaciones (8.4 – 10.0 mg/dl). Sin embargo, solamente un paciente (7%) reportó un valor máximo de 11.39 mg/dl, es decir hipercalcemia (superior a 11 mg/dl).
PTH intacta: El 73% (11 pacientes) reportó valores de PTH intacta por debajo del valor recomendado (menor a 150 pg/ml), 2 pacientes presentaron valores normales conformes con la recomendación (150 – 300 pg/ml) y 2 pacientes valores por encima de las recomendaciones(mayor a 300 pg/ml).
Parámetros clínicos de seguridad: Un 87% (13 pacientes) reportó valores de aluminio sérico dentro de los parámetros recomendados de zona gris (20 – 60 μg/l). De estos 13 pacientes: 9 pacientes mostraron una disminución en los niveles séricos de aluminio y 2 pacientes un aumento en estos niveles. Es importante aclarar que dos pacientes solo reportaron una determinación de aluminio sérico durante el periodo de estudio.
Discusión
El presente estudio, exploratorio y de resultados de práctica clínica (vida real), pretende caracterizar los niveles séricos de fósforo, calcio, hormona paratiroidea y aluminio, para evaluar la efectividad y seguridad del hidróxido de aluminio en hemodiálisis y promover intervenciones, desde el programa de Atención Farmacéutica, que permitan mejorar la toma de decisiones farmacoterapéuticas.
Las medias y desviaciones típicas de los parámetros bioquímicos encontrados fueron 6.60 ± 2.45 mg/dl para fósforo, 9.09 ± 0.80 mg/dl para calcio y 127.24± 193.80 pg/ml para PTH intacta. Estos hallazgos son coincidentes con el estudio de Marinovich SM et al13, el cual sugiere una mejoría en el control del calcio, el fósforo y una disminución de la PTH (alteraciones del MOM) en sus resultados principales.
A nivel internacional, las guías de práctica clínica reportan la disponibilidad de una gran cantidad de captores de fósforo, tales como: acetato cálcico, sevelamer, carbonato de lantano, captores basados en hierro y captores basados en aluminio2, 5, 14, 15.
Sin embargo, en Costa Rica la disponibilidad de estos captores se reduce al hidróxido de aluminio, carbonato de calcio y carbonato de sevelamer8, estos últimos disponibles en la seguridad social y el hospital. Sin embargo, se destaca que el carbonato de sevelamer tiene restricciones administrativas de prescripción en la seguridad social.
La efectividad del hidróxido de aluminio en hiperfosfatemia ha sido evaluado en otros estudios con resultados variables, sin embargo, estudios recientes son escasos 16.
Actualmente, la evidencia sugiere beneficios de seguridad y efectividad de otros captores2,5,14,17,18 tales como: acetato cálcico (menor sobrecarga de calcio y mayor efecto en distintos rangos de pH)2, asociación de acetato de calcio con carbonato de magnesio (disminución de los niveles de PTH y efectos anticalcificantes)2, carbonato de lantano (efectos secundarios poco relevantes, disminuye calcificación vascular y mejora supervivencia en diálisis)2, captores basados en hierro (relativamente bien tolerados y carecen de efectos pleiotrópicos de otros captores)2 y sevelamer (disminuye la progresión de calcificaciones aórticas y coronarias, reducción del lípidos, mejora del perfil inflamatorio y mejora de supervivencia en diálisis)2.
Es importante aclarar que las guías de práctica clínica refieren que hasta el momento, no hay ningún estudio que demuestre, con mayor nivel de evidencia, el captor de fósforo de primera elección, por lo que su prescripción debe ser acorde a las necesidades del paciente en el marco de la práctica clínica2,19. Sin embargo, sí hay evidencia de que el empleo de cualquier captor de fósforo en diálisis (excepto los basados en aluminio) se ha relacionado con un aumento en la supervivencia en diálisis2, 20.
Un 73% de los pacientes presentó hiperfosfatemia (RNM de inefectividad cuantitativa) en hemodiálisis. La hiperfosfatemia es un problema de salud frecuente en este tipo de pacientes, lo cual es coincidente con otros estudios5,18,21.Asimismo, un 27% de los pacientes presentó un nivel normal de fósforo sérico conforme con el valor bioquímico recomendado. Otros estudios publicados22 reportan una efectividad de captores del fósforo del 11% en general. Además, se hace referencia al desafío de la evaluación en la práctica clínica de su efectividad23.
El 93% de los pacientes registró niveles normales de calcio sérico conforme con el rango bioquímico recomendado, mientras que el 73% reportó un nivel de PTH intacta por debajo del valor bioquímico recomendado en las guías de práctica clínica2.
En relación con la seguridad, se destaca que: el 15.38% de los pacientes analizados presentaron niveles de aluminio sérico superiores al valor sérico recomendado. Lo anterior, confirma el riesgo de toxicidad de este quelante en hemodiálisis (riesgo de RNM), como ha sido reportado en otros estudios publicados6, 7, 22.
Por otra parte, en cuanto a la dosis diaria del hidróxido de aluminio, se destaca: una moda de 1200 mg, una media de 990.79 mg y una desviación típica de 558.34 mg; encontrándose estos resultados conformes con la ficha técnica del medicamento y la aplicación informática de información sanitaria UpToDate®. Además, es consecuente con que la media de aluminio sérico (31.72 ± 9.74μg/l) es conforme con el parámetro bioquímico recomendado.
Entre las limitaciones de este estudio se resalta el número restringido de pacientes, a pesar de trabajar con toda la población, lo cual se explica en: criterios de práctica clínica y en el carácter de investigación unicéntrica de resultados de vida real. Asimismo, ausencia de información registrada para algunas variables de interés en algunos casos individuales.
Además, se destaca la necesidad y relevancia de desarrollar investigación, en Atención Farmacéutica en Nefrología en el ámbito hospitalario costarricense, de manera conjunta con el Servicio de Nefrología. Por tanto, este estudio busca ser antecedente.
Conclusiones
En conclusión, se evidencia, en el grupo de pacientes estudiados, los valores séricos de calcio, fosforo, PTH y aluminio; así como la efectividad y seguridad del hidróxido de aluminio. Se destaca la importancia del Programa de Atención Farmacéutica para la toma de decisiones farmacoterapéuticas en la práctica clínica y la colaboración farmacéutico-nefrólogo.
Finalmente, se requieren otros estudios de vida real futuros que permitan generar una mayor evidencia y acciones, las cuales favorezcan el uso racional de captores de fósforo, así como la evaluación del impacto dela colaboración farmacéutico – nefrólogo para el alcance de los resultados clínicos, económicos y de calidad de vida en hemodiálisis en el contexto de Costa Rica.
Agradecimientos
Dr. Álvaro Herrera-Muñoz (Jefe del Servicio de Nefrología) y Dra. Marta Sánchez-Molina (Directora del Laboratorio de Nefrología e Investigación Clínica) del Hospital San Juan de Dios (Costa Rica) por su colaboración académica en el desarrollo de este estudio.
La presente investigación formó parte del trabajo fin de grado (Licenciatura en Farmacia, Universidad de Costa Rica) Caracterización de los niveles séricos de fósforo, aluminio, calcio y hormona paratiroidea en los pacientes hemodializados del Programa de Atención Farmacéutica del Hospital San Juan de Dios, en tratamiento con Hidróxido de aluminio; durante el periodo de agosto del 2013 a marzo del 2014.
Conflictos de intereses: Los autores declaran no tener conflictos de intereses.
Bibliografía
- García-Maset R, et al. Documento de información y consenso para la detección y manejo de la enfermedad renal crónica. Nefrología. 2022. doi: https://doi.org/10.1016/j.nefro.2021.07.010
- Torregrosa J-V, et al. Recomendaciones de la Sociedad Española de Nefrología para el manejo de las alteraciones del metabolismo óseo-mineral en los pacientes con enfermedad renal crónica: 2021 (SEN-MM). Nefrología. 2022. doi: https://doi.org/10.1016/j.nefro.2022.03.007
- Lundquist AL, Nigwekar SU. Optimal management of bone mineral disorders in chronic kidney disease and end stage renal disease. Curr Opin Nephrol Hypertens. 2016 Mar;25(2):120-6. doi: 10.1097/MNH.0000000000000203.
- Zoccali C, Mallamaci F, Cannata-Andía J. Phosphate Binders and Clinical Outcomes in Patients with Stage 5D Chronic Kidney Disease. Semin Dial. 2015 Nov-Dec;28(6):587-593. doi: 10.1111/sdi.12416.
- Emmett M. A comparison of clinically useful phosphorus binders for patients with chronic kidney failure. Kidney Int Suppl. 2004 Sep;(90):S25-32. doi: 10.1111/j.1523-1755.2004.09005.x.
- Arenas-Jiménez MD, Malek T, Gil MT, Moledous A, Núñez C, Álvarez U de F. Uso de captores alumínicos en hemodiálisis en la era del agua ultrapura. Nefrología [Internet]. 2008;28(2):123-238. Disponible en: https://revistanefrologia.com/es-uso-captores-aluminicos-hemodialisis-era-articulo-X0211699508032900
- Chuang PH, Tsai KF, Wang IK, et al. Blood Aluminum Levels in Patients with Hemodialysis and Peritoneal Dialysis. Int J Environ Res Public Health. 2022 Mar 24;19(7):3885. doi: 10.3390/ijerph19073885.
- Caja Costarricense de Seguro Social. Lista oficial de medicamentos y normativa. Caja Costarricense de Seguro Social; 2023.
- Faus-Dáder, MJ, Amariles-Muñoz, P, Martínez-Martínez, F. Atención Farmacéutica. Servicios farmacéuticos orientados al paciente. 2nd ed. Granada: Técnica Avicam; 2022.
- Al Raiisi F, Stewart D, Fernandez-Llimos F, Salgado TM, Mohamed MF, Cunningham S. Clinical pharmacy practice in the care of chronic kidney disease patients: a systematic review. Int J Clin Pharm. 2019 Jun;41(3):630-666. doi: 10.1007/s11096-019-00816-4
- Chua, P.C.P., Low, C.L., Lye, W.C. Drug-Related Problems in Hemodialysis Patients. Hemodialysis International. 2003;7(1): 73-104. doi: https://doi.org/10.1046/j.1492-7535.2003.01221.x
- Chemello C, Aguilera-Gómez M, Calleja-Hernández MA, Faus-Dáder MJ. Efecto del seguimiento farmacoterapéutico en pacientes con hiperparatiroidismo secundario tratados con cinecalcet. Farm Hosp. 2012; 36(5):321-327. DOI: 10.1016/j.farma.2011.03.008
- Marinovich SM, Negri AL. Trastorno mineral y óseo relacionado a la enfermedad renal crónica en pacientes prevalentes en diálisis crónica en el trienio 2011-2013 en Argentina. Nefrología, Diálisis y Trasplante [Internet].2015; 35(1): 24-31. Disponible en: https://www.revistarenal.org.ar/index.php/rndt/article/view/133/123
- Spasovski G. Advances in pharmacotherapy for hyperphosphatemia in renal disease. Expert Opin Pharmacother. 2015;16(17): 2589-2599. doi: 10.1517/14656566.2015.1092521.
- Sonikian M, Papachristou E, Goumenos DS. Optimal use of phosphate binders in chronic kidney disease. Expert Opin Pharmacother. 2013 Dic;14(18):2521-2532. doi: 10.1517/14656566.2013.852183
- Katopodis KP, Andrikos E, Pappas M, Siamopoulos KC. Effectiveness of aluminum hydroxide timing administration in relation to meals in controlling hyperphosphatemia in dialysis patients. Int J Artif Organs. 2005 Ago;28(8):803-807. doi: 10.1177/039139880502800806.
- González Casaús ML, González Parra E, Navas Serrano VM, Gracia Iguacel C, de Ribera Pieras P, de Los Ríos JE. Tratamiento de la hiperfosfatemia asociada a la enfermedad renal crónica con carbonato de lantano. nuevas evidencias. Dial Traspl [Internet]. 2011;32(3):102-107. DOI: https://doi.org/10.1016/j.dialis.2011.05.011
- Sturtevant JM, Hawley CM, Reiger K, et al. Efficacy and side-effect profile of sevelamer hydrochloride used in combination with conventional phosphate binders. Nephrology (Carlton). 2004 Dic;9(6):406-413. doi: 10.1111/j.1440-1797.2004.00338.x.
- Cannata-Andía JB, Fernández-Martín JL, Locatelli F, et al. Use of phosphate-binding agents is associated with a lower risk of mortality. Kidney Int. 2013 Nov;84(5):998-1008. doi: 10.1038/ki.2013.185
- Isakova T, Gutiérrez OM, Chang Y, et al. Phosphorus binders and survival on hemodialysis. J Am Soc Nephrol. 2009 Feb;20(2):388-396. doi: 10.1681/ASN.2008060609
- Redondo-Simón María del Carmen, Casuso-Jiménez Laura, Martínez-Jiménez Inmaculada, Rodríguez-Puertas José Francisco, Palacios-Gómez María Eugenia, Cara-Sánchez Encarnación. La hiperfosfatemia en paciente renal en programa de hemodiálisis. Enferm Nefrol [Internet]. 2015; 18(Suppl1): 124-124.
- Pepper R, Campbell N, Yaqoob MM, Roberts NB, Fan SL. Do oral aluminium phosphate binders cause accumulation of aluminium to toxic levels? BMC Nephrol. 2011 Oct 12;12:55. doi: 10.1186/1471-2369-12-55
- Caravaca F, Caravaca-Fontán F, Azevedo L, Luna E. How to assess the efficacy of phosphate binders. Nefrologia. 2017 May-Jun;37(3):311-319. doi: 10.1016/j.nefro.2016.11.012
_____
