Gómez Lluch MT1, Proy Vega B1, Notario Dongil C1, Nieto-Sandoval Martín de la Sierra P2, Alañón Pardo MM1, Valenzuela Gámez JC1
1 Servicio de Farmacia. Hospital General Mancha Centro. Alcázar de San Juan. Ciudad Real (España)
2 Servicio de Farmacia. Hospital General Universitario de Ciudad Real. Ciudad Real (España)
Fecha de recepción: 17/01/2020 – Fecha de aceptación: 23/02/2020
Correspondencia: María Teresa Gómez Lluch – Hospital General Mancha Centro (Servicio de Farmacia) – Av. Constitución, 3 – 13600 Alcázar de San Juan, Ciudad Real (España)
mglluch@sescam.jccm.es
____
RESUMEN
Objetivos: Los inhibidores de la tirosin quinasa (ITK) comprenden un conjunto de moléculas ampliamente utilizadas actualmente en onco-hematología. Los ITK han supuesto una ventaja para los pacientes, de forma que la administración oral favorece su autonomía, pero a su vez, su absorción gastrointestinal y, por ende, su biodisponibilidad, puede verse alterada por el PH-gástrico. Las interacciones con los fármacos modificadores del PH son un problema conocido y una consulta frecuente.
El objetivo del estudio fue analizar las interacciones ITK-fármacos modificadores del PH-gástrico y las discrepancias en diferentes bases de datos. Con los resultados, se elaboró una tabla, para proporcionar a los pacientes la información correcta y consensuada, y no generar así inseguridad que comprometa la adherencia al tratamiento o confianza hacia el profesional sanitario.
Métodos: Se exportaron de la web de la Agencia Española del Medicamento y Productos Sanitarios los fármacos clasificados como ITK directos (ATC: L01XE). Se consultó la interacción de éstos con los IBP, Anti-H2 y antiácidos en diversas fuentes y se resumieron los hallazgos.
Resultados y conclusiones: Para establecer una fuerte recomendación, es necesario consultar varias bases de datos, ya que las discrepancias o la información insuficiente pueden llevar a recomendaciones erróneas. Es importante establecer un consenso entre profesionales para realizar la recomendación correcta, y no ver comprometida la eficacia del tratamiento, con las importantes consecuencias que ello conllevaría.
Palabras clave: Inhibidores tirosin quinasa, fármacos modificadores del PH, interacción.
Effect of gastric-acid-reducing agents on the tyrosine kinasa inhibitors: contrasting information
SUMMARY
Objectives: Tyrosine kinase inhibitors (TKIs) include a group of molecules widely used in oncohematology today. Using the oral administration route of TKIs offers an advantage for the patient; favoring patient autonomy, however, oral administration also causes relevant new problems. Gastrointestinal absorption and, therefore, bioavailability, can be altered by gastric PH. Interactions of these TKIs with gastric acid reducing (GAR) drugs are a known problem and a frequent query in clinical practice.
The aim was to analyze ITK-GAR drugs interactions and discrepancies in different databases. Based on the results, a table was elaborated to provide the correct and consensed information, and thus not generate insecurity that compromises the adherence to the treatment or trust towards the healthcare professional.
Methods: Drugs classified as direct ITKs (ATC: L01XE) were exported from the Spanish Agency for Medicines and Health Products website. Their interaction with PPIs, Anti-H2 and antacids was consulted in different databases and findings were summarized.
Results and conclusions: To establish a strong recommendation, it is necessary to consult several databases, because of discrepancies or insufficient information can lead to erroneous recommendations. It is important to establish a consensus among professionals to make the correct recommendation, and not compromising the effectiveness of the treatment, which would entail important consequences.
Key words: Tyrosine kinase inhibitors, acid-reducing agents, drug interactions.
____
INTRODUCCIÓN Y OBJETIVOS
Con el fin de mejorar la efectividad y reducir los efectos adversos del tratamiento oncológico, en los últimos años los esfuerzos han ido centrados, entre otros, en el desarrollo de las llamadas terapias dirigidas. Una de las más prometedoras en el campo de la onco-hematología han sido los inhibidores de la tirosin quinasa (ITK).
Las tirosina quinasas son moléculas que resultan clave en la vía de transducción de señales celulares. Muchas células tumorales muestran una actividad anormal de tirosina quinasas específicas, afectando a la transcripción génica y síntesis de ADN. De ahí que los ITK sean utilizados para el tratamiento de diversas patologías, con el fin de interferir en vías de proliferación celular y angiogénesis tumoral1.
Hasta diciembre de 2019, en España estaban autorizados por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), 37 principios activos en el grupo terapéutico ATC L01XE: inhibidores directos de la tirosin-quinasa, lo que supone un reflejo del uso ya común en la práctica clínica2.
Una de las grandes diferencias de los ITK con la llamada tradicionalmente quimioterapia es la administración vía oral y de forma continua de estos fármacos, mejorando en este aspecto la calidad de vida del paciente.
Esta administración oral aporta ciertas ventajas, pero no hay que olvidar que nos enfrentamos a otro problema relevante referente a su administración, ya que la absorción gastrointestinal depende de varios factores, algunos inherentes, como por ejemplo su solubilidad, pero también de la existencia de posibles interacciones con otros fármacos orales.
Debido a sus propiedades débilmente básicas, los ITK poseen una solubilidad dependiente de PH3, por lo que pueden estar presentes en forma ionizada o no ionizada, dependiendo del pH en el estómago y el pKa del fármaco (pH en el cual el ITK alcanza el equilibrio entre la forma ionizada y no ionizada). Dado que la forma ionizada tiene mejor solubilidad, la absorción de ITK del tracto gastrointestinal es óptima a un pH intragástrico bajo; sin embargo, cuando éste es elevado (por ejemplo, debido al uso simultáneo de inhibidores de la bomba de protones (IBP)), el equilibrio se desplaza hacia la forma no ionizada del fármaco y la solubilidad y biodisponibilidad pueden disminuir significativamente4. De ahí que la administración conjunta de fármacos modificadores del PH e ITK pueda dar lugar a interacciones clínicamente relevantes por variaciones en la exposición al fármaco. Aunque no hay estudios prospectivos disponibles, algunos datos retrospectivos muestran que el uso de IBP concomitante se asoció con una menor eficacia de los ITK5-7.
Aunque los fármacos modificadores del PH se usan ampliamente en el tratamiento de los pacientes oncológicos, todavía hay mucha controversia sobre cómo gestionar estas interacciones fármaco-fármaco, siendo un problema conocido y una consulta frecuente. Además no hay que olvidar que la terapia con ITK se puede asociar con problemas gastrointestinales, por lo que existiría la indicación de fármacos gastroprotectores8.
A este escenario, se suma que la información obtenida para realizar una recomendación en base a esta interacción, no siempre concuerda según la fuente consultada. Lo cual, a menudo, exige un consenso por parte de los profesionales sanitarios implicados para proporcionar al paciente la información de forma consensuada y sin discrepancias.
El objetivo de este estudio fue analizar las interacciones descritas entre los ITK con los fármacos modificadores del PH gástrico en diferentes bases de datos. Con los resultados, realizar una tabla de consulta rápida con las recomendaciones para ser aplicadas en la práctica clínica diaria.
MÉTODOS
Se exportó de la AEMPS un listado con los ITK directos (clasificados en el grupo terapéutico L01XE). Se consultó la interacción de estos fármacos uno a uno con los IBP, Anti-H2 y antiácidos disponibles en las fuentes que se listan a continuación:
1. Ficha técnica del medicamento. (Disponible en la aplicación web de CIMA: https://cima.aemps.es/cima/publico/ home.html).
2. Herramienta online para la consulta rápida de interacciones entre citostáticos orales y otros medicamentos. GEDEFO. (Disponible en: http://interacitoral.sefh.es/interacciones).
3. Recurso online para el manejo seguro de los ITK. Incluido en el portal Oncology/PRO ESMO. (Disponible en: https://oncologypro.esmo.org/Oncology-in-Practice/Anti-Cancer-Agents-and-Biological-Therapy/Drug-Drug-Interactions-with-Kinase-Inhibitors/Types-of-Drug-Drug-Interactions/Acid-Reducing-Agents).
4. Lexicomp® Drug Interactions. (Disponible en: https:// www.uptodate.com/drug-interactions/?source=responsive_home#di-druglist).
5. Conciliación en el paciente oncológico. Guía de interacciones. UGC Farmacia HU Puerta del Mar. Cádiz9.
Con la información obtenida se construyó una tabla donde los hallazgos se resumieron en:
ND: no se refleja interacción o no hay información disponible.
NS: interacción considerada no significativa.
B: monitorizar tratamiento, pero no es necesaria acción.
D: considerar modificación de la terapia.
X: se recomienda evitar combinación.
Posteriormente se analizaron las discrepancias encontradas para cada uno de los ITK en las diferentes bases de datos consultadas.
RESULTADOS
Se exponen en la tabla anexa.
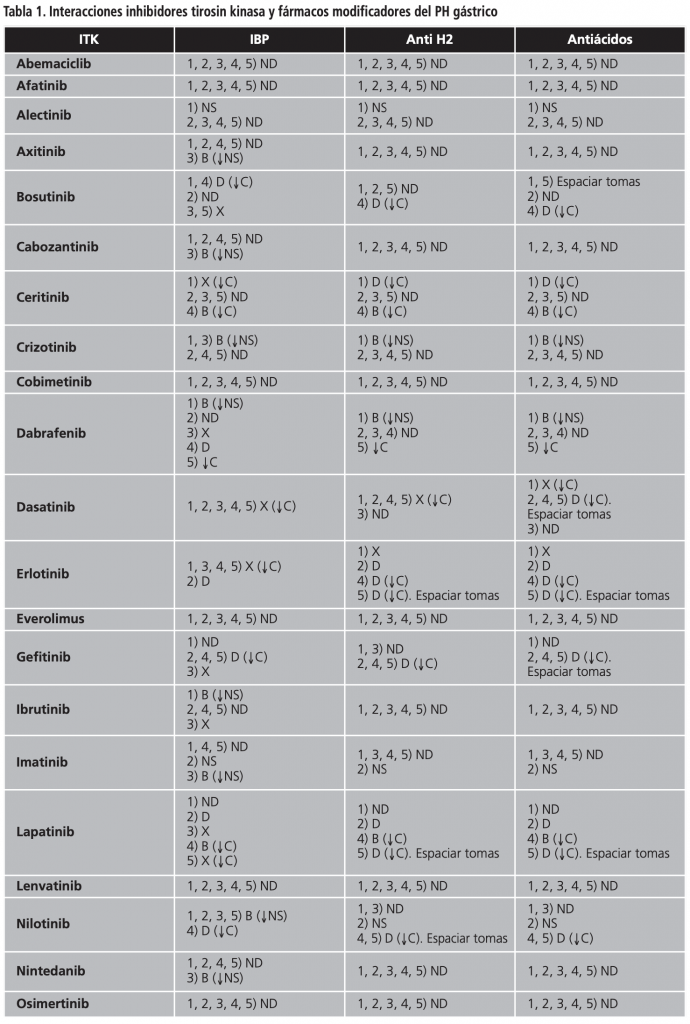
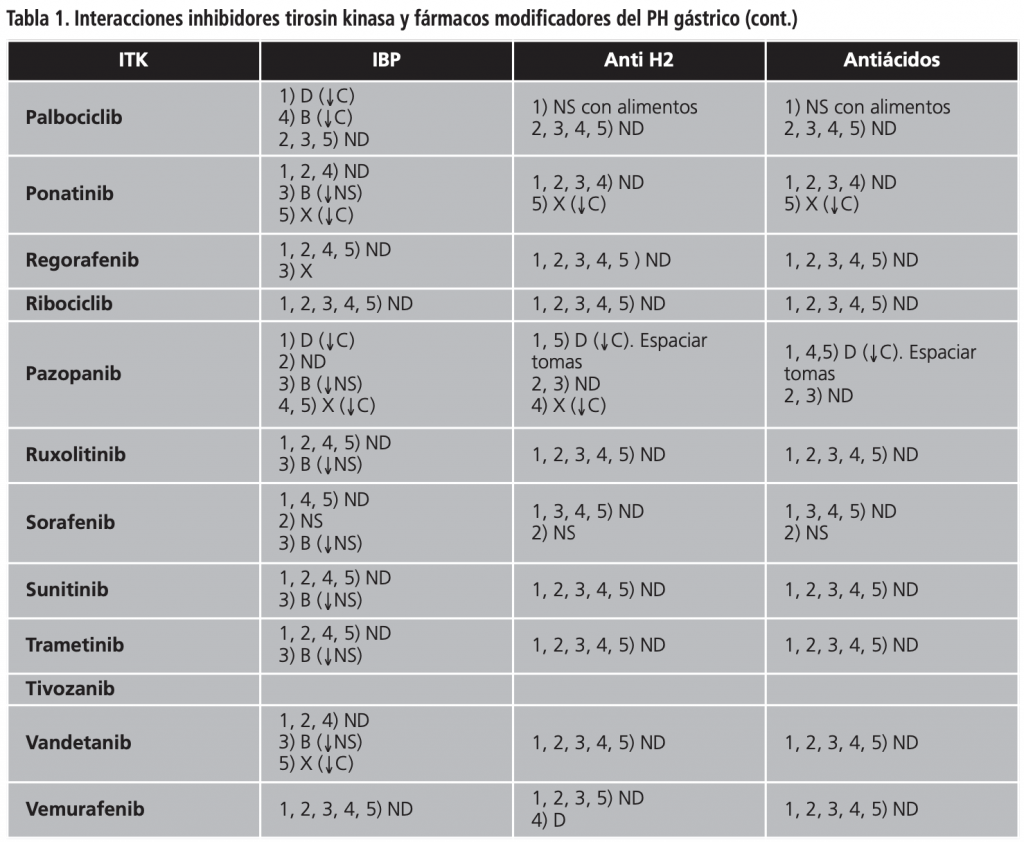
DISCUSIÓN
De estos resultados se deduce que, para establecer una fuerte recomendación, es necesario consultar varias bases de datos, ya que podemos encontrar discrepancias en la información o ésta puede ser insuficiente, llevando de esta manera a recomendaciones erróneas.
Los profesionales sanitarios, en ciertas ocasiones, nos encontramos con dificultad para establecer recomendaciones de salud, debido a la diferente y abundante bibliografía publicada en torno a un mismo tema. Esto dificulta la atención a los pacientes, y crea incluso discrepancias entre profesionales al encontrar información contradictoria.
En este caso, la búsqueda se basó en esas 5 bases de datos por ser las principalmente consultadas por los profesionales del sector.
En base a los resultados obtenidos, encontramos distintos escenarios. Por un lado, se da el caso de medicamentos, como el abemaciclib, donde la evidencia es escasa (debido a su reciente aparición). Otros, donde la recomendación de evitar la administración conjunta es clara, como el caso de dasatinib, y otros donde encontramos discrepancias, como el caso de pazopanib, donde habría que buscar alternativas o valorar beneficio/riesgo.
Con este análisis, y la información disponible recogida en una tabla, resulta más fácil establecer un consenso entre profesionales para realizar la recomendación correcta, en un escenario donde una recomendación errónea no debe comprometer la eficacia del tratamiento.
A su vez, la información consensuada es percibida por los pacientes como un signo de seguridad, que les aporta tranquilidad y les permite mantener una relación de confianza con los profesionales sanitarios que les atienden durante su proceso, lo cual se traduce en una mejora de la adherencia al tratamiento y en un mayor empoderamiento de éstos. Ello además tiene gran importancia, en la era en que nos encontramos, en la que los pacientes cada vez tienen más acceso a la información, pero deberían seguir necesitando al profesional para el análisis crítico de ésta.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
BIBLIOGRAFÍA
1. Krause DS, Van Etten RA. Tyrosine kinases as targets for cancer therapy. N Engl J Med. 2005;353:172-87.
2. Buscador para profesionales sanitarios. CIMA. Agencia Española Medicamentos y Productos Sanitarios. Disponible en: https://cima.aemps.es/cima/publico/buscadoravanzado.html [Acceso 25 feb. 2020].
3. Budha NR, Frymoyer A, Smelick GS, Jin JY, Yago MR, Dresser MJ, et al. Drug absorption interactions between oral targeted anticancer agents and PPIs: is pH-dependent solubility the Achilles heel of targeted therapy? Clin Pharmacol Ther. 2012 Aug;92(2):203-13.
4. Van Leeuwen RW, van Gelder T, Mathijssen RH, Jansman FG. Drug-drug interactions with tyrosine-kinase inhibitors: a clinical perspective. Lancet Oncol. 2014 Jul;15 (8):e315-26.
5. Chu MP, Ghosh S, Chambers CR, Basappa N, Butts CA, Chu Q, et al. Gastric acid suppression is associated with decreased erlotinib efficacy in non-small-cell lung cancer. Clin Lung Cancer. 2015;16(1):33-9.
6. Mir O, Lia M, Litie`re S, Le Cesne A, Sleijfer S, Leahy M, et al. Impact on outcome of concomitant administration of gastric acid suppression (GAS) therapy and pazopanib in soft tissue sarcoma (STS) patients treated within EORTC 62043/62072 trials.
7. Ha VH, Ngo M, Chu MP, Ghosh S, Sawyer MB, Chambers CR. Does gastric acid suppression affect sunitinib efficacy in patients with advanced or metastatic renal cell cancer? J Oncol Pharm Pract. 2015;21(3):194-200.
8. Oude Munnink TH, Schouwink JH, Colen HB, Movig KL. Erlotinib and gastric acid-reducing agents: a combination to avoid or to support? Clin Pharmacol Ther. 2014 Dec;96(6):658.
9. González-Carrascosa Vega T, editora. Conciliación en el Paciente Oncológico. Guía de interacciones. Septiembre 2013. ISBN: 978-84-695-8411-8.
____
