Rodríguez-Ferreras A, Zapico-García I
UGC Farmacia. Hospital Universitario Central de Asturias. Oviedo. Asturias (España)
Fecha de recepción: 12/09/2018 – Fecha de aceptación: 08/10/2018
Correspondencia
Adrián Rodríguez Ferreras – Avda. Roma, s/n – 33011 Oviedo, Asturias (España)
adrianrf7@gmail.com
____
Resumen
Objetivos: Estimar el tiempo empleado en la preparación y administración de las formas intravenosa (IV) y subcutánea (SC), así como los costes del fármaco y del material necesario en ambos procesos.
Métodos: Estudio observacional retrospectivo que incluyó a 64 pacientes mujeres con cáncer de mama HER2+ que recibieron trastuzumab SC. Se calculó el coste de las dosis administradas, estimándose la dosis que hubieran recibido las pacientes en el caso de haber sido tratadas con traztuzumab IV (incluyendo la dosis de carga). Se tuvo en cuenta el tiempo necesario para la preparación de ambas formas farmacéuticas y el necesario para la administración en Hospital de Día. Se realizó un análisis de sensibilidad considerando el peso como principal variable, así como el aprovechamiento o no de los viales en el proceso de preparación.
Resultados: La preparación de la forma SC supone un ahorro medio de 7 minutos respecto a la preparación de la forma IV. Teniendo en cuenta el peso medio de la muestra del estudio, la administración SC supone un ahorro de 255,96 €/ciclo. El hecho de utilizar la vía intravenosa conlleva la administración de una dosis de carga inicial, suponiendo un coste adicional de 477,40 €/paciente. En términos de acondicionamiento, la utilización de la forma SC supondría un ahorro de 438.272 € en cuanto a salario del personal de enfermería.
Conclusiones: Los resultados obtenidos en este estudio favorecen a la formulación SC de trastuzumab, suponiendo una mejora para los pacientes y para el SNS.
Palabras clave: Trastuzumab, minimización de costes, subcutáneo, cáncer de mama HER2+, administración, costes, biosimilar.
____
Cost-minimization analysis in the treatment of HER2+ breast cancer: IV vs. SC trastuzumab
Summary
Objectives: To determine the time required for preparation and administration for both intravenous (IV) and subcutaneous (SC) trastuzumab, as well as the drug and necessary material costs.
Methods: A retrospective observational study that included 64 women with HER2+ breast cancer who received SC trastuzumab. The cost of the administered doses was calculated, estimating the dose that patients would have received in case of having been treated with IV traztuzumab (including loading dose). The time required for preparation of both pharmaceutical forms and the time needed for administration at Day Hospital were taken into account. A sensitivity analysis was carried out considering the weight as the main variable, as well as the vials optimization in the preparation process.
Results: Preparation of SC trastuzumab means an average saving of 7 minutes compared to the IV form. Considering the average weight of the study sample, the SC administration represents a saving of € 255.96/cycle. The fact of using the intravenous route involves the administration of an initial loading dose, assuming an additional cost of € 477.40/patient. In terms of conditioning, the use of the SC form would mean a saving of € 438,272 in nursing staff salary.
Conclusions: The results obtained in this study favor the SC formulation of trastuzumab, assuming an improvement for the patients and for the NHS.
Key Words: Trastuzumab, cost-minimization analysis, HER2+ breast cancer, administration, costs, biosimilar.
____
Introducción
Trastuzumab es un anticuerpo monoclonal IgG1 humanizado recombinante contra el receptor 2 del factor de crecimiento epidérmico humano (HER2). La unión del trastuzumab a HER2 inhibe la vía de señalización de HER2 independiente del ligando y previene la división proteolítica de su dominio extracelular. Además, trastuzumab es un potente mediador de la citotoxicidad dependiente de anticuerpos mediada por células (ADCC). La sobre-expresión de HER2 se observa en el 20%-30% de los cánceres de mama primarios1.
Trastuzumab puede ser administrado cada 7 o 21 días en perfusión intravenosa, calculando la dosis en función del peso del paciente. En la pauta trisemanal la dosis de inicio recomendada de trastuzumab es de 8 mg/Kg de peso, con una dosis de mantenimiento de 6 mg/Kg. En la pauta semanal la dosis recomendada es de 4 mg/Kg, continuando con 2 mg/Kg cada 7 días1.
La dosis inicial de trastuzumab IV se debe administrar durante 90 minutos por un profesional sanitario entrenado en el manejo de anafilaxis y con un dispositivo de emergencia disponible. Si esta es bien tolerada, las siguientes dosis pueden administrarse en 30 minutos.
Se debe observar a los pacientes durante al menos seis horas desde el comienzo de la primera perfusión y durante dos horas desde el comienzo de las siguientes1,2.
En Europa se aprobó en 2013 la presentación SC a dosis fija de 600 mg. Esta formulación requiere menos tiempo de preparación y administración que la forma IV4. Por lo tanto, el reemplazo de la forma IV por la SC podría reducir el tiempo y los recursos empleados en los tratamientos con trastuzumab, tanto desde el punto de vista del Sistema Nacional de Salud (SNS) como de los pacientes y sus familiares2,3. Además, el tratamiento con trastuzumab SC no requiere dosis de carga (DC) ni cálculo de dosis en función del peso, reduciendo así el tiempo y la posibilidad de errores2. Los resultados de los estudios HannaH y PrefHer realizados en pacientes con cáncer de mama HER2+, demostraron la no inferioridad de la formulación SC respecto a la IV en términos de eficacia, con un perfil farmacocinético y de seguridad similar. Por lo tanto, se puede considerar la administración SC como una alternativa de tratamiento válida4,5.
Objetivos
Los objetivos de este estudio fueron: 1) estimar el tiempo empleado en la preparación y administración de las formas IV y SC, 2) costes derivados del empleo de una u otra alternativa; coste del propio fármaco y del material necesario para su acondicionamiento y administración, y coste generado en base al tiempo empleado para su preparación y administración.
Material y métodos
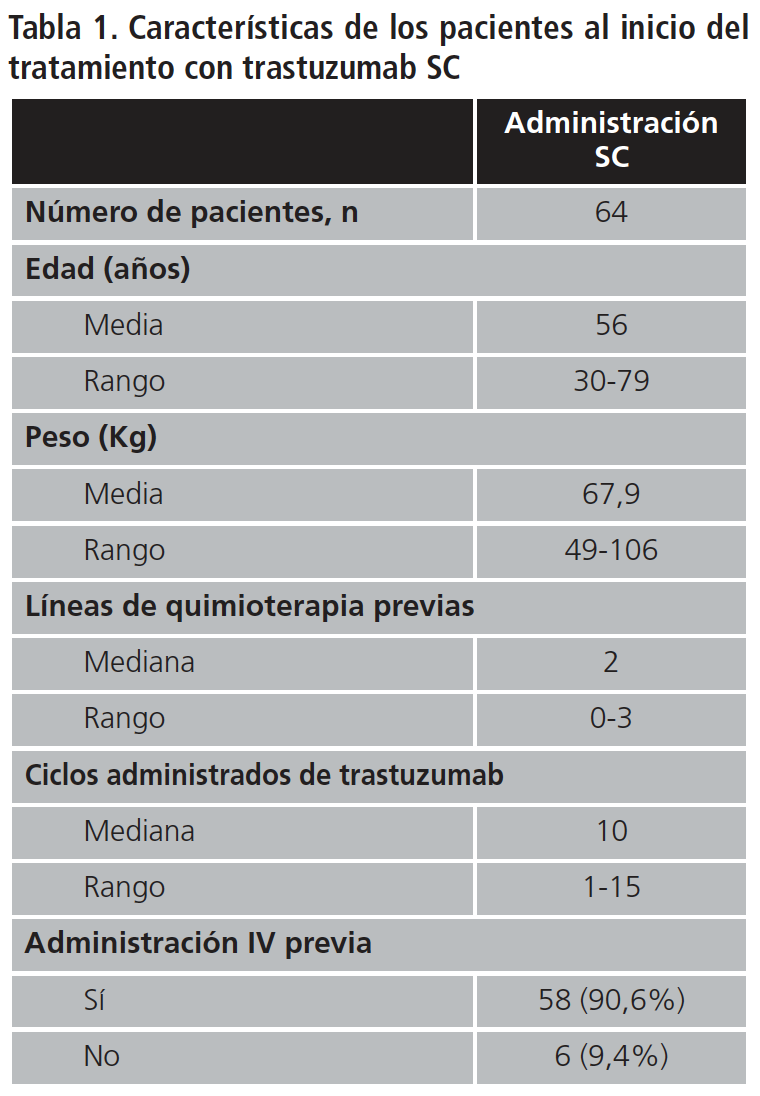
Estudio observacional retrospectivo en el que se analizaron 64 pacientes mujeres con cáncer de mama HER2+ que recibieron trastuzumab SC entre diciembre de 2015 y julio de 2017 (las características basales de las pacientes se pueden ver en la Tabla 1). Para calcular los costes referentes a la administración IV se estimó la dosis que hubieran recibido tales pacientes en caso de haber sido tratadas con la presentación IV. Para ello se registró el peso y se obtuvo el valor medio. Además, se calculó la dosis correspondiente para la DC así como para las administraciones sucesivas.
Para contabilizar el tiempo empleado tanto en la preparación como en la administración se tomó un valor medio en minutos en ambos procesos. La Figura 1 muestra los pasos en la preparación de ambas formas farmacéuticas. El tiempo que el paciente permaneció en el Hospital de Día de Oncología se calculó sumando el tiempo requerido para la administración y el tiempo de observación necesario en el caso de la forma IV.
Los costes implicados en la preparación y administración se obtuvieron multiplicando el tiempo empleado en cada caso por la cuantía en euros correspondiente al salario base bruto del personal de enfermería (según las retribuciones del Servicio de Salud del Principado de Asturias para el personal sanitario; BOPA 140, 2016)6. En el análisis de sensibilidad se consideró el peso como principal variable que genera incertidumbre. Se calculó el coste del fármaco IV con un valor de peso ±5% del valor medio. También se consideró el aprovechamiento de los viales teniendo en cuenta la posibilidad de administración a más de una paciente el mismo día. Además, se discutirán aspectos relacionados con la calidad de vida de las pacientes, como la posible extravasación que conlleva la administración IV o el malestar que genera el tiempo de espera necesario en Hospital de Día. También se comentará la diferencia en la gestión de residuos para ambas alternativas y la introducción en el mercado del medicamento biosimilar de trastuzumab.

Resultados
Tiempo empleado en la preparación y administración
Se evidenció una disminución en el tiempo de preparación de la forma SC respecto a la IV (3 vs. 10 min), debido al menor uso de material y a la no necesidad de reconstitución en la forma SC. En Hospital de Día, trastuzumab SC supuso un ahorro de tiempo debido a la ausencia de colocación de catéter, administración de premedicación y monitorización durante la administración. La inyección subcutánea se administró en un tiempo medio de 1,5 min mientras que la infusión intravenosa hubiera supuesto una demora de 150 min para la segunda perfusión y sucesivas (30 minutos de perfusión y 120 minutos de observación) y 450 min para la primera administración (90 minutos de perfusión y 360 minutos de monitorización post-infusión).
Extrapolando a las 64 pacientes incluidas en el estudio, y considerando la mediana de ciclos administrados (10), los tiempos de preparación y administración serían los siguientes:
• La preparación de la forma IV hubiera llevado un total de 6.400 minutos (106,7 horas) frente a los 1.920 minutos (32 horas) que supuso el acondicionamiento de la forma SC.
• La administración IV hubiera supuesto un tiempo total de 115.200 minutos (1.920 horas) mientras que la inyección SC ha conllevado un total de 960 minutos. Esto ha supuesto un ahorro de tiempo del personal de enfermería de 114.240 minutos (1.904 horas).
El ahorro de tiempo total obtenido al utilizar la forma SC en términos de preparación y administración fue de 118.720 minutos (1.978,7 horas).
Costes directos
El coste de los viales utilizado en este estudio es de 1.326 € para la forma SC y 527,32 € para la IV. El coste que supondría una administración IV teniendo en cuenta el peso medio (67,9 Kg) y una pauta trisemanal sería de 1.581,96 €/ciclo (considerando la utilización de los viales para un único paciente). El coste de la administración SC se corresponde con el precio del vial (1.326 €), lo que supone un ahorro a favor de la administración SC de 255,96 €/ciclo.
La mediana de ciclos administrados fue de 10 (rango: 1-15). La media de viales utilizados para la administración por vía IV sería de 26 (SD: 13,8). El coste de la administración IV por 10 ciclos sería de 13.710,32 € frente a 13.260 € en el caso de la forma SC, suponiendo un ahorro de 450,32 €/10 ciclos.
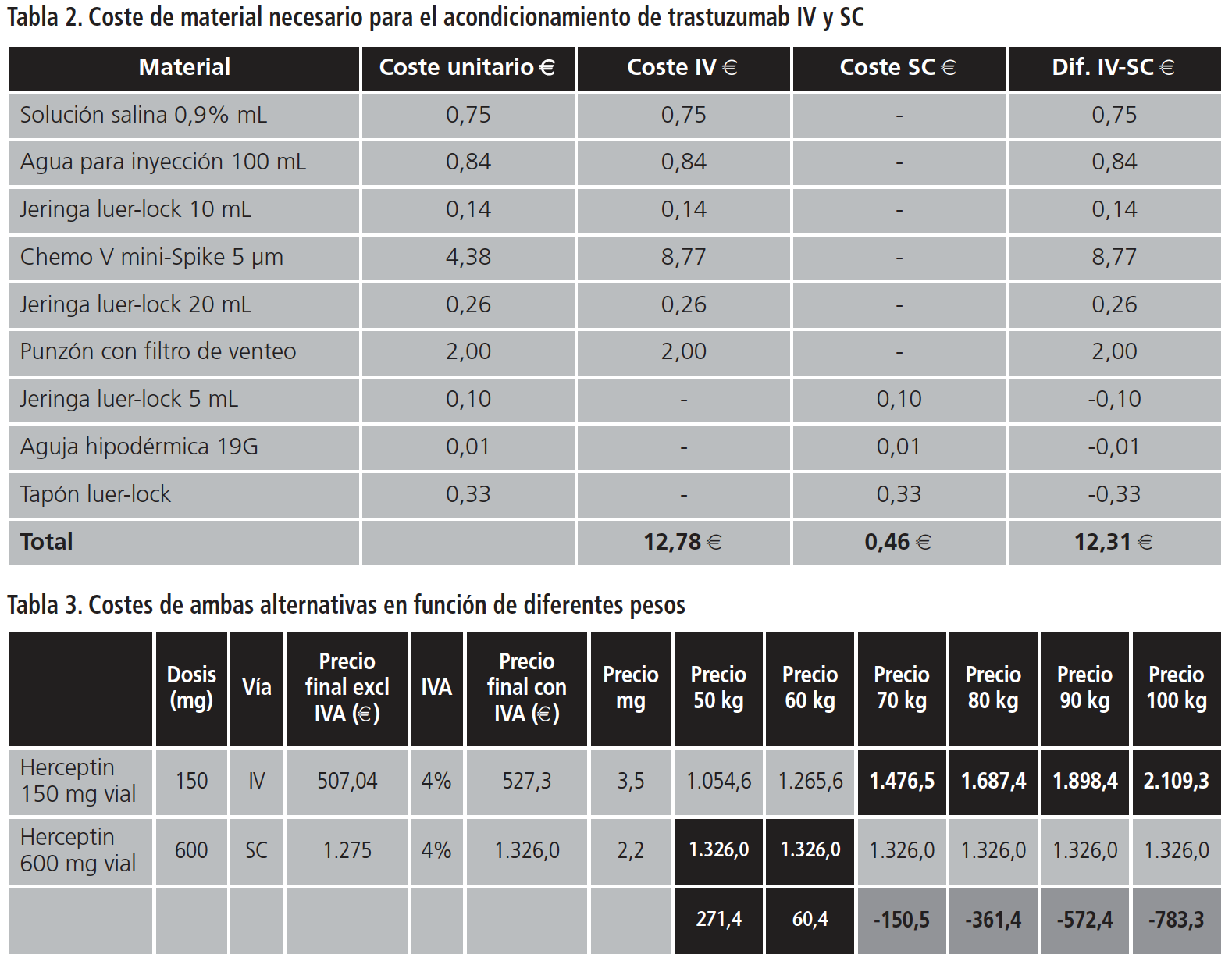
Además, para la administración IV en la pauta trisemanal se requiere una DC (8 mg/Kg) que supone un aumento de 2 mg/Kg adicional, comportando un gasto extra de 477,40 € por paciente. Se calculó también el total en euros que supuso el tratamiento de las 64 pacientes con la forma SC y se estimó el coste que hubiera supuesto el mismo tratamiento IV considerando el peso real de cada una de las pacientes y la DC inicial, siendo respectivamente 765.102 € y 862.885,4 €. En la Tabla 2 se indican los precios del material necesario para el acondicionamiento de ambas formas farmacéuticas. Tal y como se observa en dicha Tabla, las diferencias en cuanto a coste de material para las diferentes alternativas son notables. El coste total está calculado para una sola administración de trastuzumab, por lo que en el caso de utilizar la forma SC se ahorrarían 12,31 €/administración.
En la Tabla 3 se muestran los costes de ambas alternativas en función de diferentes pesos teóricos. Se observa una evolución favorable del gasto a favor de la forma SC a partir de pesos iguales o mayores a 70 Kg.
El valor monetario de la hora de trabajo de enfermería es de 5,87 €6. Teniendo en cuenta el tiempo invertido en la preparación de la forma de administración SC, el coste que supuso la preparación para una sola administración fue de 0,29 €. Para el total de las pacientes y considerando 10 ciclos administrados, el valor fue de 187,84 €. En el caso de la preparación de la forma IV, una administración supondría un coste de 0,97 €. Considerando las 64 mujeres y la mediana de ciclos administrados el coste sería de 626,11 €. En términos de acondicionamiento, la utilización de la forma SC conllevaría un ahorro de 438,27 € en cuanto a salario del personal de enfermería.
Considerando ahora el tiempo invertido en Hospital de Día; el coste necesario para una administración de trastuzumab SC fue de 0,14 € (para todas las pacientes x 10 ciclos: 93,92 €). En el caso de la administración IV; 14,67 €/dosis (8.452,8 € para todas las pacientes y teniendo en cuenta 9 ciclos, excluyendo DC). Considerando la dosis de carga inicial, el total del gasto salarial de enfermería necesario ascendería a 11.270,4 € para las 64 pacientes y los 10 ciclos incluyendo la DC.
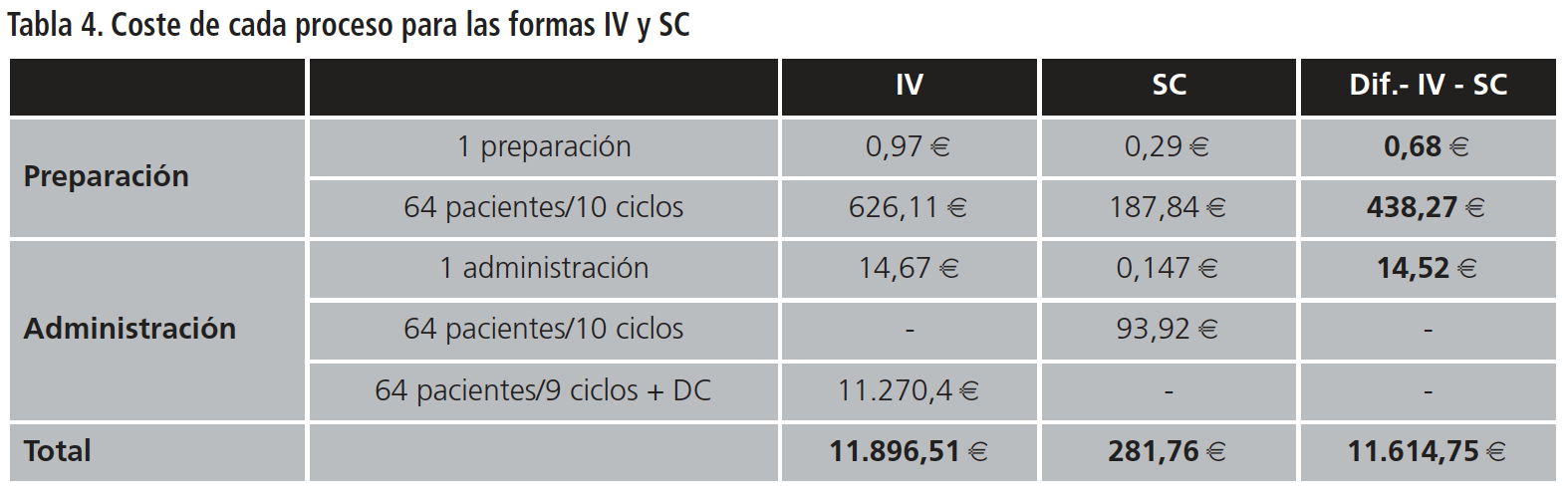
Se observó una reducción del coste generado en concepto de retribuciones del personal de enfermería con la utilización de la forma SC, siendo el total de 281,76 € contando los procesos de preparación y administración. En cambio, con la forma IV el total ascendería a 11.896,51 €. La diferencia entre ambas alternativas puede considerarse notoria: 11.614,75 €. En la Tabla 4 se muestran de forma resumida los costes de preparación y administración para las dos formas farmacéuticas.
Costes totales
Considerando el coste de los viales, el material empleado, y el tiempo del personal en la preparación y administración el total en euros para las formas IV y SC sería de 882.961 € y 765.680 € respectivamente. Con una diferencia neta a favor de la forma SC de 117.282 €.
Análisis de sensibilidad
Existe una ligera diferencia en el total de viales utilizados para administración IV si consideramos un aprovechamiento máximo de los miligramos contenidos en cada vial o no, teniendo en cuenta la limitada estabilidad de la solución reconstituida (48 horas entre 2-8ºC)7. Administrando el fármaco a varias pacientes el mismo día se consiguió un consumo total de 1.627,3 viales frente a los 1.636 que hubiera supuesto la no optimización del contenido de los mismos. Esto supone una diferencia de 8 viales netos (4.218,56 €).
La forma farmacéutica IV se dosifica en función del peso del paciente. En este trabajo se ha considerado el peso medio de nuestra población muestral para estimar los costes que hubiera supuesto la utilización de dicha formulación. Dado que el peso es una variable interindividual que puede dar un resultado menos exacto de los costes antes descritos, se ha considerado como uno de los factores que genera mayor incertidumbre en el análisis. Para ello se ha calculado un rango de peso tomando ±5% del valor medio (64,5 a 71,3 Kg), y se han estimado de nuevo los costes.
• Para un peso de 64,5 Kg: el aprovechamiento de los viales conllevaría un gasto de 1.360,49 €/ciclo frente a 1.581,96 € en caso contrario.
• Para un peso de 71,3 Kg: el aprovechamiento de los viales conllevaría un gasto de 1.503,92 € frente a 1.581,96 € en caso contrario.
Si consideramos una sola dosis de trastuzumab la diferencia no es alta, pero teniendo en cuenta la mediana de ciclos administrados a las 64 pacientes del estudio, el incremento sería considerable.
Discusión
Este estudio describe el tiempo invertido en la preparación y administración de trastuzumab IV y SC y los costes que ello supone. Los resultados muestran que remplazar la forma IV por la SC supondría una simplificación de los procesos de preparación y administración y una reducción significativa del tiempo empleado por el personal sanitario, con el coste asociado que ello conlleva. Así como una reducción del coste total del medicamento.
El menor tiempo de administración para el paciente en Hospital de Día supondría un ahorro de costes. Esto permitiría tratar el mismo número de pacientes con menos recursos o más pacientes con los mismos recursos. También podría traducirse en mejoras en la calidad asistencial, por ejemplo, tratar el mismo número de pacientes pero con una atención más individualizada y mayor calidad.
Se ha notificado un mayor número de casos de pacientes con complicaciones o disconfort durante la infusión. La necesidad de colocación de catéter puede generar complicaciones de tipo infeccioso (al tratarse en algunos casos de pacientes inmunodeprimidos), flebitis o incluso extravasación. Sin olvidar que el mayor tiempo de administración requerido para la forma IV genera mayor incomodidad y malestar en los pacientes al permanecer más horas en el hospital, afectando negativamente a su calidad de vida.
La administración SC generaría un ahorro si tenemos en cuenta la gestión de los residuos generados. El menor uso de material fungible y la utilización de un solo vial por paciente reducirían costes en este aspecto. Un beneficio extra para la formulación SC es que permitiría un tratamiento más flexible de cara a los pacientes, pudiéndolo adaptar mejor a sus necesidades laborales y sociales.
Los resultados de este estudio pueden verse alterados en un futuro próximo debido a la introducción en el mercado de trastuzumab biosimilar8. La comercialización producirá seguramente un abaratamiento en el precio de adquisición del medicamento IV9, teniendo que reevaluarse entonces la posible sustitución por la forma SC.
Por el momento y con la evaluación realizada en este estudio, se puede concluir que los resultados clínicos y económicos favorecen a la formulación SC de trastuzumab, suponiendo una mejora para los pacientes y para el SNS.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
Bibliografía
1. Agemed: Agencia Española de Medicamentos y Productos Sanitarios. CIMA (centro de información de medicamentos). Ficha técnica trastuzumab [Internet]. España: Agencia Española de Medicamentos y Productos Sanitarios. Disponible en: www.ema.europa.eu/docs/es_ES/document_library/EPAR_-_Product_Information/human/000278/WC500074922.pdf.
2. Ismael G, Hegg R, Muehlbauer S, Heinzmann D, Lum B, Kim SB, et al. Subcutaneous versus intravenous administration of (neo)adjuvant trastuzumab in patients with HER2-positive, clinical stage I-III breast cancer (HannaH study): a phase 3, open-label, multicentre, randomised trial. Lancet Oncol. Sep 2012;13(9):869e78.
3. Olofsson S, Norrlid H, Karlsson E, Wilking U, Ragnarson Tennvall G. Societal cost of subcutaneous and intravenous trastuzumab for HER2-positive breast cancer e An observational study prospectively recording resource utilization in a Swedish healthcare setting. Breast. 2016 Oct;29:140-6. doi: 10.1016/j.breast.2016.07.008.
4. Lopez-Vivanco G, Salvador J, Diez R, López D, De Salas-Cansado M, Navarro B. Cost minimization analysis of treatment with intravenous or subcutaneous trastuzumab in patients with HER2-positive breast cancer in Spain. Clin Transl Oncol. 2017 Jun 2. doi: 10.1007/s12094-017-1684-4.
5. Pivot X, Gligorov J, Müller V, Barrett-Lee P, Verma S, Knoop A, Curigliano G, et al. Preference for subcutaneous or intravenous administration of trastuzumab in patients with HER2-positive early breast cancer (PrefHer): an open-label randomised study. Lancet Oncol. 2013 Sep; 14(10):962-70. doi: 10.1016/S1470-2045(13)70383-8.
6. Boletín oficial del Principado de Asturias, Consejería de Hacienda y Sector Público. Acuerdo de 16 de junio de 2016, del Consejo de Gobierno, por el que se fijan para 2016 las cuantías de las retribuciones del personal al servicio de la Administración del Principado de Asturias. Núm. 140 de 17-vi-2016.
7. Guía de estabilidad y condiciones de administración de citostáticos, anticuerpos monoclonales y otros medicamentos. Font-Serra N, Mullera-Martí M, Cardenete-Ornaque J, Cardona-Pera D, Mangues-Bafalluy MA. Edimsa. ISBN-13: 978-84-7714-410-6.
8. Rugo HS, Barve A, Waller CF, Hernandez-Bronchud M, Herson J, Yuan J, et al. Effect of a Proposed Trastuzumab Biosimilar Compared With Trastuzumab on Overall Response Rate in Patients With ERBB2 (HER2)-Positive Metastatic Breast Cancer: A Randomized Clinical Trial. JAMA. 2017 Jan 3;317(1):37-47. doi: 10.1001.
9. American Association for Cancer Research. Trastuzumab Biosimilar on Track for Approval. Cancer Discov. 2017 Aug 16. doi: 10.1158/2159-8290.
____
