Rev. OFIL 2018, 28;1:15-21
Fecha de recepción: 27/01/2017 – Fecha de aceptación: 28/01/2017
Valero García S1, Vila Clérigues N2, López Briz E2, Borrás Almenar C2, Escobar Cava P2, Poveda Andrés JL2
1 Instituto de Investigación Sanitaria La Fe. Valencia (España)
2 Hospital Universitario y Politécnico La Fe. Valencia (España)
____
Correspondencia:
Silvia Valero García
C/Albal, 16 – esc dcha – piso 4º – pta 13
46200 Paiporta (Valencia)
Correo electrónico: silvia.valero.garcia@gmail.com
____
Resumen
Introducción: La exposición laboral a determinados fármacos puede provocar efectos nocivos en el personal sanitario si no se toman las medidas de protección adecuadas. La manipulación de los considerados “fármacos peligrosos” (FP) está siendo revisada por parte de sociedades científicas y otras organizaciones, lo que obliga a los Servicios de Farmacia (SF) a establecer las medidas oportunas para la adecuación de sus procedimientos a la legislación que resulta de aplicación. Este artículo muestra las acciones desarrolladas por el SF del Hospital Universitario y Politécnico La Fe en este ámbito y el impacto asistencial que supuso la implantación de dichas acciones.
Métodos: Estudio descriptivo. Las medidas se clasifican en cuatro ámbitos de actuación: establecimiento de un listado de FP, mejora de la seguridad en la manipulación, normalización de procedimientos de trabajo y circuitos, y formación e información.
Resultados: Se estableció un listado de FP. Se dotó al SF de medidas de protección colectiva y a la totalidad de las unidades de hospitalización (UH) con medidas de protección individuales. Se desarrollaron procedimientos normalizados de trabajo de diferente alcance, estandarizándose circuitos y almacenamiento especiales, y se llevaron a cabo sesiones formativas e informativas en todo el hospital.
Discusión: La adecuación a las recomendaciones internacionales resulta imprescindible para la protección de los profesionales sanitarios implicados en el circuito farmacoterapéutico de FP. El SF es el agente ideal para liderar las actuaciones necesarias en colaboración con el resto de servicios implicados y con la dirección del centro.
Palabras clave: Medicamentos peligrosos, gestión, seguridad laboral.
____
Introducción
La definición de fármaco peligroso (FP) fue utilizado por primera vez en los años 90 por la American Society of Hospital Pharmacists (ASHP)1 y posteriormente adoptada por el National Institute for Occupational Safety and Health (NIOSH) en 20042.
A su vez, el NIOSH estableció el primer listado de FP, que incluía mayoritariamente fármacos antineoplásicos, pero también antivíricos o medicamentos hormonales entre otros2. Dicha lista ha sufrido diversos procesos de revisión a lo largo del tiempo, siendo la última revisión disponible la realizada en 20163. En ella, se establece una clasificación de FP en tres grupos: fármacos antineoplásicos (grupo 1), fármacos no antineoplásicos que cumplen uno o más de los criterios establecidos por el NIOSH (grupo 2) y fármacos que pueden provocar alteraciones reproductivas en hombres y mujeres que están intentando concebir de manera activa, mujeres embarazadas o en periodo de lactancia activa (grupo 3).
La bibliografía muestra que la exposición laboral a algunos FP puede inducir la aparición de efectos adversos agudos4-6 o crónicos7-10, como erupciones, trastornos reproductivos7-14 o posibles alteraciones cromosómicas13. Establecer la relación causal directa entre la exposición a FP y el desarrollo de neoplasias resulta muy difícil debido al carácter multifactorial de ese tipo de procesos patológicos, a lo que hay que añadir la inexistencia de biomarcadores adecuados de tipo diagnóstico o pronóstico.
La presencia de contaminación por citostáticos en el entorno laboral sanitario ha sido demostrada en múltiples estudios15-24. Esto demuestra que la exposición laboral a FP es una realidad, y la probabilidad de contacto del personal sanitario con los mismos, si no se toman precauciones, alta.
Esta exposición puede darse cuando los FP producen aerosoles o generan polvo durante su manipulación y acondicionamiento, cuando se limpian líquidos derramados o cuando se tocan superficies contaminadas durante la preparación, administración o eliminación de los mismos2.
La concienciación de los profesionales sanitarios acerca de la exposición a FP en el entorno laboral y los riesgos que dicha exposición suponen desde el punto de vista de la seguridad laboral, se ha centrado de manera casi exclusiva en la manipulación de fármacos antineoplásicos.
Son múltiples las recomendaciones que, a nivel nacional e internacional, han sido desarrolladas por la comunidad científica para aumentar la protección de los profesionales que se ven expuestos a FP en su entorno laboral2,25-33.
El Instituto Nacional de Seguridad e Higiene en el Trabajo español (INSHT) ha publicado una Nota Técnica de Prevención 1.051 (NTP1051)29, en la que se establece que una de las fuentes de la contaminación de superficies de trabajo proviene de la generación de aerosoles durante el proceso de acondicionamiento de antineoplásicos para su posterior administración. Para disminuir dicha contaminación recomienda la utilización de sistemas cerrados y robots en la fase de preparación. Incluye también los requisitos que debe cumplir cualquier dispositivo para considerarse cerrado.
A su vez, el INSHT ha publicado un listado de FP disponibles en el mercado español. Este listado se acompaña de una serie de medidas de protección que el profesional sanitario debe seguir en función del tipo de manipulación que lleve a cabo.
En el Hospital Universitario y Politécnico La Fe (HUP La Fe), los fármacos citostáticos (grupo 1) se preparan de manera centralizada en el Servicio de Farmacia desde hace más de 20 años. Sin embargo, otros FP del grupo 2 y 3 se preparaban y administraban en las Unidades de Hospitalización (UH) sin medidas específicas de protección. El grado de concienciación acerca del riesgo de exposición a otros FP en determinadas unidades de hospitalización (UH) obligó al Servicio de Farmacia a liderar las acciones a desarrollar para establecer un circuito seguro en el uso de FP en todo el hospital.
El objetivo de este artículo es presentar las acciones desarrolladas para la mejora de la gestión integral de FP en el HUP La Fe.
Metodología
Estudio descriptivo en el que se explican las acciones llevadas a cabo por el SF del HUP La Fe para la mejora en la gestión integral de FP. El ámbito de aplicación de las acciones propuestas fue la totalidad de las UH del HUP La Fe, si bien existieron acciones específicas desarrolladas de manera exclusiva en el propio SF.
Las acciones desarrolladas pueden clasificarse en función de la índole de aplicación y de los objetivos que persiguen en:
a) Establecimiento de un listado de FP propio del centro.
b) Mejora de la seguridad en la manipulación de FP.
- En las medidas de protección colectiva: este tipo de medidas son de tipo estructural y de dotación de nuevas instalaciones e infraestructuras.
- En las medidas de protección individual.
c) Normalización de los procedimientos de trabajo y los circuitos de gestión de FP.
d) Formación e información.
Resultados
Las acciones que se desarrollaron en este periodo se recogen a continuación.
Establecimiento de un listado de FP propio del centro
Se consensuó un listado de FP para administración por vía parenteral o vía oral que requerían adecuación para la administración o reconstitución (Tablas 1 y 2) y que se elaborarían de manera centralizada en el SF. Este listado se elaboró de acuerdo con la lista del NIOSH actualizada en 20163 y el listado de FP publicado por el INSHT ese mismo año31.
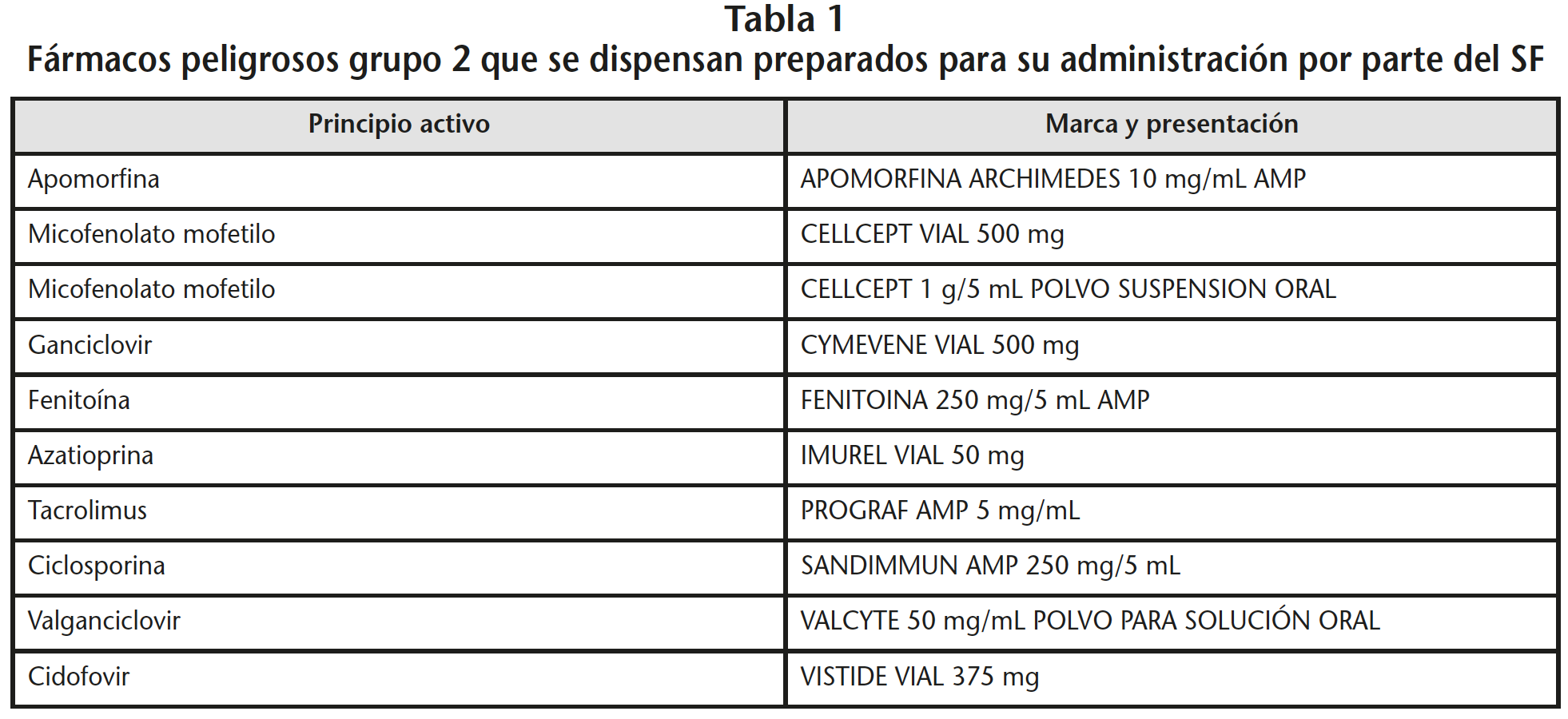
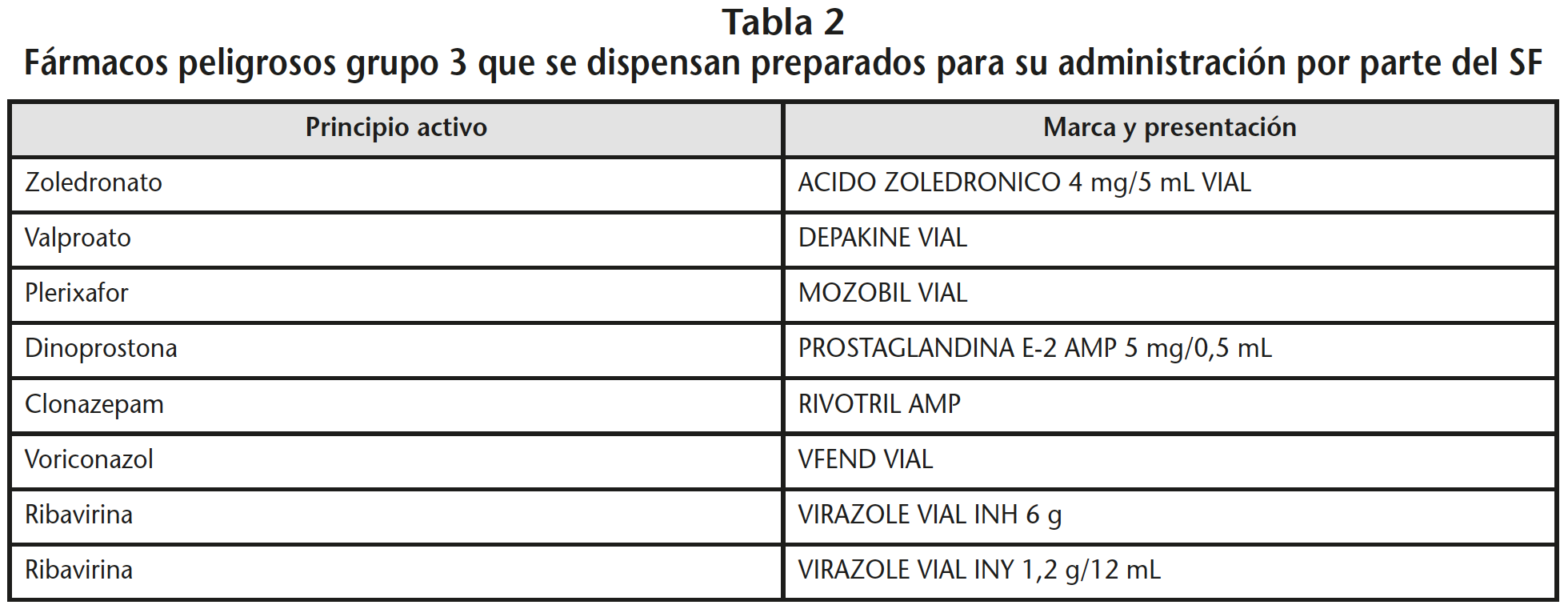
Se eliminaron las especialidades que se administraban por vía oral y que no requirieran reconstitución, y aquellas para administración tópica o nasal. Se actualizó y colgó en la intranet del hospital una “Guía segura para la administración de medicamentos por sondas digestivas” en la que se describían los procedimientos para la administración por sonda de cada uno de los fármacos orales de la Guía Farmacoterapéutica del centro, señalando los FP y haciendo notar que en caso de necesitar manipular alguno de ellos se contactara con el SF.
Se excluyó de la elaboración centralizada en el SF la oxitocina (grupo 3), que debido a su elevado consumo y al uso exclusivo en los paritorios, podía manipularse en la UH siempre que se establecieran medidas organizativas para excluir de su manipulación a profesionales susceptibles.
Asimismo, se excluyeron aquellos FP con presentaciones listas para la administración (jeringa precargada, bolsa de infusión o forma oral que no requiriera manipulación previa, implante subcutáneo, etc.).
En función de a qué grupo pertenecía el principio activo, se establecían una serie de acciones relacionadas con su manipulación.
En los casos específicos de la fenitoína y el clonazepam para administración parenteral, que debido a su escasa estabilidad en vehículos de administración intravenosa resultaban inadecuados para su elaboración y manipulación centralizada, se solventó mediante la dispensación de ambos en jeringas precargadas. Estas jeringas están listas para diluir en fluidos intravenosos in situ mediante el uso de sistemas cerrados de transferencia de fármacos o para su administración intravenosa directa. La ausencia de datos de estabilidad obligó al SF a desarrollar un estudio basado en matriz de riesgos para asignar fecha de caducidad a dichos preparados.
Para especialidades orales líquidas de FP que requirieran reconstitución previa a la administración y cuya estabilidad fuera larga (ejem: valganciclovir o micofenolato de mofetilo), dicha acción se llevaría a cabo en el SF, dispensándose la solución o suspensión lista para la administración a partir de un stock previamente elaborado.
Se consensuó con todas las partes que el listado de medicamentos considerados peligrosos en el centro se revisaría de manera periódica de acuerdo con las sucesivas actualizaciones de evidencia científica disponible. Este listado sería de aplicación en todo el HUP La Fe.
Mejora de seguridad en la manipulación de FP
a) Mejora de las medidas de protección colectiva en el SF:
Las instalaciones del área de elaboración del SF disponen de una superficie total de 406 m2, estando asignados 140 m2 a la manipulación de FP de manera exclusiva. Se distribuyen en una presala (grado C) y cuatro salas (grado B) dotadas cada una de ellas con 2 cabinas de seguridad biológica clase II. De las 8 cabinas de seguridad biológica, 4 se utilizan para el acondicionamiento de citostáticos, 2 se habilitaron para el acondicionamiento de FP no citostáticos, otra para la elaboración de fórmulas magistrales (FM) no estériles de FP y otra para la manipulación de hemoderivados (colirios de suero autólogo).
Las condiciones ambientales de cada sala cumplen con las normas GMP (Good Manufacturing Practices). Las salas están dotadas de filtros de alta eficacia (HEPA), que aseguran los niveles adecuados de partículas en aire y evitan la contaminación del medio ambiente, y de un sistema de esclusas que permite establecer presiones parciales negativas respecto a las áreas colindantes (10-15 Pa).
Asimismo se monitoriza de manera continua e independiente la temperatura, la humedad, la presión relativa de aire respecto al resto de salas y el número de partículas, alertando al personal elaborador de cualquier desvío respecto a las condiciones ideales de trabajo, y verificándose de manera periódica el grado de contaminación microbiológica.
Además, las instalaciones disponen de las medidas de seguridad en lo que a evacuación de aire contaminado o derrames, salidas de emergencia y actuación ante incendios se refiere.
El acceso del personal está controlado mediante tarjeta identificativa. En estas salas, la elaboración se desarrolla según técnica aséptica y el personal elaborador está dotado del equipo de protección individual (EPI) adecuado.
A los EPI disponibles se añadió la adquisición de sistemas cerrados de transferencia para la manipulación de FP. Para confirmar la eficacia de los mismos, se desarrolló un estudio de utilización, en el que se cuantificaron los niveles de contaminación por FP en las superficies de trabajo del área antes y después de su implementación. Las cuantificaciones fueron llevadas a cabo por un laboratorio independiente, y demostraron una reducción significativa de los niveles de contaminación (resultados pendientes de publicación).
Desde el punto de vista del almacenamiento, los FP se almacenan en ubicación separada del resto de fármacos y productos. A su vez, existe una nevera de uso exclusivo para el almacenamiento de FP. El flujo de FP y de preparaciones de FP se lleva a cabo a través de sistemas de esclusas de uso exclusivo, de la misma forma que la distribución a las UH se hace mediante un carro específico y nunca utilizando el sistema de tubo neumático.
La disponibilidad de estas instalaciones y sistemas de distribución, posibilitan la existencia de un “circuito cerrado” de gestión de FP paralelo al del resto de medicación, pero que asegura la seguridad de los profesionales que entran en contacto con estas sustancias.
b) Mejora de las medidas de protección colectiva en las UH:
Se dotó a todas las UH con sistemas de árbol para la administración. Estos sistemas disponen de punzón para conectar una solución de mantenimiento y lavado y varias conexiones valvulares en “Y” donde se insertan las preparaciones. Las preparaciones elaboradas en el SF se dispensan con una línea “purgada” con vehículo disolvente. De esta manera, la conexión al sistema de administración es segura y la posterior eliminación en bloque sin desconexión tras la administración, evita el riesgo de exposición del personal administrador.
Se dotó de dispositivos cerrados de transferencia de fármacos para la manipulación de FP con presentación en viales a todas las UH. Este tipo de manipulación sólo sería precisa en caso de necesidad de administración de una dosis urgente o si, por cuestiones de estabilidad, no se pudiera llevar a cabo la preparación de manera centralizada en el SF.
Se dotó de contenedores específicos para FP y sus residuos en todas las UH, informándose de la necesidad de gestión especial de este tipo de sustancias.
c) Mejora de las medidas de protección individual en todas las UH:
EPI completos: se revisó el contenido y la disponibilidad de los EPI en las UH. Uso de bata larga o traje desechable de polipropileno o cubierto con polietileno, cerrado en el cuello, de manga larga con puños elásticos, impermeables en la parte frontal y mangas y estériles, calzas de uso exclusivo, mascarillas tipo FPP2 o FPP3, gafas de seguridad si hay riesgo de salpicaduras, doble guante estéril, sin talco, de látex, nitrilo o neopreno, si no se dispone de guantes específicos para la manipulación de citostáticos, y gorro28-30.
Kit de derrames: se revisó la dotación de los kits de derrames disponibles en las UH (talla plastificada, calzas de plástico, pinza Pean Kocher, empapador 40×60, gorro, gafas policarbonato, 2 pares de guantes nitrilo, bata impermeable, mascarilla FFP3, 2 bolsas plástico 25×3, recogedor y cepillo, arena absorbente 400 gr) referencia GEDEFO.
Acciones para la normalización de los procedimientos de trabajo y los circuitos de gestión de FP
Se crearon, consensuaron y aplicaron los siguientes Procedimientos Normalizados de Trabajo (PNT).
a) De aplicación en el SF:
PNT de limpieza de Salas Blancas: este procedimiento incluye las acciones de limpieza específicas y un protocolo semanal de descontaminación del área de elaboración de FP basado en la guía “Estándares de calidad de los Servicios de Farmacia Oncológica. (QuapoS 4)”27.
PNT de vestuario de Salas Blancas: este documento recoge la vestimenta específica para la manipulación de FP y el EPI a utilizar en función de las acciones a desarrollar.
PNT de elaboración de FM no estériles de FP: recoge los procedimientos generales para la manipulación de FP en la elaboración de FM, desde la localización de la elaboración, los EPI a utilizar, el utillaje necesario o la metodología de limpieza. Este protocolo incluye el fraccionamiento de FP para ajuste de dosis, que se lleva a cabo en CSB en el interior de las Salas Blancas y por personal dotado con el EPI adecuado.
PNT de elaboración y dispensación de antineoplásicos y fármacos relacionados: incluye todas las actividades relacionadas con el manejo de FP en el SF, desde la preparación de materiales de partida, la elaboración del preparado, la revisión del producto final y su dispensación, así como las validaciones pertinentes en cada paso del proceso y los responsables de cada una de las etapas.
PNT de gestión del circuito hospitalario de FP no oncológicos: este documento recoge las características especiales de gestión de cada una de las etapas del circuito farmacoterapéutico donde se manipulan FP no antineoplásicos. En él se incluyeron los cambios organizativos del SF necesarios para la centralización de la elaboración individualizada por paciente de este grupo de fármacos:
- Prescripción electrónica en los programas utilizados en el HUP La Fe: Prisma® para FP no antineoplásicos y Farmis-Oncofarm® para antineoplásicos y terapias relacionadas.
- Validación del tratamiento prescrito por el farmacéutico asignado al área clínica correspondiente o por el farmacéutico de guardia en función del horario.
- Impresión de hojas de elaboración y dispensación con las instrucciones necesarias para el personal elaborador o distribuidor.
- Horario de preparación y dispensación en el SF: cuatro turnos estandarizados (8:30, 13:00, 17:00 y 20:00) que permiten cubrir todos los rangos horarios habituales de administración establecidos.
- Especificaciones técnicas para la manipulación de FP concretos: ribavirina inhalada, clonazepam y fenitoína en jeringa precargada (elaboración por lotes), micofenolato de mofetilo y valganciclovir suspensión o solución oral (elaboración por lotes).
- Excepciones a la elaboración centralizada en el SF:
– BCG. Por problemas de estabilidad, se elaboraría en la UH de Urología, en una ubicación controlada, con el EPI necesario y el uso de sistemas cerrados de transferencia de fármacos.
– Oxitocina. Por su uso localizado en paritorios, se establecieron medidas de tipo organizativo para evitar la exposición de profesionales embarazadas, en proceso de concepción activa o en lactancia activa.
– Primeras dosis urgentes de determinados FP (ácido valproico).
- Metodología para la validación técnica de las preparaciones.
- Consideraciones para la preparación de primeras dosis urgentes de determinados FP en las UH.
- Imputación de costos a las respectivas UH.
Creación de un circuito alternativo e independiente para reenvasado de FP: los FP que requieran de un proceso de reenvasado para su dispensación en dosis unitarias serán acondicionados en una reenvasadora manual de uso exclusivo y por personal dotado de las EPI necesarias.
Creación de una zona específica de almacenaje de FP en las diferentes secciones del SF: los FP se almacenan de manera separada al resto de medicación en las diferentes secciones del SF: almacén general, Salas Blancas, unidosis.
b) De aplicación en el resto de las UH del HUP La Fe:
PNT de manipulación de FP: describe el procedimiento sistemático de manipulación de FP, con objeto de garantizar tanto la calidad del producto, como la seguridad del paciente y la del manipulador y minimizar la contaminación ambiental. Este PNT es de aplicación en todas aquellas circunstancias en las que sea necesario preparar dosis de FP fuera de las instalaciones del SF:
- Se adaptó la terminología al nuevo conocimiento disponible.
- Se actualizó el alcance del PNT, ya que sólo sería de aplicación en aquellas circunstancias en las que fuera necesario preparar dosis de medicamentos de FP fuera de las instalaciones del SF, como puede ocurrir con las primeras dosis de antiepilépticos, o cuando la forma farmacéutica ya está preparada para su administración al paciente, no requiriéndose manipulación adicional alguna.
- Se revisaron las recomendaciones de manipulación, incluyéndose indicaciones acerca de la administración de formas orales líquidas y restringiéndose las actividades de trituración de comprimidos y apertura de cápsulas al SF.
PNT de actuación ante derrames de FP y exposiciones agudas: describe los pasos a seguir en caso de producirse un derrame o exposición aguda de FP, así como el contenido del kit de derrames. Este kit y cómo manejarlo, debe estar disponible y ser conocida su ubicación en todas las UH donde se manipulan FP, en los lugares de almacenamiento y estar a disposición del personal distribuidor de este tipo de fármacos.
c) De aplicación a nivel de gestión central del HUP La Fe:
PNT de Circuito de las actuaciones relacionadas con la actualización de los medicamentos peligrosos en los sistemas de información: Este documento recoge los procedimientos de actualización de bases de datos de programas de prescripción e información en la intranet del HUP La Fe cuando se incluye un nuevo FP en la Guía Farmacoterapéutica del Hospital. El circuito incluye la difusión de la información al personal no sanitario que pueda entrar en contacto con los FP a lo largo de su vida útil en el hospital. En él se recogen los mensajes estándares que mostrarán los programas de prescripción electrónica al personal sanitario en función del grupo al que pertenezca el FP incluido y las manipulaciones que requiera.
Adaptación de recursos informativos a disposición de la totalidad del personal sanitario y no sanitario del HUP La Fe:
- Revisión de la Guía para administración segura de medicamentos por sondas digestivas: como ya se ha adelantado, en ella se recomienda contactar con el SF en caso de no existir una especialidad lista para la administración y de ser necesaria la adecuación para la administración por sonda nasogástrica del FP. En el caso de FP del grupo 3, se recomendaba evitar la manipulación del mismo por parte de personal susceptible.
- Para FM no estériles elaboradas a partir de FP: todas aquellas pertenecientes al grupo 1 y 2 se elaborarían de manera centralizada en el SF. Para aquellas elaboradas a partir de FP del grupo 3, se incluyó información específica en el etiquetado para evitar su manipulación por parte de personal susceptible. Asimismo, el etiquetado de las FM elaboradas a partir de principios activos de los grupos 1 y 2 se modificó para que incluyera la advertencia “fármaco peligroso, manejar con EPI adecuado”. El SF dispone de un aplicativo informático de manufactura propia, Druida®, para la gestión integral de FM estériles y no estériles. Se llevó a cabo una adaptación del mismo para la inclusión de la información relativa a la manipulación de FP en todas las guías de elaboración y etiquetas que lo requirieran. Esta modificación permite al personal elaborador conocer qué materias primas y FM requieren del uso de EPI para su elaboración y de su manipulación en cabina de seguridad biológica.
Acciones formativas e informativas
En el SF se desarrollaron dos sesiones formativas para la totalidad del personal de enfermería y auxiliares, en las que se informó del nuevo circuito y de las medidas de protección y EPI necesarios para la manipulación de FP.
Se crearon documentos de acogida, de manera que cualquier trabajador que desarrolla su actividad en estas nuevas instalaciones requiere de una formación previa que asegura el cumplimiento de las normas de correcta elaboración (protocolos de vestimenta, de limpieza del área y acondicionamiento de la zona de trabajo, procedimientos de elaboración siguiendo técnica aséptica, actuación ante derrames, etc.). Dichos documentos son proporcionados al nuevo personal por la supervisión responsable del área, que registra la confirmación de lectura por parte del personal implicado.
A nivel de UH, de manera periódica y en colaboración con el Servicio de Prevención de Riesgos, se llevan a cabo sesiones formativas para todos los profesionales de enfermería y auxiliares de enfermería de las UH donde se manejan FP.
El temario desarrollado incluye la formación en riesgos y medidas preventivas en la manipulación de FP: valoración de la peligrosidad de FP, medidas de prevención para evitar la exposición laboral, situaciones especiales (especial sensibilidad, maternidad, lactancia), actuación en caso de exposición accidental, procedimiento de manipulación, vías de administración, etc.
Estas sesiones se complementan con dos talleres que se realizan simultáneamente bajo la supervisión y coordinación de las supervisoras de enfermería del SF: taller sobre FP para enfermeras y taller sobre FP para auxiliares de enfermería.
Asimismo, en dichas reuniones formativas se entrega al personal asistente un dosier con documentación: listado de FP de los grupos 2 y 3 que se elaboran de manera centralizada en el SF; EPI: elementos y códigos de solicitud al almacén general; ficha informativa sobre la manipulación de FP; PNT de manipulación de FP en las UH; PNT de actuación ante derrames de FP y exposiciones agudas junto con el póster de actuación ante dichos derrames del grupo GEDEFO de la Sociedad Española de Farmacia Hospitalaria.
Estos talleres han sido impartidos a más de 1.000 profesionales sanitarios, aumentando la concienciación y buenas prácticas relacionadas con el manejo de FP en el HUP La Fe.
Asimismo, se llevaron a cabo sesiones formativas para informar al personal no sanitario que pudiera entrar en contacto con FP a lo largo de su vida útil en el hospital, de las medidas de protección y de actuación ante derrames que deberían llevar a cabo.
Discusión
Desde el punto de vista de la seguridad de los profesionales, sanitarios o no, la manipulación de sustancias con efectos carcinógenos o mutágenos ha sido fruto de atención por parte de las autoridades gubernamentales nacionales29,31, europeas34 e internacionales30. El desarrollo de legislación específica, que por otra parte es de obligado cumplimiento, y recomendaciones técnicas29-31 al respecto así lo demuestra.
La aplicación de las correctas medidas de protección a la hora de manipular FP en el entorno sanitario, ha quedado relegada en muchos casos por cuestiones económicas o de falta de concienciación. Sin embargo, de un tiempo a esta parte, numerosas sociedades científicas, organizaciones sindicales y de pacientes han centrado sus esfuerzos en hacer visible esta circunstancia32.
La adecuación de las condiciones de trabajo resulta imprescindible para asegurar el máximo grado de seguridad laboral alcanzable en el entorno sanitario. En el HUP La Fe se abordó la tarea de maximizar la adecuación de las condiciones laborales a las recomendaciones existentes al respecto. Las decisiones tomadas fueron consensuadas por parte de los principales agentes implicados.
Desde este punto de vista, el SF del HUP La Fe ha intentado establecer una concordancia entre las recomendaciones y legislación y las medidas desarrolladas:
- La dotación con dispositivos cerrados de transferencia de fármacos a todas las UH cumple con lo establecido en las recomendaciones.
- La limitación de las cantidades de un agente carcinógeno o mutágeno en el lugar de trabajo se asegura mediante una correcta gestión de stocks, que eviten, en la medida de lo posible, la acumulación de FP en las zonas de almacenamiento.
- La limitación, al nivel más bajo posible, del número de trabajadores expuestos o que puedan estarlo se asegura mediante el control del acceso a las zonas de elaboración de FP que, en el caso del SF del HUP La Fe, se realiza mediante tarjeta identificativa.
- La aplicación de procedimientos y métodos de trabajo apropiados, se consigue mediante la creación y seguimiento de los PNT correspondientes referentes a la gestión y manipulación de FP en el SF y en las UH.
- La evacuación de los agentes carcinógenos o mutágenos en origen y la aspiración local o ventilación general adecuadas se realiza gracias a la dotación tecnológica del área de elaboración de FP (filtros HEPA, sistemas extractores, etc.). Estas instalaciones también permiten delimitar las zonas de riesgo, y están dotadas de señales adecuadas de aviso y de seguridad.
- La disponibilidad de instalaciones dotadas con cabinas de seguridad biológica clase II constituye la medida de protección colectiva recomendada por todas las guías nacionales e internacionales de manipulación de FP. A esto hay que añadir la dotación con EPI apropiados a todas las UH y al SF, lo que asegura la disponibilidad de las medidas individuales de protección mencionadas.
- Las medidas higiénicas, en particular la limpieza regular de suelos, paredes y demás superficies se encuentra protocolizada y consensuada con la empresa de limpieza del hospital.
- Las labores de información a los trabajadores se desarrollaron en colaboración con el servicio de Medicina Preventiva del HUP La Fe.
- En caso de que se produzcan vertidos, todas las UH y el SF están dotados de kits de derrames, que disponen de todo el material necesario para contener y limpiar el vertido de FP.
- Asimismo, se dispone de medios para la seguridad en la recogida, almacenamiento y eliminación de residuos, constituidos por contenedores específicos para FP, que siguen un circuito de recogida y eliminación separado del resto de residuos sanitarios y no sanitarios generados en el HUP La Fe.
- Para el almacenamiento, manejo y transporte seguros, se dispone de recipientes herméticos y etiquetados de manera clara, inequívoca y visible.
En principio, con estas medidas se cubrirían todas las disposiciones dirigidas a evitar o reducir la exposición, salvo la referente a la utilización de métodos de medición adecuados para agentes carcinógenos o mutágenos, en particular para la detección precoz de exposiciones anormales debidas a imprevistos o accidentes. Actualmente, no se llevan a cabo mediciones periódicas de los niveles de contaminación por FP en las zonas de manipulación o administración de los mismos. Este aspecto debe valorarse y normalizarse, ya que el conocimiento de la situación permitiría instaurar las medidas necesarias para minimizar la contaminación.
La gestión de FP puede resultar abrumadora si se intenta abordar de manera integral sin la colaboración del servicio de Medicina Preventiva y sin el apoyo de la Dirección del centro. Sin embargo, el consenso con las partes implicadas y la voluntad de mejorar la seguridad global del centro, son fuerzas impulsoras que permiten alcanzar el objetivo final de mejora de las condiciones laborales de todo el personal potencialmente expuesto a FP.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
Bibliografía
- American Society of Hospital Pharmacists. ASHP technical assistance bulletin on handling cytotoxic and hazardous drugs. Am J Hosp Pharm. 1990;47:1033-49.
- Burroughs G, Connor T, McDiarmid M. NIOSH Alert: preventing occupational exposures to antineoplastic and other hazardous drugs in health care settings. DHHS (NIOSH) Publ No. 2004-165.
- NIOSH [2016]. NIOSH list of antineoplastic and other hazardous drugs in healthcare settings, 2016. By Connor TH, MacKenzie BA, DeBord DG, Trout DB, O’Callaghan JP. Cincinnati, OH: U.S. Department of Health and Human Services, Centers for Disease Control and Prevention, National Institute for Occupational Safety and Health, DHHS (NIOSH) Publication Number 2016-161 (Supersedes 2014-138).
- Valanis BG, Vollmer WM, Labuhn KT, Glass AG. Association of antineoplastic drug handling with acute adverse effects in pharmacy personnel. Am J Hosp Pharm. 1993;50(3):455-62.
- McDiarmid M, Egan T. Acute occupational exposure to antineoplastic agents. J Occup Med. 1988;30(12):984-7.
- Krstev S, Perunicić B, Vidaković A. Work practice and some adverse health effects in nurses handling antineoplastic drugs. Med Lav. 2003;94(5):432-9.
- Selevan SG, Lindbohm ML, Hornung RW, Hemminki K. A study of occupational exposure to antineoplastic drugs and fetal loss in nurses. N Engl J Med. 1985;313(19): 1173-8.
- Stücker I, Caillard JF, Collin R, Gout M, Poyen D, Hémon D. Risk of spontaneous abortion among nurses handling antineoplastic drugs. Scand J Work Environ Health. 1990;16(2):102-7.
- Valanis B, Vollmer WM, Steele P. Occupational exposure to antineoplastic agents: self-reported miscarriages and stillbirths among nurses and pharmacists. J Occup Environ Med. 1999;41(8):632-8.
- Valanis B, Vollmer W, Labuhn K, Glass A. Occupational exposure to antineoplastic agents and self-reported infertility among nurses and pharmacists. J Occup Environ Med. 1997;39(6):574-80.
- Hemminki K, Ludlum DB. Covalent modification of DNA by antineoplastic agents. J Nat Cancer Inst. 1984;73(5):1021-8.
- Zielhuis G, Peelen SJ, Florack EI, Roeleveld N. Hospital work and fecundability. Scand J Work Environ Health. 1999;25 Suppl 1:47-8.
- McDiarmid MA, Oliver MS, Roth TS, Rogers B, Escalante C. Chromosome 5 and 7 abnormalities in oncology personnel handling anticancer drugs. J Occup Environ Med. 2010;52(10):1028-34.
- Connor TH, Lawson CC, Polovich M, McDiarmid MA. Reproductive health risks associated with occupational exposures to antineoplastic drugs in health care settings: a review of the evidence. J Occup Environ Med. 2014 Sep;56(9):901-10.
- Sessink P, Trahan J, Coyne J. Reduction in Surface Contamination With Cyclophosphamide in 30 US Hospital Pharmacies Following Implementation of a Closed-System Drug Transfer Device. Hosp Pharm. 2013; 48(3):204-12.
- Miyake T, Iwamoto T, Tanimura M, Okuda M. Impact of closed-system drug transfer device on exposure of environment and healthcare provider to cyclophosphamide in Japanese hospital. Springerplus. 2013;2(1):273.
- Connor TH, Sessink PJM, Harrison BR, Pretty JR, Peters BG, Alfaro RM, et al. Surface contamination of chemotherapy drug vials and evaluation of new vial-cleaning techniques: Results of three studies. Am J Health Pharm. 2005;62(5):475-84.
- Spivey S, Connor TH. Determining Sources of Workplace Contamination with Antineoplastic Drugs and Comparing Conventional IV Drug Preparation with a Closed System. Hosp Pharm. 2003;38(2):135-9.
- Nyman H A, Jorgenson JA, Slawson MH. Workplace Contamination with Antineoplastic Agents in a New Cancer Hospital Using a Closed-System Drug Transfer Device. Hosp Pharm. 2010;42(3):219-25.
- Contractor S, Kumar A, Phillip M, Patel D, Karcich J, Kisza P. Use of PhaSeal Transfer System during Chemoembolization to Prevent Unintentional Leakage of Chemotherapeutic Agents during Preparation and Delivery. J Vasc Interv Radiol. 2015;26(1):137-9.
- Siderov J, Kirsa S, McLauchlan R. Reducing workplace cytotoxic surface contamination using a closed-system drug transfer device. J Oncol Pharm Pract. 2010; 16(1):19-25.
- Sessink PJM, Connor TH, Jorgenson JA, Tyler TG. Reduction in surface contamination with antineoplastic drugs in 22 hospital pharmacies in the US following implementation of a closed-system drug transfer device. J Oncol Pharm Pract. 2011;17(1):39-48.
- Fleury-Souverain S, Mattiuzzo M, Mehl F, Nussbaumer S, Bouchoud L, Falaschi L et al. Evaluation of chemical contamination of surfaces during the preparation of chemotherapies in 24 hospital pharmacies. Eur J Hosp Pharm. 2015;22:333-341.
- González Álvarez A, López-Montenegro Soria MA, Albert Marí A, Martínez Gómez MA, Porta Oltra B, Jiménez Torres NV. Exposición a fármacos citotóxicos en el personal sanitario. Farm Hosp. 2012;36(5):368-73.
- Easty AC, Coakley N, Cheng R, Cividino M, Savage P, Tozer R, et al. Safe handling of cytotoxics: guideline recommendations. Curr Oncol. 2015;22(1):e27-37.
- ISOPP standards of practice. Safe handling of cytotoxics. J Oncol Pharm Pract. 2007;13Suppl:1-81.
- Estándares de calidad de los Servicios de Farmacia Oncológica. (QuapoS 4). Disponible en: http://www. esop.li/downloads/library/quapos4_english.pdf. Acceso: Agosto 2015.
- Guía de Buenas Prácticas para Trabajadores Profesionalmente Expuestos a Agentes Citostáticos. Asociación Madrileña de Medicina del Trabajo en el ámbito Sanitario (AMMTAS).Escuela Nacional de Medicina del Trabajo. Instituto de Salud Carlos III. Madrid, 2014. Disponible en: http://gesdoc.isciii.es/gesdoccontroller?action=download&id=26/03/2014-199edf956b.
- Instituto Nacional de Seguridad e higiene en el Trabajo. NTP 1.051: Exposición laboral a compuestos citostáticos: sistemas seguros para su preparación. 2015. Disponible en: http://www.insht.es/InshtWeb/Contenidos/Documentacion/NTP/NTP/Ficheros/1043a1054/ntp-1051w.pdf. Acceso: Diciembre 2015.
- USP 800. Hazardous Drugs-Handling in Healthcare Settings. Mayo 2015. Disponible en: http://www.usp. org/sites/default/files/usp_pdf/EN/m7808_pre-post.pdf. Acceso: Diciembre 2015.
- Medicamentos peligrosos. Medidas de prevención para su preparación y administración. Instituto Nacional de Seguridad e Higiene en el Trabajo (INSHT). Acceso septiembre 2017: http://www.insht.es/InshtWeb/ Contenidos/Documentacion/FICHAS%20DE%20PUBLICACIONES/EN%20CATALOGO/Higiene/2016% 20medicamentos%20peligrosos/Medicamentos%20peligrosos.pdf.
- Documento de consenso: Seguridad del paciente y del profesional sanitario en la preparación y administración de medicinas peligrosas. Enero 2015. Disponible en: http://panelfenin.es/uploads/noticias/pdf_noticia_315.pdf. Acceso: Diciembre 2015.
- Gaspar Carreño M, Achau Muñoz R, Torrico Martín F, et al. Safe procedure development to manage hazardous drugs in the workplace. Farm Hosp. 2017 Mar 1;41(2):222-256.
- DIRECTIVA 90/394/CEE, de 28 de junio, relativa a la protección de los trabajadores contra los riesgos relacionados con la exposición a agentes cancerígenos durante el trabajo.
____
Descargar artículo en PDF: Implementación de un circuito seguro para la gestión integral de fármacos peligrosos en un hospital de tercer nivel
