Rev. OFIL 2017, 27;3:264-271
Fecha de recepción: 01/07/2016 – Fecha de aceptación: 27/09/2016
Gallego Úbeda M1, Delgado Téllez de Cepeda L1, Campos Fernández de Sevilla MA1, Egües Lugea A1,
Iglesias Peinado I2, Tutau Gómez F1
1 Hospital Universitario del Henares. Coslada. Madrid (España)
2 Universidad Complutense de Madrid (España)
____
Correspondencia:
Marta Gallego Úbeda
Hospital del Henares
(Servicio de Farmacia)
Avda. Marie Curie, s/n
28822 Coslada (Madrid)
Correo electrónico: mgallegoubeda@hotmail.com
____
RESUMEN
Antecedentes: La complejidad de la utilización de medicamentos en pacientes con enfermedad renal, hace necesario desarrollar metodologías que permitan una atención eficiente evitando problemas relacionados con medicamentos (PRMs).
Objetivo: Describir las intervenciones farmacéuticas (IF), su evolución, y fármacos que requieren ajuste de dosis, en pacientes con insuficiencia renal (IR).
Métodos: Estudio retrospectivo en el que se aplicó una herramienta informática (SONAR) basada en el concepto interoperabilidad (capacidad sistemas informáticos para trabajar integrados).
SONAR se aplicó a tres periodos: P0: previo a implantar la herramienta, P1: inicio implantación, P2: un año después implantación.
Se realizó un análisis descriptivo de las variables sexo, edad, MDRD-4, pacientes susceptibles a presentar un PRM, pacientes con IF, número IF, grado de aceptación, distribución de IF por principio activo y sistema. Se aplicó el test estadístico Kruskal-Wallis considerándose como estadísticamente significativas las diferencias con una probabilidad inferior al 5% (p<0,05).
Resultados: Las IF se reducen del P1 (229) al P2 (96). El grado de aceptación se incrementa (P1 -47,6%- vs. P2 -77,1%-). Principio activo con mayor número IF: levofloxacino.
Las intervenciones afectaron a pacientes en cuyo diagnóstico se encontraba implicado principalmente el sistema cardiovascular.
Conclusiones: SONAR incrementa la eficiencia de detección de PRMs. Muestra un grado de aceptación de IF elevado. Genera efecto aprendizaje en profesionales sanitarios y confianza en IF. Además, genera recomendaciones consensuadas y bien documentadas. Es flexible y evita el exceso de alertas. Es implementada con facilidad con múltiples reglas o criterios.
Palabras clave: Insuficiencia renal, intervención farmacéutica, interoperabilidad, problema relacionado con la medicación, validación farmacéutica.
____
INTRODUCCIÓN
La enfermedad renal crónica (ERC) es un problema de salud pública relevante, asociada a una importante morbi-mortalidad cardiovascular y que influye de manera significativa en los costes. Se ha convertido en un problema sanitario, social y económico de primer orden para todos los sistemas sanitarios de los países desarrollados1.
Datos del año 2015, hacen referencia al notable incremento de la tasa de ERC durante los próximos 20 años viéndose afectados más de la mitad de los individuos con edades entre los 30-64 años. En EE.UU. se estima, que la población de más de 30 años con ERC alcanzará los 28 millones en 2020 y cerca de 38 millones en 20302.
Algunos autores destacan la importancia de desarrollar programas de detección precoz de enfermedad renal y cómo la atención farmacéutica (AF) en estos pacientes, mediante ajuste de dosis, aumento de intervalo posológico, etc. contribuye a evitar efectos nefrotóxicos de ciertos fármacos3.
Esto conjuntamente con la invitación del grupo TECNO de la SEFH (Sociedad Española de Farmacia Hospitalaria) a la reingeniería de procesos y a una búsqueda e introducción constante de mejoras e innovaciones en procesos ya establecidos de utilización y gestión del medicamento4,5, hace que sea necesario desarrollar nuevas metodologías que permitan la detección de problemas relacionados con la medicación (PRMs) o situación en la que el proceso de uso de medicamentos causa o puede causar la aparición de un resultado negativo asociado con la medicación6, y la realización de intervenciones farmacéuticas (IF) de manera sencilla y eficiente, solventando el problema actual de falta de recursos
Por lo tanto, el objetivo de este estudio es describir las IF y su evolución en pacientes con deterioro de la función renal y fármacos que requieren ajuste, mediante una herramienta informática diseñada para la ayuda a la toma de decisiones al farmacéutico en el proceso de validación farmacoterapéutica.
MATERIAL Y MÉTODOS
Tipo de estudio: retrospectivo en el que se aplicó una herramienta informática, diseñada por el Servicio de Farmacia y basada en el concepto interoperabilidad, en tres periodos diferentes y sobre pacientes con deterioro de la función renal que reciben fármacos que requieren ajuste en insuficiencia renal (IR).
Ámbito y duración del estudio: pacientes ingresados en unidades médico-quirúrgicas y urgencias.
Se aplicó la herramienta informática a lo largo de tres periodos entre octubre 2009 y febrero 2012:
– P0 o periodo previo a la implantación de la herramienta (octubre 2009–febrero 2010): la incorporación de la herramienta informática al proceso de validación comenzó en marzo 2010, por lo tanto el P0 es un periodo libre de actuación.
– P1 o de inicio de la implantación (octubre 2010-febrero 2011): puesta en marcha la herramienta.
– P2, un año después de la implantación (octubre 2011-febrero 2012): herramienta y metodología totalmente consolidadas.
Diseño de la herramienta informática: SONAR.
Se ha utilizado un nuevo método de validación farmacoterapéutica basado en el concepto de interoperabilidad (integración de la información de distintas aplicaciones informáticas) que permite el análisis de los PRMs de una manera eficiente. El Servicio de Farmacia diseñó una herramienta informática que se acuñó con el término SONAR (Sistema de Optimización de la farmacoterapia mediante la utilizacióN de señales AleRtantes) por la similitud conceptual con la tecnología Sónar (usa la propagación del sonido bajo el agua principalmente para, entre otros, hacer visible la orografía del fondo marino, así como para la detección de objetos sumergidos) con el proceso de hacer fácilmente visible toda la información de la historia clínica de los pacientes que puede afectar al resultado óptimo de la farmacoterapia, así como para la detección de PRMs en todos los pacientes hospitalizados.
Para la detección de PRMs, la herramienta SONAR permite:
1. Integrar todos los sistemas de información del hospital7,8 (Figura 1)
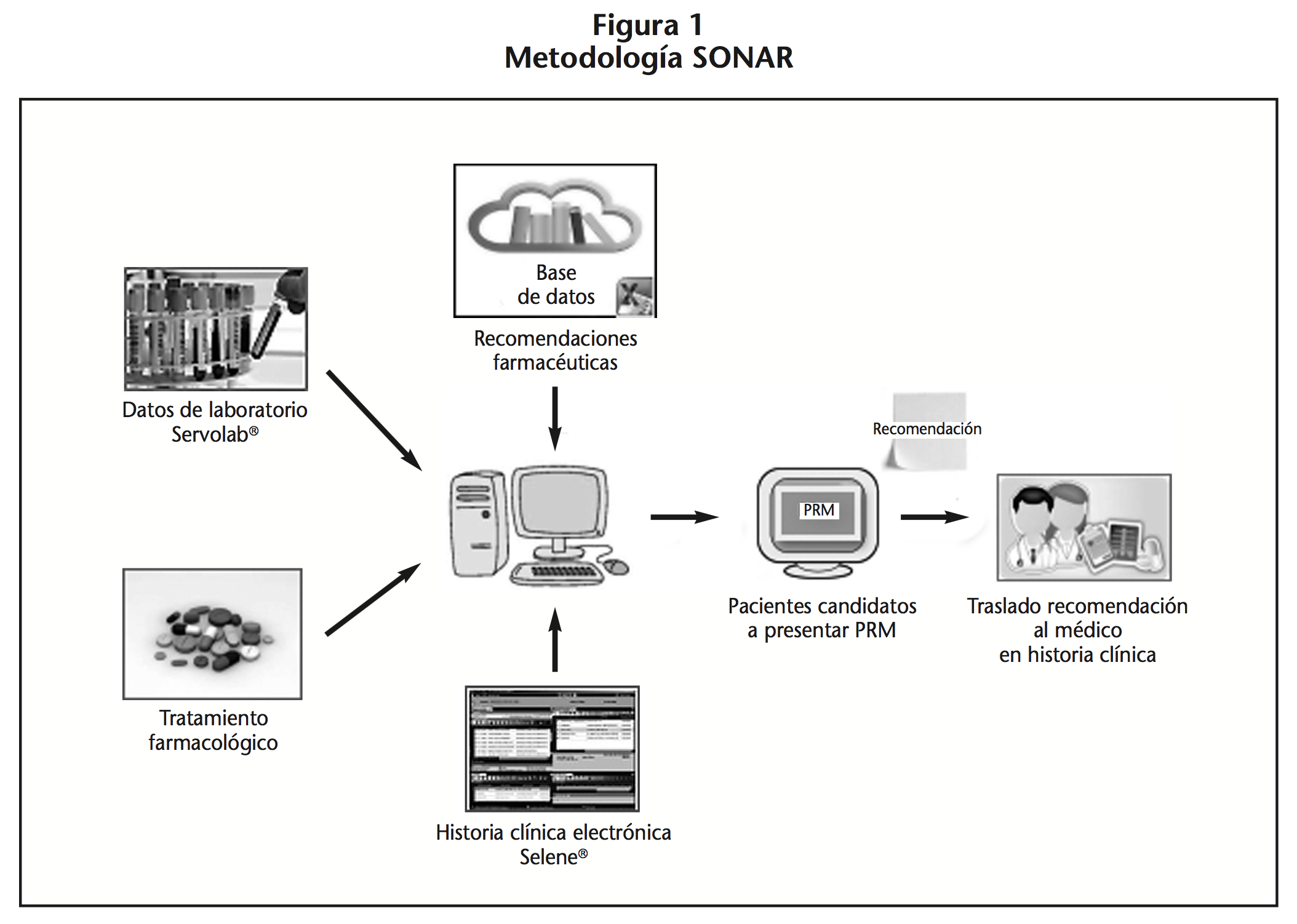
• Historia clínica electrónica: Selene®.
• Farmacoterapia del paciente: Farmatools®.
• Datos de laboratorio (datos analíticos): Servolab®.
• Bases de datos de recomendaciones farmacéuticas con principios activos incluidos en la guía farmacoterapéutica del hospital que requerían ajuste en situación de IR. Para su elaboración se consultaron diferentes fuentes bibliográficas como: ficha técnica, Drug Dex Micromedex®, UpToDate®, guías de práctica clínica y artículos relacionados.
2. La identificación automática, en base a unos criterios de selección previamente definidos, de pacientes candidatos a presentar un PRM junto con la información relevante para el caso. En una pantalla aparece toda la información clínica y farmacológica relevante de ayuda a la toma de decisiones farmacoterapéuticas en el proceso de validación: datos del paciente (número de historia clínica, nombre y apellidos), servicio y unidad de hospitalización, tratamiento farmacológico, datos analíticos, fármaco y recomendación. Con toda esta información, el farmacéutico realiza las IF que considere oportunas. (Figura 2). 3. Trasladar de manera sencilla a la historia clínica las recomendaciones al médico prescriptor.
3. Trasladar de manera sencilla a la historia clínica las recomendaciones al médico prescriptor.
4. Realizar un seguimiento de las IF y su clasificación según grado de aceptación.
5. Realizar IF precoces (en urgencias), que aseguren la continuidad asistencial.
6. Optimizar recursos humanos: validación de un gran número de pacientes en pocos minutos.
7. Que ningún paciente candidato a tener algún PRM definido en la aplicación quede sin revisar.
Selección de pacientes: pacientes hospitalizados, incluido el Servicio de Urgencias, con:
• FG <60 ml/min/1,73m2, expresado según la ecuación MDRD-4, con o sin ERC.
• Pacientes con fármacos prescritos que requieran ajuste/recomendación en IR.
Se excluyeron pacientes ingresados en UCI, por disponer de un programa de prescripción diferente de tal manera que los datos farmacoterapéuticos no pueden ser extraídos con facilidad.
Procedimiento: SONAR comenzó a implantarse en marzo 2010. Con objeto de obtener un periodo libre de actuación se decidió seleccionar el rango de fechas entre octubre 2009 y febrero 2010 (P0) y se aplicó de forma retrospectiva y simulada SONAR obteniéndose los pacientes que teóricamente hubieran sido candidatos a intervención. El farmacéutico valoró la necesidad de realizar la intervención teórica y seleccionó los principios activos que hubieran sido susceptibles de intervención. En el P0, puesto que la intervención fue teórica, todas las IF fueron clasificadas como rechazadas al no poderse evaluar el grado de aceptación.
En los P1 y P2 SONAR se encontraba implantada, las IF fueron reales y clasificadas como aceptadas o rechazadas por el médico.
Se realizó un análisis descriptivo según las variables recogidas: sexo, edad, MDRD-4, número de pacientes candidatos a IF, número de pacientes con IF, número de IF y grado de aceptación, distribución de las IF por principio activo y por sistema.
Para el análisis estadístico se empleó el test de Kruskal-Wallis considerándose como estadísticamente significativas las diferencias con una probabilidad inferior al 5% (p<0,05).
RESULTADOS
Los resultados se expresan por periodo de estudio (0,1 y 2).
Las características demográficas se muestran en la tabla 1.
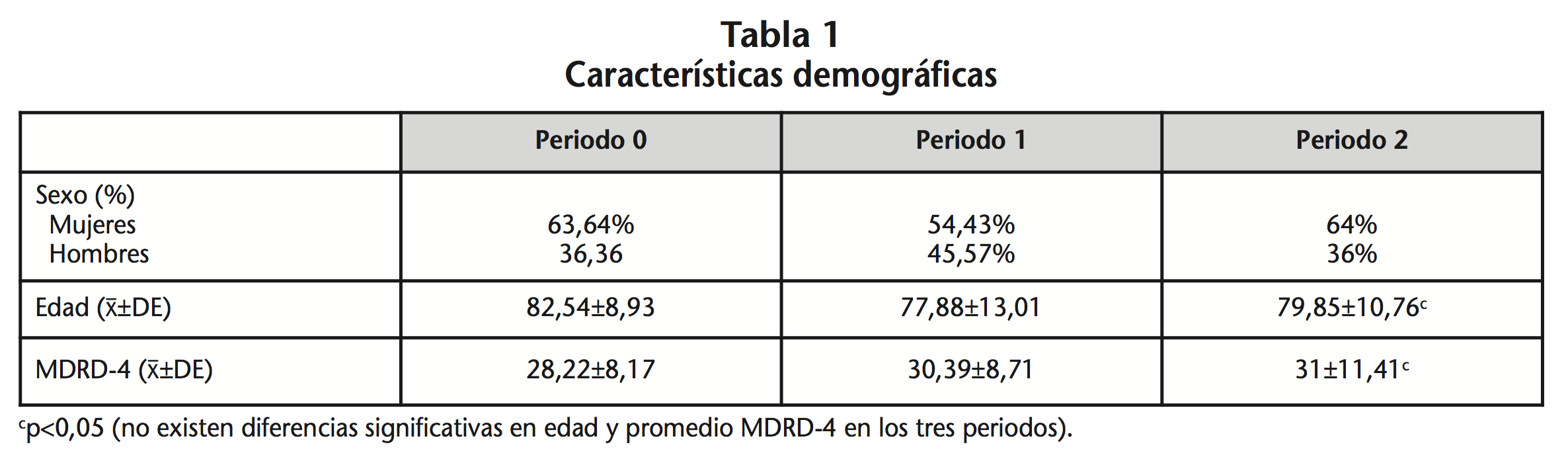
No existen diferencias significativas en edad y MDRD-4 entre los tres periodos por lo que se pueden considerar homogéneos.
Los datos descriptivos se muestran en la tabla 2.
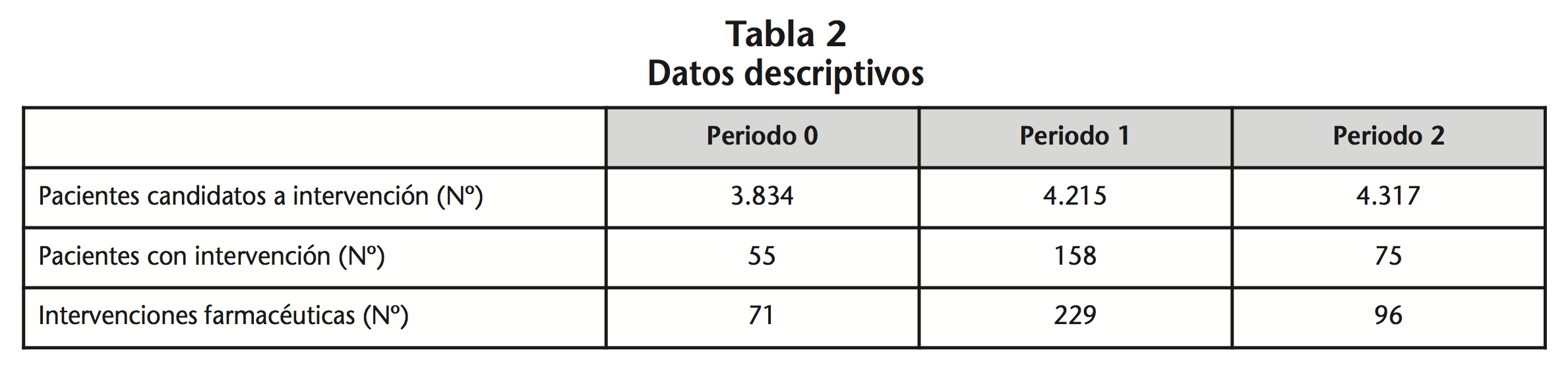
El número de pacientes candidatos a intervención fue 3.834, 4.215 y 4.317 en el P0, P1 y P2 respectivamente. Tanto el número de pacientes con IF y el número de IF es notablemente mayor en P1 respecto a P0 y P2.
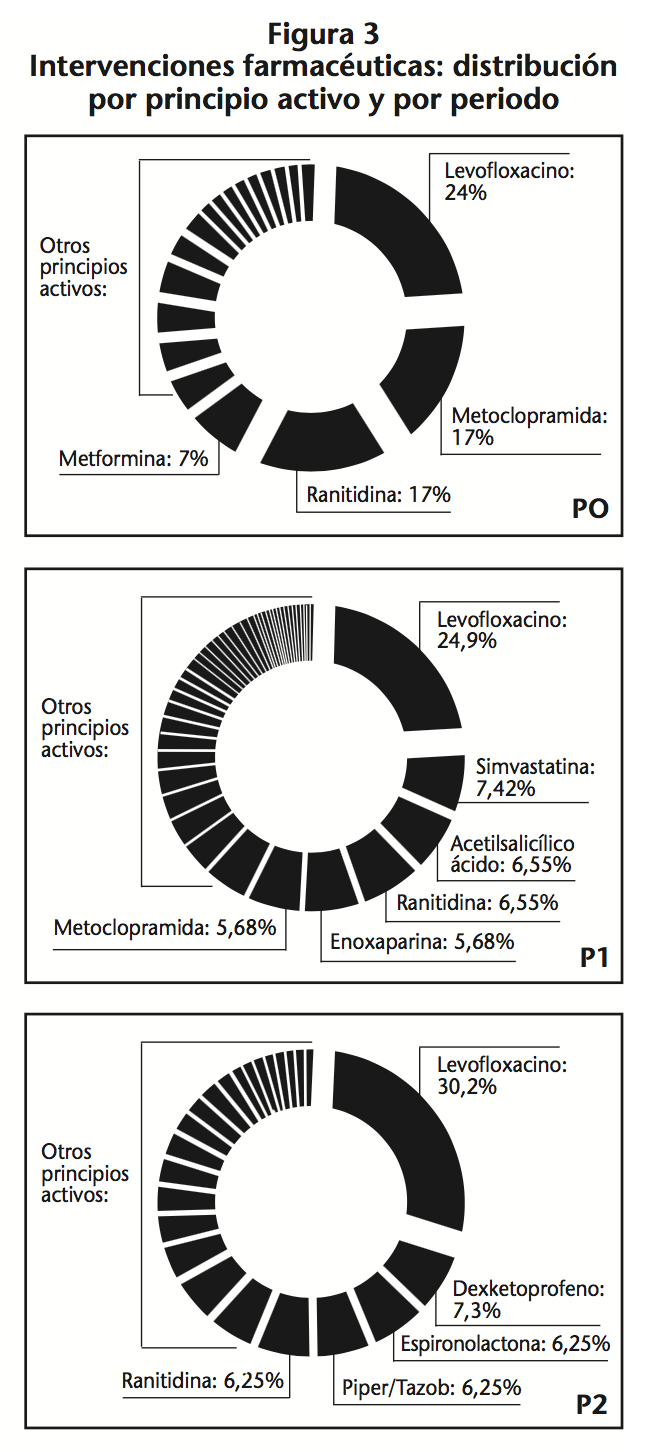
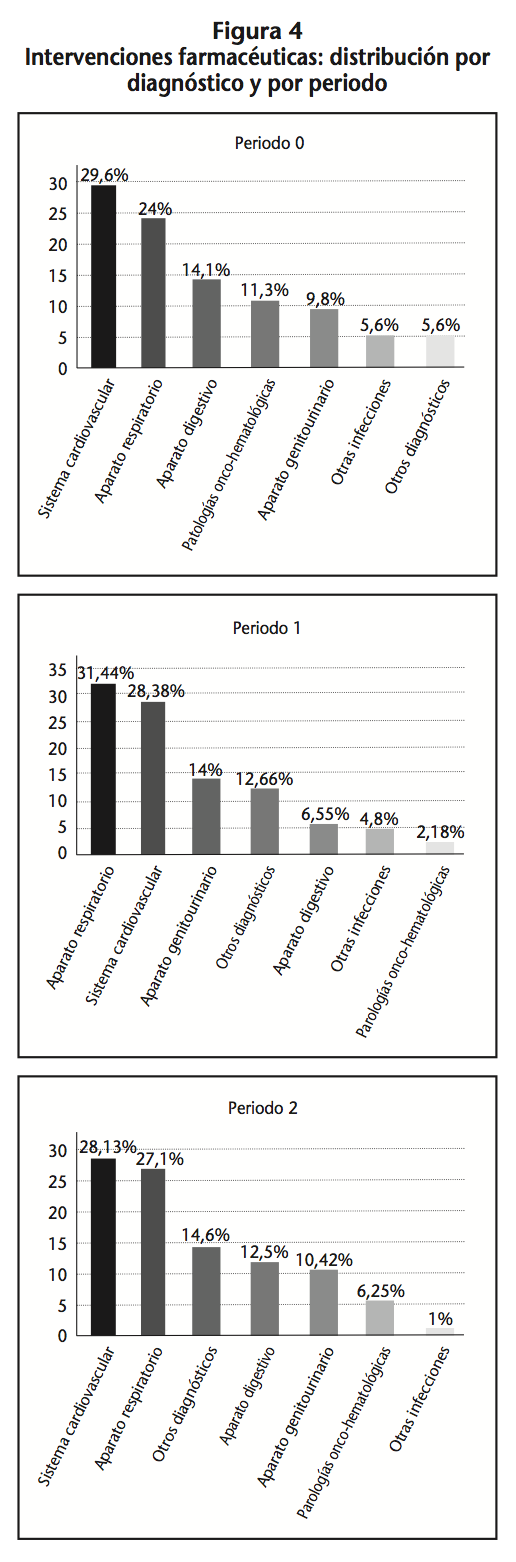
En las figuras 3 y 4 se puede observar la distribución de las intervenciones por principio activo y por sistema anatómico/diagnóstico. Levofloxacino es el principio activo donde se centra el mayor número de intervenciones y las intervenciones afectaron a pacientes en cuyo diagnóstico se encontraban implicados principalmente el sistema cardiovascular y aparato respiratorio.
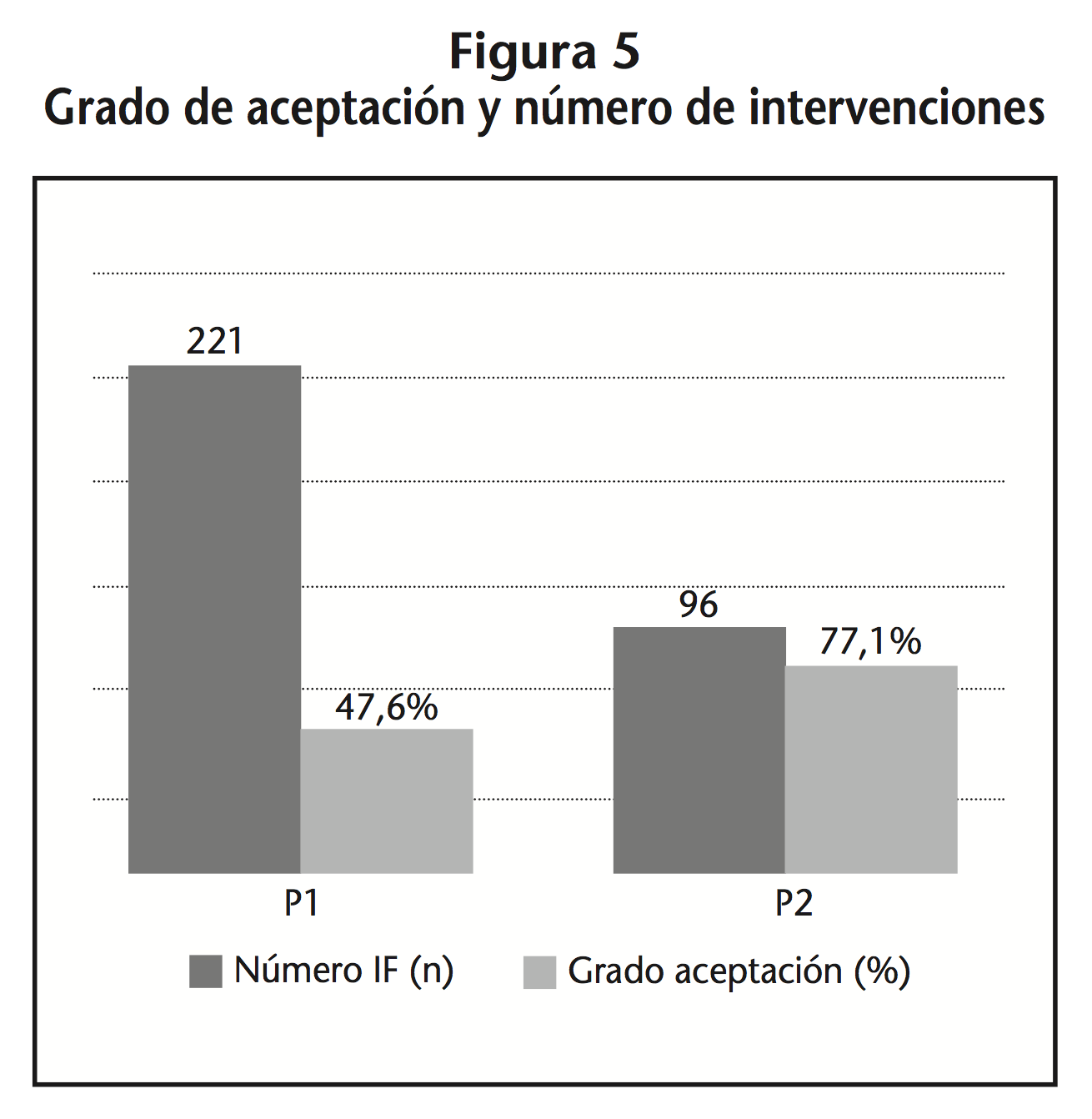
En cuanto al grado de aceptación de las IF, en el P0 todas las IF se consideraron rechazadas al ser teóricas. En el P1, de las 229 intervenciones realizadas el 47,6% (109) fueron intervenciones aceptadas mientras que el 52,4% (120) se clasificaron como rechazadas. En el P2, de las 96 intervenciones realizadas el 77,1% (74) fueron intervenciones aceptadas mientras que el 22,9% (22) se clasificaron como rechazadas.
La figura 5 muestra la evolución en el grado de aceptación y el número de intervenciones entre el periodo 1 y 2.
DISCUSIÓN
Los sistemas de soporte a la toma de decisiones clínicas son sistemas de ayuda a la toma de decisiones, en los que las características individuales de los pacientes se utilizan para generar recomendaciones que son presentadas a los clínicos para su consideración9. Se caracterizan como ágiles, útiles, proporcionan información a tiempo real e integrada en los flujos de trabajo del usuario, proactivos ya que ofrecen una alternativa o cambio de orientación, permiten acceso a información adicional solo en caso requerido, permiten la monitorización del impacto y un feedback e información permanentemente actualizada9-11.
Apoyándonos no solo en estas consideraciones sino también en la necesidad de optimización de la farmacoterapia y mejora en la eficiencia de detección de PRMs se diseñó una nueva herramienta basada en el concepto de interoperabilidad que permitiese compensar la falta de recursos humanos incrementando la calidad de la AF. Gracias al concepto de interoperabilidad conseguimos explotar de manera coordinada y eficaz los diferentes sistemas informáticos del hospital obteniéndose beneficios indiscutibles y salvándose obstáculos tan importantes como el acceso a todos ellos por separado, con la consiguiente disminución del tiempo dedicado a la detección de PRMs y realización de IF.
Destacar que SONAR permite salvar además desventajas de los sistemas de soporte a la toma de decisiones, como la falta de flexibilidad y situaciones de “fatiga” derivada de exceso de información y que conlleva a un desinterés hacia las recomendaciones establecidas13. SONAR permite realizar modificaciones, en el mismo momento de detección del PRM, de la nota dirigida al médico lo que deriva en información personalizada. Por otro lado, permite modificar la base de datos con recomendaciones de una manera sencilla y rápida siendo su actualización continua.
El exceso de alertas se minimiza gracias a la selección que realiza el farmacéutico. SONAR presenta a los pacientes candidatos y el farmacéutico valora los principios activos susceptibles de intervención. Este “filtro” previo evita que al médico le estén saltando alertas de una manera continua y solo le lleguen aquellas que sean relevantes.
Such Diaz A. y col.12 realizan la detección de PRMs en pacientes con IR de manera semiautómática empleando un tiempo medio por farmacéutico de 30-45 min/día para la revisión de este PRM en una media de 28 pacientes. Este dato fue ligeramente superior al obtenido en un estudio realizado por el Servicio de Farmacia del Hospital del Henares previo a este trabajo, donde un farmacéutico emplea un tiempo medio de 26,7 min/día para realizar este tipo de validación en todos los pacientes ingresados7,12.
De los pacientes candidatos a IF presentados por SONAR, el mayor número tanto de pacientes con IF como de IF realizadas se registró en el P1 (158 pacientes y 229 IF).
El P1 (puesta en marcha aplicación) se puede considerar de “rodaje” ya que todos los profesionales sanitarios implicados en el proceso (médicos y farmacéuticos) se enfrentan por primera vez a la toma de decisiones ante una recomendación.
Tanto en el P0 (SONAR se aplicó de manera retrospectiva) como en el P2 (un año después de implantación) el periodo de “rodaje” ha concluido y la aplicación funciona al 100% lo que ha generado un mayor conocimiento en los profesionales (PO: farmacéuticos y P2: médicos y farmacéuticos) sobre utilización de fármacos en la enfermedad renal que deriva en un número menor número de IF en ambos periodos (P0: 71 IF, P2: 96 IF), hecho que corrobora el estudio previo realizado por Devesa García y col.14 en el que la diminución en el número de IF del inicio al final del estudio se atribuye al efecto educativo de la realización de IF en pacientes con IR. Sin embargo, la metodología empleada en la realización de las mismas es diferente a SONAR (no utilizan un soporte informático que integre toda la información de manera fácil y rápida) y esto se consideró una de las limitaciones de su estudio, los autores destacan la necesidad de un buen soporte informático que integre toda la información de manera fácil y rápida para un empleo eficiente del tiempo.
Si tenemos en cuenta las características de los pacientes sobre los que se ha realizado intervención:
– Edad media entorno a los 80-90 años en los tres periodos: los pacientes de edad avanzada tienen mayor probabilidad de sufrir reacciones adversas, incluyendo las derivadas del mal manejo de fármacos en IR, tanto por motivos farmacocinéticos como por las patologías o comorbilidades existentes que derivan en la toma de un número importante de fármacos. Delgado Silveira y col. exponen que hasta un 30% de los ingresos hospitalarios en pacientes mayores se debe a reacciones adversas a medicamentos por prescripción inapropiada. Realizar un ajuste adecuado de la medicación en este tipo de pacientes es de gran importancia15-17.
– Promedio de MDRD-4 entorno a los 30-40 ml/min/1,73m2 en los tres periodos: A partir de los 20-30 años el FG tiende a disminuir aproximadamente 1 ml/min/1,73m2 por año, tanto en mujeres como en hombres. A la edad de 70 años el valor medio de FG se encuentra en torno a 70 ml/min/1,73m2. Esto provoca que ante ciertas situaciones, el FG se desestabilice y con facilidad disminuya por debajo de 60 ml/min/1,73m2 siendo necesario el ajuste de fármacos18.
– Las principales IF se realizaron en pacientes en cuyo diagnóstico se encontraba implicado el sistema cardiovascular, el aparato respiratorio y el aparato digestivo. Estos sistemas se encuentran relacionados con las patologías/comorbilidades frecuentes en pacientes de edad avanzada (patologías cardiacas, cerebrovasculares, diabetes, EPOC, etc.), experimentando muchos de los fármacos para el tratamiento de las mismas un riesgo incrementado de PRMs7,15,19,20.
En los tres periodos el principio activo con mayor número de IF es levofloxacino (25-30%), este dato coincide con otros estudios donde los antibióticos están a la cabeza de las IF3,14,21-24.
– En cuanto al grado de aceptación de las IF; en el P0, intervención teórica, todas las IF fueron clasificadas como rechazadas. En los P1 y P2 SONAR se encontraba implantada, por lo que las IF fueron reales y clasificadas como aceptadas o rechazadas. En el P1 el grado de aceptación fue de 47,6% mientras que en P2 fue de un 77,1%. Estudios de la misma índole cifran su grado de aceptación entorno al 65%14,21-25, dato superior al P1 pero inferior al del P2. Es lógico pensar, que en la época de implantación existiera mayor reticencia por parte del médico a la hora de aceptar las recomendaciones. A medida que la implantación y el funcionamiento de SONAR se fueron afianzando se generó, no solo un grado de aprendizaje en los profesionales sino también una confianza en las recomendaciones que posiblemente justifique el elevado grado de aceptación durante el P2.
Confirmando los resultados de nuestro estudio, existe literatura que evidencia como la implantación de sistemas de soporte a la toma de decisiones clínicas en pacientes con deterioro de la función renal contribuye a la reducción de prescripciones inapropiadas9,12.
CONCLUSIONES
SONAR incrementa la eficiencia de detección de PRMs, muestra un grado de aceptación de las IF elevado, genera efecto aprendizaje en profesionales sanitarios así como confianza en las IF. Además, genera recomendaciones consensuadas y bien documentadas.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
BIBLIOGRAFÍA
1. J. L. Górriz Teruel* y A. Otero González. Impacto socio sanitario de la enfermedad renal crónica avanzada. Nefrología (2008) Supl. 3, 7-15.
2. Swift D. CKD: Individual Risk Tops 50% in Midlife, Study Estimates Am J Kidney Dis. 2015;65:403-411.
3. Ramírez Herráiz E, Ainhoa Aranguren, Oyarzábal, Helena Casas Agudo, Amparo Ibáñez Zurriaga, Alberto Morell Beladrón. Evaluación de las intervenciones farmacéuticas en pacientes con insuficiencia renal. Registro en un programa de prescricpción electrónica. Aten Farm. 2010;12(3):189-92.
4. T. Bermejo Vicedo y Grupo TECNO. Papel del farmacéutico de hospital en las nuevas tecnologías en el sector sanitario. Farm Hosp. 2010;34(2):56-58.
5. Grupo de Nuevas Tecnologías de la SEFH (TECNO). Disponible en: http://www.sefh.es/01grupotecno.php.
6. Tercer Consenso Granada sobre problemas relacionados con medicamentos y resultados negativos asociados a la medicación. Ars Pharm. 2007;48(1):5-17.
7. Gallego Úbeda, M, Tutau Gómez, F, Delgado Téllez, L, Campos Fernández de Sevilla, MA. Impacto de un programa de validación transversal en atención farmacéutica al paciente con insuficiencia renal. Aten Farm. 2011,13(5):257-270.
8. MA. Campos Fernández de Sevilla, F. Tutau Gómez, M. Gallego Úbeda, L. Delgado. Desarrollo de un software integrado de ayuda a la validación farmácéutica. Farm hosp. 2012;36(5):351-355.
9. Martínez Bernabé E, Paluzie- Ávila G, Terre Ohme S, Ruiz Poza D, Parada Aradilla M.A , González Martínez J, et al. Sistemas de soporte a la toma de decisiones clínicas en insuficiencia renal. Farm Hosp. 2014;38(3):216-222.
10. Kawamoto K, Houlihan CA, Balas EA, Lobach DF. “Improving clinical practice using clinical decision support systems: a systematic review of trials to identify features critical to success”. BMJ. 2005;330:765.
11. Bates DW, Kuperman GJ, Wang S, Gandhi T, Kittler A, Volk L, et al. Ten commandments for effective clinical decision support: making the practice of evidence-based medicine a reality. J Am Med Inform Assoc. 2003;10(6):523-30.
12. Such Díaz A, Saez de la Fuente J, Esteva J, Alañón Pardo AM, Barrueco N, Esteban C, et al. Drug prescribing in patients with renal impairment optimized by a computer-based, semi-automated system. Int J Clin Pharm. 2013 Dec;35(6):1170-7.
13. Computerized decision support systems: improving patient safety in nephrology. Chang J. et al. Nat. Rev. Nephrol. 7, 348-355 (2011); published online 19 April 2011; doi:10.1038/nrneph.2011.50.
14. Devesa García C, Matoses Chirivella C, Peral Ballester L, Sanz Tamargo G, Murcia A.C. Atención farmacéutica en pacientes ingresados con insuficiencia renal. Farm Hosp. 2012;36(6):483-491.
15. Gallieni M, Cancarini G. Drugs in the Elderly With Chronic Kidney Disease. Nephrol Dial Transplant. 2015;30(3):342-344.
16. Van Pottelbergh G, Mertens A, Azermani M, Vaes B, Adriaensen W, Mathei C, et al. Drug prescriptions unadapted to the renal function in patients aged 80 years and older. Eur J Gen Pract. 2014 Sep;20(3):190-5.
17. Delgado Silveira E, Muñoz García M, Montero Errasquin B, Sánchez Castellano C,Gallagher P.F.,Cruz-Jentoff A.J. Prescripción inapropiada de medicamentos en los pacientes mayores: los criterios STOPP/START. Rev Esp GeriatrGerontol. 2009;44(5):273-279.
18. Chronic kidney disease: national clinical guideline for early identification and management in adults in primary and secondary care. September 2008: Disponible en http:// guidance.nice.org.uk/CG73/Guidance/pdf/English.
19. Jackson CF, Wenger NK. Enfermedad cardiovascular en el anciano. Rev Esp Cardiol. 2011;64:697-712.
20. De la Iglesia Martínez F, Serrano Arreba J, Montes Santiago J. Enfermedad obstructiva crónica (EPOC) y comorbilidades. Galicia Clin [Internet]. 2012 [citado 30 May 2014]; 73(Supl.1):[aprox. 6 p.]. Disponible en: http://www.galiciaclinica.info/PDF/17/310.pdf.
21. Ruano M, Villamañan Bueno E, Larrubia Márfil Y, Buño Soto A, Pérez E, Moreno F, Herrero A. Adecuación de la farmacoterapia en insuficiencia renal. Utilidad de la prescripción electrónica. Aten Farm. 2012;14(1):27-33.
22. Alañón Pardo AM, Salazar Bravo M, Calleja Hernández MA. Ajuste posológico de antibióticos en pacientes con insuficiencia renal. Aten Farm. 2010;12(1):33-8.
23. Montañés Pauls B, Sáez-Lleó C, Martínez Romero G. Ajuste de dosificación de medicamentos en pacientes ancianos institucionalizados con insuficiencia renal. Farm Hosp. 2009;33(1):43-7.
24. Arrabal-Durán P, Durán García M, Ribed Sánchez A,Hidalgo Collazos P, Sanjurjo Sáez M. Intervenciones farmacéuticas en las prescripciones de pacientes ingresados con insuficiencia renal crónica. Nefrologia. 2014;34(6):710.
25. Hassan Y, Al-Ramahi RJ, Aziz NA, Ghazali R. Impact of a renal drug dosing service on dose adjustment in hospitalized patients with chronic kidney disease. Ann Pharmacother. 2009 Oct;43(10):1598-605.
____
Descargar artículo en PDF: Interoperabilidad aplicada a la atención farmacéutica de pacientes con deterioro de la función renal
