Rev. OFIL 2017, 27;2:201-204
Fecha de recepción: 01/07/2016 – Fecha de aceptación: 14/07/2016
González Freire L, Dávila Pousa MC, Crespo Diz C
Servicio de Farmacia. Complexo Hospitalario Universitario de Pontevedra. Pontevedra (España)
Correspondencia:
Lara González Freire
Avda. de Montecelo, s/n
36071 Mourente (Pontevedra)
Correo electrónico: lara.gonzalez.freire@sergas.es
____
Resumen
La queratoconjuntivitis vernal (QCV) es un episodio severo de conjuntivitis alérgica estacional, más común en los niños durante la primera década de vida, cuyo tratamiento de base son colirios antialérgicos, antiinflamatorios no esteroideos (AINES) y corticoides; en casos refractarios se puede utilizar ciclosporina.
El tacrolimus es un macrólido inmunosupresor que inhibe las fosfatasas de la calcineurina de forma más potente que la ciclosporina y que ha demostrado beneficio a nivel tópico ocular en diversas patologías entre las que se encuentra la QCV.
Se describe el caso de un paciente pediátrico de 6 años de edad diagnosticado desde hace 3 de QCV para el que solicitan la elaboración de un colirio y pomada oftálmica de tacrolimus. Después de un estudio minucioso y revisión bibliográfica de las posibles formulaciones, se recomienda iniciar tratamiento con tacrolimus colirio al 0,03% para probar tolerancia y respuesta a dicha concentración. Tras 6 meses de tratamiento el paciente muestra respuesta sostenida con adecuada tolerancia sin necesidad de administrar otros tratamientos concomitantes.
Palabras clave: Tacrolimus, queratoconjuntivitis, colirio.
Pharmaceutical intervention in the treatment of vernal keratoconjunctivitis with a 0,03% tacrolimus eye drops for a pediatric patient: a case report
____
INTRODUCCIÓN
La queratoconjuntivitis vernal (QCV) es un episodio severo de conjuntivitis alérgica estacional, generalmente presente en ambos ojos y que cursa con inflamación recurrente de la conjuntiva. Es más común en los niños, y aparece en la primera década de vida1. Se considera, junto con la queratoconjuntivitis atópica, la forma más grave de alergia ya que pueden dañar la superficie de la córnea y con ello inducir un déficit de visión permanente. En ella se observan procesos de hipersensibilidad tipo I y IV con elevación de la IgE constante2. Los síntomas consisten en picor intenso, ojos rojos, llorosos, fotofobia y una secreción espesa y pegajosa; en casos graves, puede producirse úlcera en escudo. El tratamiento de elección son colirios antialérgicos, AINES y corticoides3. En casos más graves también se pueden utilizar inmunosupresores como ciclosporina1.
El tacrolimus es un agente macrólido inmunosupresor obtenido por fermentación de Streptomyces tsukubaensis en Japón en 1984. Produce inmunosupresión al inhibir la primera fase de activación de las células T mediante la formación de un complejo con la inmunofilina FKBPB12 que inhibe la actividad de fosfatasas de la calcineurina1,2. La reducción de los niveles de activadores de las células T reduce la respuesta proliferativa de estas células frente a antígenos y mitógenos. Todas estas acciones provocan una disminución del reconocimiento de antígenos y una regulación de los efectos inflamatorios de las conjuntivitis graves2. Esta actividad es similar a la ciclosporina, sin embargo, el tacrolimus posee actividad antiinflamatoria e inmunomoduladora que ha demostrado ser de 10 a 100 veces superior a la ciclosporina4. A nivel tópico ocular ha demostrado su eficacia en diferentes cuadros inflamatorios y alérgicos como queratoconjuntivitis vernal, atópica, papilar gigante, trasplantes corneales de alto riesgo y síndrome de ojo seco severo cuando hay intolerancia a la ciclosporina o refractariedad a otros tratamientos1,5.
DESCRIPCIÓN DEL CASO
El Servicio de Farmacia recibe la solicitud de elaboración de una pomada oftálmica y colirio de tacrolimus 0,1% para un paciente pediátrico de 6 años de edad diagnosticado desde hace 3 de QCV. Los tratamientos ensayados hasta la fecha fueron lágrimas artificiales, antihistamínicos, AINES tópicos, corticoides tópicos y orales. Ante una respuesta no satisfactoria, se inicia tratamiento con ciclosporina 1%. A los 2 meses de tratamiento se reduce la concentración al 0,5% por mala tolerancia. Posteriormente, ante la falta de respuesta con la concentración más baja se suspende el tratamiento.
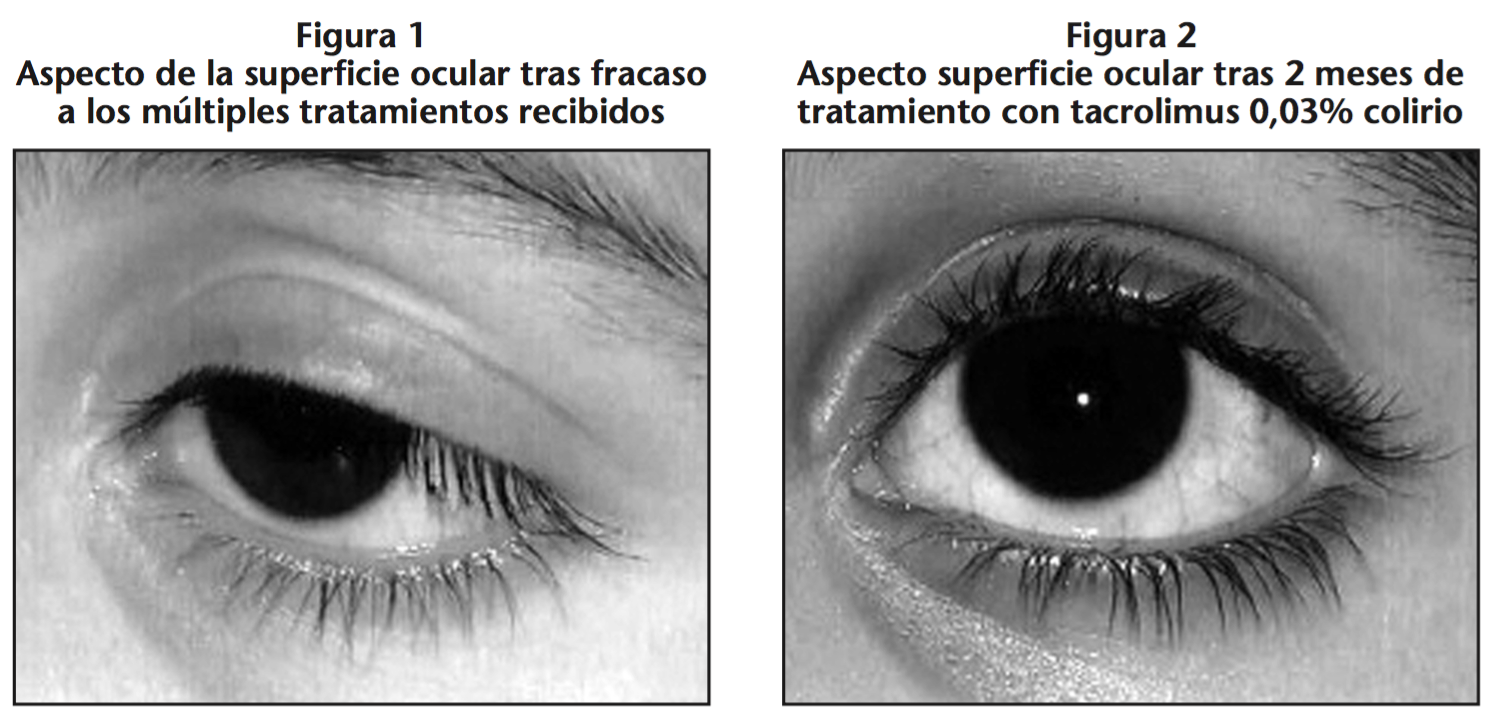
La situación clínica del paciente es preocupante debida a la progresión de la patología y a la mala respuesta a los diferentes tratamientos recibidos, llegando a necesitar intervención quirúrgica para la limpieza de la placa de moco y material adherido a la úlcera producida por la evolución de dicha patología (Figura 1).
Puesto que en el Servicio de Farmacia no se había elaborado ninguna preparación oftálmica de tacrolimus con anterioridad, se realiza una búsqueda bibliográfica.
Diversos estudios consideraron el uso de tacrolimus tópico como una alternativa efectiva y segura para el control de los brotes de QCV y el mantenimiento de sus síntomas. El estudio de Ohashi et al. comparó dosis crecientes de tacrolimus oftálmico (0,01%, 0,03% y 0,1%) y placebo, obteniendo mejores resultados en el grupo que recibió tacrolimus como tratamiento6.
Rikkers y col. mencionaron el beneficio secundario en los síntomas oculares al administrar tacrolimus 0,03% tópico para el tratamiento del eccema del párpado en pacientes con QCV. También, Virtanen reportó mejoría clínica en pacientes con blefaroconjuntivitis atópica tratados con tacrolimus 0,03%7.
Fukushima A y col. realizaron un estudio observacional prospectivo incluyendo a 1.436 pacientes con QCV refractaria al tratamiento convencional, corticoides administrados por vía sistémica e incluso con mala respuesta al tratamiento con ciclosporina. En dicho estudio se demostró que el tratamiento con colirio de tacrolimus 0,1% era altamente efectivo8.
Tacrolimus está disponible como materia prima en España y comercializado en ampollas por vía parenteral (Prograf® 5 mg/mL) que contienen etanol en su composición9. Tacrolimus es insoluble en agua, lo que dificulta la elaboración de un colirio partiendo de materia prima. Desestimamos la elaboración de una pomada oftálmica como primera alternativa por la dificultad del proceso de elaboración y manipulación. Se decide elaborar un colirio partiendo de la presentación comercial en ampollas, pero se propone al Servicio de Oftalmología una concentración más baja, 0,03%, principalmente para minimizar la cantidad de etanol que contiene la presentación comercial y probar la tolerancia del paciente al nuevo tratamiento. Además, ya que se trata de una indicación no autorizada en la ficha técnica de Prograf® 5 mg/mL, se autoriza el tratamiento como uso “fuera de ficha técnica” previa firma del consentimiento informado por parte de los progenitores.
Para la elaboración de la fórmula se tomó como referencia la composición descrita en el ensayo clínico anteriormente comentado de Yuichi Ohashi et al.6 que utilizaba alcohol polivinílico como diluyente en pacientes a partir de 6 años de edad. Se seleccionó como vehículo Liquifilm® lágrimas 14 mg/mL colirio, que contiene alcohol polivinílico como principio activo y cloruro de benzalconio como conservante y que, gracias a su actividad viscosizante, va a favorecer la biodisponibilidad del fármaco al prolongar el tiempo de permanencia del mismo en el epitelio conjuntival.
La composición de la fórmula elaborada para 10 mL de colirio fue la siguiente: 0,6 mL de Prograf® 5 mg/mL y 9,4 mL de Liquifilm® lágrimas 14 mg/mL colirio. Como indicador de estabilidad fisicoquímica se utilizó el pH, cuya lectura se realizó con un medidor Crison Micro pH 2001, obteniendo un valor de 7,22 en el momento de la elaboración y 7,21 a los 7 días. Este valor, próximo al pH fisiológico, es el mejor tolerado por la superficie ocular produciendo una menor alteración del epitelio corneal10.
La Guía de Buenas Prácticas de Preparación de Medicamentos en un Servicio de Farmacia (GBPP) establece para las preparaciones de riesgo bajo (nuestro caso) elaboradas bajo cabina de flujo laminar con entorno controlado un plazo de validez microbiológico de 14 días a 2-8°C11. Sin embargo, se estableció un periodo de validez de 7 días a 2-8°C que permitiese el tratamiento domiciliario, validando durante este tiempo las propiedades físicas y control de pH.
A los 7-10 días del inicio del tratamiento, se había resuelto el proceso ulceroso y con ello se produjo una disminución de la secreción de moco, fotofobia, picor y el lagrimeo (Figura 2).
El paciente ha recibido, desde su inicio, 6 meses de tratamiento con tacrolimus 0,03% con respuesta sostenida y buena tolerancia.
En la actualidad el tratamiento de base es, únicamente, tacrolimus 0,03% colirio administrado dos veces al día. Todos los tratamientos a base de corticoides y antiinflamatorios han sido suspendidos. El oftalmólogo considera imprescindible el tratamiento hasta la resolución definitiva del proceso.
DISCUSIÓN
La QCV es conocida como una de las patologías oftálmicas alérgicas más severas pudiendo llegar a provocar daño corneal e incluso pérdida de visión. Durante la evolución de la enfermedad, los pacientes pueden tener múltiples recaídas de los síntomas afectando a su calidad de vida de forma importante7.
Ninguno de los medicamentos disponibles, utilizado de manera aislada, es suficiente para controlar el proceso inflamatorio. Los corticoesteroides son utilizados en casos severos y refractarios pero su uso prolongado por vía oftálmica puede llegar a provocar aumento de la presión intraocular y opacificación del cristalino lo que limita su aplicación. Aunque La ciclosporina A ha demostrado ser un tratamiento efectivo, la sensación de quemazón que reportan algunos pacientes hace que disminuya su tolerancia, especialmente en pacientes pediátricos7.
En la bibliografía revisada, diversos estudios consideraron el uso de tacrolimus por vía tópica oftálmica como una alternativa efectiva y segura en el tratamiento de la QCV y con una actividad inmunomoduladora y antiinflamatoria superior a la ciclospirina.
Frente a estas ventajas, la insolubilidad de tacrolimus limita su uso como materia prima para la elaboración de un colirio. La presentación comercial en ampollas (Prograf®) permite su utilización en solución aunque el contenido en etanol puede presentar problemas de tolerancia a concentraciones más altas. Por este motivo es recomendable iniciar tratamiento con la concentración más baja (0,03%) y probar tolerancia.
Salvo la sensación de quemazón, atribuida en nuestro caso a la pequeña cantidad de etanol que contienen las ampollas de Prograf®; en la literatura no se ha descrito ningún efecto adverso con el uso de tacrolimus, ya sea en forma de gotas oftálmicas como en pomada.
Dada la mejoría observada en nuestro paciente con la concentración más baja referenciada en la bibliografía y con respuesta rápida, mantenida y sin aparición de efectos adversos, tacrolimus 0,03% colirio se presenta como una buena alternativa para el tratamiento de la QCV refractaria al tratamiento convencional.
CONCLUSIÓN
En base a los resultados obtenidos en este caso, la elaboración de un colirio de tacrolimus 0,03% está justificada para su utilización como tratamiento único de los síntomas de la QCV. Aunque es necesaria una mayor experiencia, el desarrollo de esta fórmula podría ser un gran avance en el tratamiento de la QCV.
Conflicto de intereses: Los autores declaran no tener conflictos de intereses.
BIBLIOGRAFÍA
1. Rodriguez Ausin P. Uso actual del tacrolimus y ciclosporina tópicos en enfermedades de la superficie ocular. Boletín de la Soc. Oftalmo. De Madrid – Nº 53 (2013). Disponible en: http://www.oftalmo.com/som/index. php/2012-11-30-17-37-36/numero-53-2013/31-revista/revista-53/controversias-en-superficie-e-inflamacion-ocular/89-m2013-16 (acceso 28 Mar 2016).
2. De la Torre Morín F. Tacrolimus en las blefaroconjuntivitis graves. Alergia, asma e inmunología pediátricas. Vol. 17, Num. 2 Mayo-Agosto 2008 (70-73). Disponible en: http://www.medigraphic.com/pdfs/alergia/al-2008/al082c.pdf (citado 28 Mar 2016).
3. Sacchetti M, lambiase A, Mantelli F, Deligianni V, Leonardi A, Bonini S. Tailored approach to the treatment of vernal keratoconjunctivitis. Ophthalmology. 2010 Jul;117(7):1294-9. Diponible en: http://www.ncbi. nlm.nih.gov/pubmed/20382430 (citado 28 Mar 2016).
4. Coral Ghanem R, Ferreira Da Costa Vargas J and Coral Ghanem Vinícius. Tacrolimus for the teratment of subepithelial infiltrates resistant to topical steroids after adenoviral keratoconjunctivitis. Cornea, Volume 33, Number 11, November 2014. Disponible en: http://ovidsp.ovid.com/ovidweb.cgi?T=JS&CSC=Y&NEWS=N&PAGE=fulltext&D=ovft&AN=00003226-201411000-00015&PDF=y (citado 28 Mar 2016).
5. Sanz-Marco E, et al. Treatment of refractory dry eye associated with graft versus host disease with 0.03% tacrolimus eyedrops. Journal of ocular pharmacology and therapeutics. Vol. 29, Nume. 8, 2013 (776-783). Disponible en: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3787325/pdf/jop.2012.0265.pdf (citado 28 Mar 2016).
6. Yuichi Ohashi, et al. A Randomized, placebo-controlled clinical trial of tacrolimus ophthalmic suspension 0.1% in severe allergic conjunctivitis. Journal of Ocular Pharmacology and Therapeutics. Vol. 26. Num. 2, 2010 (165-173). Disponible en: http://www.ncbi.nlm.nih. gov/pmc/articles/PMC3158389/pdf/jop.2009.0087.pdf (citado 28 Mar 2016).
7. Helena Ramirez R, et al. Queratoconjuntivitis vernal refractaria: ¿es el tacrolimus una opción terapéutica? Estudio prospectivo. Alergia, Asma e Inmunología Pediátricas. Vol. 21, Num. 1 Enero-Abril 2012 (5-12). Disponible en: http://www.medigraphic.com/pdfs/ alergia/al-2012/al121b.pdf (citado 28 Mar 2016).
8. Atsuki Fukushima, et al. Therapeutic effects of 0.1% tacrolimus eye drops for refractory allergic ocular diseases with proliferative lesion or corneal involvement. Br J Ophthalmol. 2014;98:1023-1027. Disponible en: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4112440/pdf/bjophthalmol-2013-304453.pdf (citado 19 Abr 2016).
9. Agencia Española del Medicamento y Productos Sanitarios (AEMPS). Ficha técnica Tacrolimus (Prograf® 5mg/mL). 2015. Disponible en: http://www.aemps. gob.es/cima/pdfs/es/ft/61004/FT_61004.pdf (citado 28 Mar 2016).
10. Gubert Müller G, Kara José N, Silvestre de Castro R. Topical tacrolimus 0.03% as sole therapy in vernal keratoconjunctivitis, a randomized double-masked study. Eye Contact Lens. 2014;40(2):79-83. Disponible en: http://www.ncbi.nlm.nih.gov/pubmed/24418865 (citado 28 Mar 2016).
11. Guía de Buenas Prácticas de Preparación de Medicamentos en Servicios de Farmacia Hospitalaria. Junio 2014. Ministerio de Sanidad, Servicios Sociales e Igualdad. Disponible en: http://www.msssi.gob.es/profesionales/farmacia/pdf/GuiaBPP3.pdf (citado 08 Jul 2016).
____
Descargar artículo en PDF: Intervención farmacéutica en el tratamiento de la queratoconjuntivitis vernal con tacrolimus 0,03% colirio en paciente pediátrico, a propósito de un caso
