Espadas Hervás N, Molina Mendoza MD, Gramage Caro T, Vélez-Díaz-Pallarés M
Servicio de Farmacia. Hospital Ramón y Cajal. Madrid (España)
Fecha de recepción: 30/07/2018 – Fecha de aceptación: 06/08/2018
Correspondencia
Noelia Espadas Hervás – Hospital Ramón y Cajal – Ctra. de Colmenar Viejo, km. 9,100 – 28034 Madrid (España)
noelia.espadas@salud.madrid.org
____
Resumen
Fundamentos: La aparición del tratamiento antirretroviral (TAR) supuso una disminución en la mortalidad por síndrome de inmunodeficiencia adquirida (SIDA).
El cobicistat se ha situado en primera línea del TAR. Se incluye en combinaciones de alta eficacia, buena tolerancia y elevada comodidad por su posología. Su principal inconveniente es el alto número de interacciones, ya que es inhibidor metabólico a distintos niveles. Este hecho resalta la importancia de conciliar los tratamientos crónicos de los pacientes que empiezan tratamiento con cobicistat, y los tratamientos introducidos una vez iniciado este TAR.
Métodos y resultados: Se presentan los casos de dos pacientes con una intoxicación por tacrolimus y budesonida, al administrarse de forma concomitante con cobicistat. En el caso 1, el paciente presentó niveles tóxicos de tacrolimus en sangre que se tradujeron en síntomas de toxicidad por dicho fármaco. En el caso 2, el paciente sufrió un síndrome de Cushing iatrogénico, descrito como una probable reacción adversa de budesonida.
Conclusiones: Actualmente, numerosos TAR incluyen fármacos potenciadores farmacocinéticos como ritonavir y cobicistat. Éste último, actúa de forma predominante sobre el CYP3A4, lo que teóricamente reduce el riesgo de interacciones potenciales respecto a ritonavir. A pesar de esto, los TAR con cobicistat presentan un elevado número de interacciones por lo que es imprescindible conciliar el tratamiento crónico al inicio de la terapia antirretoviral, así como con los fármacos introducidos durante la misma. En dicha tarea, el farmacéutico hospitalario tiene un papel fundamental, así como en la educación al paciente.
Palabras clave: Interacción farmacológica, cobicistat, tacrolimus, budesonida, farmacia hospitalaria.
____
Severe intoxications in patients with cobicistat containing HIV therapies: case series
Summary
Background: The introduction of antiretroviral therapy (ART) has decreased the mortality in patients with acquired immune deficiency syndrome (AIDS).
Cobicistat is a first line ART. It is included in fixed-dose combination of drugs with high effectiveness, good tolerance and convenience. Its main handicap is the great amount of drug-drug interactions, because the molecule is a metabolic inhibitor at different levels. Thus, the importance of medication reconciliation of the chronic treatments of patients who start treatment with cobicistat, and the prescriptions introduced once this ART has begun.
Methods and results: We present the cases of two patients with overdose of tacrolimus and budesonide, when cobicistat was administered. In the first case, the patient presented toxic blood tacrolimus concentrations, which caused symptoms of tacrolimus toxicity. In the second case, the patient suffered a Cushing syndrome, as a probable adverse reaction to budesonide.
Conclusions: At the present time, many ART include pharmacokinetic boosters such as ritonavir or cobicistat. The last one is more specific for CYP3A4, which should reduce the risk of interactions in comparison with ritonavir. However, ART with cobicistat presents numerous drug-drug interactions, thus it is very important to check the chronic treatment at the beginning of antiretroviral therapy, as well as the drugs introduced during the treatment. The hospital pharmacist plays an important role in this task and in patient education.
Key Words: Drug interactions, cobicistat, tacrolimus, budesonide, Pharmacy Service Hospital.
____
Introducción
La aparición del tratamiento antirretroviral (TAR) supuso una disminución en la mortalidad por síndrome de inmunodeficiencia adquirida (SIDA)1. Las nuevas combinaciones farmacológicas, junto al aumento de la esperanza de vida, han incrementado la complejidad del manejo farmacológico de estos pacientes, necesitando un control estricto de las interacciones.
El cobicistat se ha situado en primera línea del TAR1. Se incluye en combinaciones de alta eficacia, buena tolerancia y elevada comodidad por su posología. Su principal inconveniente es el alto número de interacciones, ya que es un potente inhibidor del CYP3A, inhibidor débil del CYP2D6 e inhibidor de la glicoproteína-P. Este hecho resalta la importancia de conciliar los tratamientos crónicos de los pacientes que empiezan tratamiento con cobicistat, y los tratamientos introducidos una vez iniciado este TAR.
Se presentan los casos de dos pacientes que sufrieron intoxicación con tacrolimus y budesonida al cambiar su TAR e introducir cobicistat.
Material y métodos
Caso 1
Varón de 46 años que acudió a Urgencias por náuseas, vómitos, diarrea, cefalea y distermia. Como antecedentes médicos presentaba infección por VIH diagnosticada en 1994 y trasplante hepático en 2009. El paciente estaba en tratamiento con tacrolimus (Advagraf®) 2 mg/día. Al iniciar tratamiento con elvitegravir-cobicistat-emtricitabina-tenofovir alafenamida (Genvoya®), su medico decidió reducir la dosis de forma empírica a 1 mg/día. Tras 4 días, se observaron niveles infraterapéuticos de tacrolimus, subiendo la dosis de nuevo a 2 mg/día.
Una semana después de iniciar Genvoya®, se observó deterioro de la función renal (Cr: 2,04 mg/dL; TFG: 35,33 mL/min) y se ingresó al paciente con sospecha de intoxicación por tacrolimus por posible interacción con cobicistat (niveles séricos de tacrolimus: 39,40 ng/mL; niveles terapéuticos en mantenimiento: 5-20 ng/mL).
Tras 24 horas de la suspensión de tacrolimus se recuperó la función renal (Cr: 1,17 mg/dL; TFG: 67,11 mL/min) y descendieron los niveles séricos del fármaco (29,90 ng/mL). El paciente fue dado de alta tras 48 horas de ingreso sin tacrolimus, manteniendo Genvoya®.
Tras el alta hospitalaria, se reintrodujo tacrolimus a dosis de 0,5 mg dos veces en semana, alcanzando niveles de tacrolimus de 5,10 ng/mL una semana después. Durante los meses sucesivos se ajustaron las dosis de tacrolimus, cuyos niveles fueron estrechamente monitorizados tanto en la consulta médica como en la de atención farmacéutica. (Figura 1 y Figura 2).
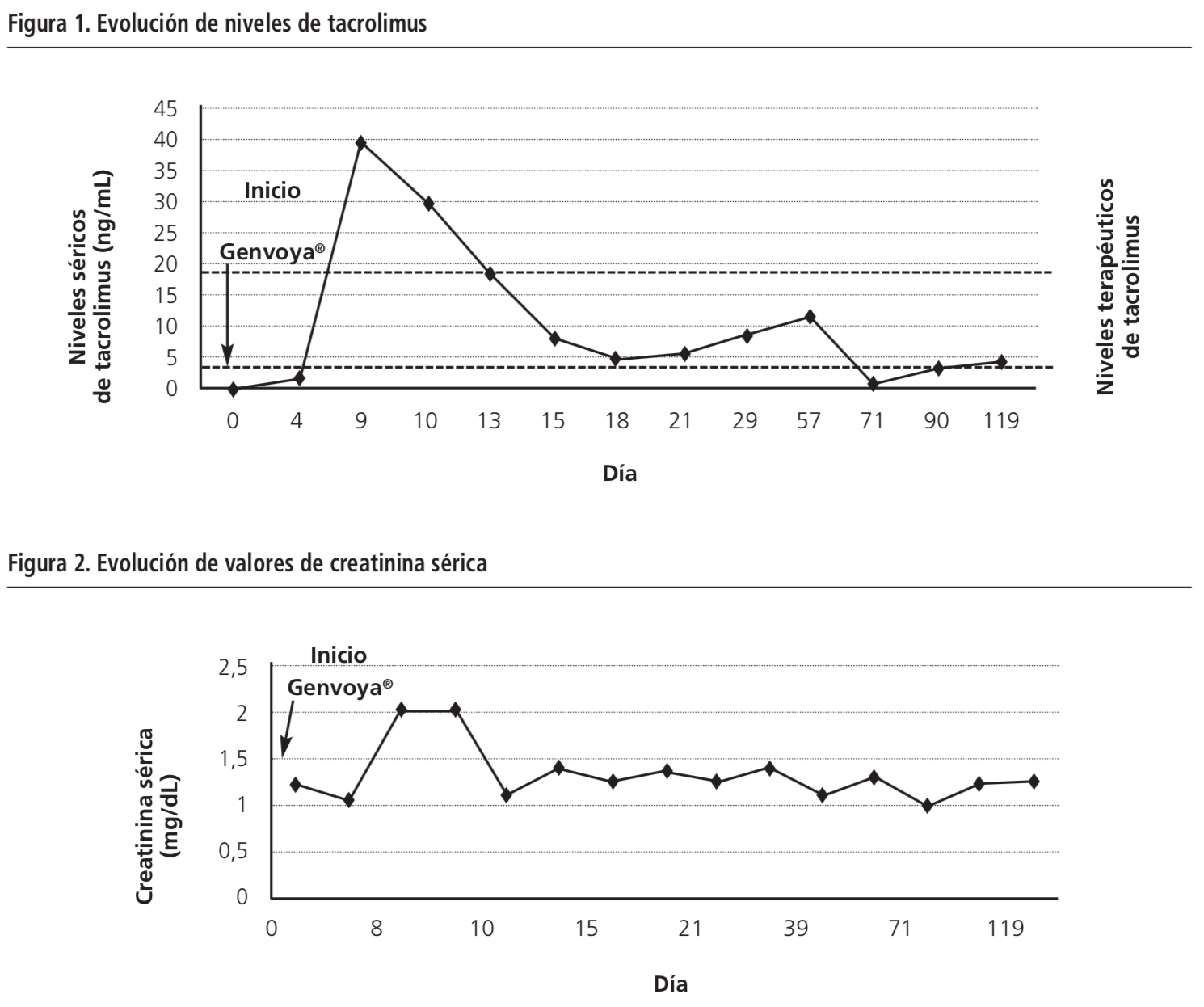
Este caso se ha notificado al Centro Español de Farmacovigilancia.
Caso 2
Varón de 54 años que ingresó a cargo de Enfermedades Infecciosas para estudio de edema facial y abdominal, y leves edemas vespertinos de miembros inferiores. Como antecedentes médicos destacaban EPOC tipo enfisema centrolobulillar e infección crónica por VIH diagnosticada en 2003, en tratamiento actual con Genvoya®.
Cuatro meses antes, comenzó progresivamente a manifestar los edemas y una reagudización respiratoria del EPOC, por lo que inició tratamiento con formoterol-budesonida (Symbicort®). Al ingreso, el paciente presentó una tensión arterial de 130/80 mmHg, una frecuencia cardíaca de 120 latidos por minuto, facies cushingoide, obesidad troncular y un valor de glucosa de 135 mg/dL (70-110 mg/dL).
El diagnóstico fue de síndrome de Cushing iatrogénico. Se suspendió formoterol-budesonida y se pautó hidrocortisona, pendiente de reevaluar en 1-2 meses mediante test corto de cortisol tras estimulación con corticotropina (ACTH). Se pautó como nuevo inhalador tiotropio-olodaterol (Spiolto®) y se modificó el TAR, sustituyéndose Genvoya® por dolutegravir (Tivicay®) y emtricitabina-tenofovir (Truvada®), tras la comprobación por el farmacéutico de que en este caso no había interacciones. El paciente fue dado de alta tras 10 días de ingreso.
Este caso se ha notificado al Centro Español de Farmacovigilancia.
Discusión
Se presentan los casos de dos pacientes con una intoxicación por tacrolimus y budesonida, al administrarse de forma concomitante con cobicistat. En el caso 1, el paciente presentó niveles tóxicos de tacrolimus en sangre que se tradujeron en síntomas de toxicidad por dicho fármaco. La ficha técnica de Advagraf® especifica que al administrarse junto con inhibidores enzimáticos del CYP3A4 se recomienda la monitorización estrecha del fármaco2. En el caso 2, el paciente sufrió un síndrome de Cushing iatrogénico, descrito como una probable reacción adversa de budesonida3. La administración de Genvoya® con budesonida está contraindicada por el riesgo de desarrollar síndrome de Cushing y supresión adrenal4,5.
Aplicando la escala de probabilidad de interacción de fármacos (Drug Interaction Probability Scale-DIPS)6 se obtuvo una puntuación de 7 en el caso 1, y una puntuación de 6 en el caso 2, lo que determina la relación causal de interacción entre dichos fármacos como “probable”5-8. Han et al.7 describen una interacción similar entre tacrolimus (Prograf®) y Stribild®, y obtienen una puntuación de 6 aplicando la misma escala. Ambas reacciones adversas se comunicaron al Centro Madrileño de Farmacovigilancia.
Actualmente, numerosos TAR incluyen fármacos potenciadores farmacocinéticos como ritonavir y cobicistat, que logran un aumento de la exposición sistémica de los inhibidores de la proteasa. Cobicistat actúa de forma predominante sobre el CYP3A4, lo que teóricamente reduce el riesgo de interacciones potenciales respecto a ritonavir. Sin embargo, distintas publicaciones describen la interacción de cobicistat con otros fármacos, algunas de ellas con graves resultados como isquemia aguda en miembros inferiores o neuropatía periférica8,9.
Estos dos casos resaltan la importancia del papel del farmacéutico en la monitorización de los tratamientos y la detección de problemas relacionados con los medicamentos (PRM). En los tratamientos con inmunosupresores en pacientes trasplantados, es recomendable revisar los niveles del fármaco al introducir un TAR con cobicistat y advertir al médico de la potencial interacción. Para detectar la posible toxicidad es aconsejable revisar las analíticas y entrevistar al paciente en la consulta de Atención Farmacéutica para identificar posibles efectos adversos. En el caso de tratamientos con corticoides, es recomendable evitar tratamientos prolongados y seleccionar aquellos con un metabolismo distinto al que inhibe cobicistat. En pacientes con EPOC o asma, el farmacéutico debe conciliar la medicación y recomendar al médico evitar tratamientos que contengan budesonida o fluticasona. Como alternativa se podría utilizar beclometasona5, cuyo metabolismo es menos dependiente de la vía CYP3A4. El riesgo de interacción es menor por vía inhalatoria, aunque no debe subestimarse nunca el riesgo de producir interacciones5,10.
En conclusión, los TAR con cobicistat presentan un elevado número de interacciones por lo que es imprescindible conciliar el tratamiento crónico al inicio de la terapia antirretoviral, así como con los fármacos introducidos durante la misma. En dicha tarea, el farmacéutico hospitalario tiene un papel fundamental así como en la educación al paciente.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
Bibliografía
1. GeSIDA [página web]. Documento de consenso de GeSIDA/Plan Nacional sobre el Sida respecto al tratamiento antirretroviral en adultos infectados por el virus de la inmunodeficiencia humana. (Actualización de Enero de 2017, acceso 30 de marzo de 2017) http://www.gesida-seimc.org/contenidos/guiasclinicas/2017/gesida-guiasclinicas-2017-TAR.pdf
2. Agencia Española de Medicamentos y Productos Sanitarios. CIMA (centro de información de medicamentos). Ficha técnica de Advagraf® 1mg (tacrolimus) [Base de datos en Internet]. España: Agencia Española de Medicamentos y Productos Sanitarios [consultado el 24/08/2017]. Disponible en: https://www. aemps.gob.es/cima/pdfs//ft/07387014/FT_07387014.pdf
3. Agencia Española de Medicamentos y Productos Sanitarios. CIMA (centro de información de medicamentos). Ficha técnica de Symbicort Turbuhaler® 80mcg/4,5mg (budesonida-formoterol fumarato dihidrato) [Base de datos en Internet]. España: Agencia Española de Medicamentos y Productos Sanitarios [consultado el 24/08/2017]. Disponible en: https://www.aemps.gob.es/cima/ dochtml/ft/63956/FichaTecnica_63956.html.
4. Agencia Española de Medicamentos y Productos Sanitarios. CIMA (centro de información de medicamentos). Ficha técnica de Genvoya® 150mg/150mg/ 200mg/10mg (Emtricitabina-tenofovir alafenamida-elvitegravir -cobicistat) [Base de datos en Internet]. España: Agencia Española de Medicamentos y Productos Sanitarios [consultado el 24/08/2017]. Disponible en: http://www. ema.europa.eu/docs/es_ES/document_library/EPAR_-_Product_Information/ human/004042/WC500197861.pdf.
5. Elliot ER, Theodoraki A, Jain LR, Marshall NJ, Boffito M, Baldeweg SE, et al. Iatrogenic Cushing’s syndrome due to drug interaction between glucocorticoids and the ritonavir or cobicistat containing HIV therapies. Clin Med. 2016;16(5): 412-418.
6. Horn J, Hansten P, Chan L. Proposal for a new tool to evaluate drug interaction cases. Ann Pharmacother. 2007;41(4):674-80.
7. Han Z, Kane BM, Petty LA, Josephson MA, Sutor J, Pursell KJ. Cobicistat significantly increases tacrolimus serum concentrations in a renal transplant recipient with immunodeficiency virus infection. Pharmacotherapy. 2016;36(6): e50-e53.
8. Navarro J, Curran A, Burgos J, Torrella A, Ocaña I, Falcó V, et al. Acute leg ischaemia in an HIV-infected patient receiving antirretroviral treatment. Antivir Ther. 2017;22(1):89-90.
9. Bidon D, Bauler S, Venon MD, Dupont C. Cobicistat-vinblastine interaction and severe peripheral neuropathy. AIDS. 2015;29(9):1120-1.
10. Choi T, Neven A, Al Hadithy AF. A disulfiram-alcohol reaction after inhalation of a salbutamol aerosol: a plausible interaction? Tijdschr Psychiatr. 2016;58(5): 407-10.
____
