Gil-Sierra MD1, Briceño-Casado MP2
1 Servicio de Farmacia. Hospital Universitario de Puerto Real. Puerto Real. Cádiz (España)
2 Servicio de Farmacia. Hospital General Nuestra Señora del Prado. Talavera de la Reina. Toledo (España)
Fecha de recepción: 01/03/2021 – Fecha de aceptación: 22/03/2021
Correspondencia: Manuel David Gil Sierra – Calle Playa de Bolonia, 10 – 11406 Jerez de la Frontera, Cádiz (España)
mangilsie@yahoo.com
____
RESUMEN
La enfermedad de Crohn es una patología inflamatoria que afecta a cualquier parte del tracto gastrointestinal, aunque puede tener manifestaciones sistémicas y extraintestinales. Los fármacos biológicos se usan en pacientes con enfermedad de Crohn moderada-severa refractarios a terapias previas. Existen reacciones psoriasiformes paradójicas asociadas a tratamientos biológicos que actúan sobre el factor de necrosis tumoral (anti-TNF α), como adalimumab. Por otra parte, ustekinumab ha sido descrita como una alternativa terapéutica eficaz con un favorable perfil de seguridad en pacientes con co-morbilidades y/o reacciones de hipersensibilidad a otros fármacos. La colaboración multidisciplinar de diferentes profesionales sanitarios permite la identificación de eventos adversos poco frecuentes, como es la reacción psoriasiforme paradójica, y la optimización terapéutica de pacientes complejos. Este trabajo permite profundizar en la experiencia clínica y terapéutica de una colaboración multidisciplinar en una paciente complicada diagnosticada de enfermedad de Crohn, con reacción psoriasiforme paradójica secundaria a adalimumab.
Palabras clave: Ustekinumab, comorbilidad, reacción adversa, reacción psoriasiforme.
Multidisciplinary clinical management of complex patient with Crohn’s disease and paradoxical psoriasiform reaction
SUMMARY
Crohn’s disease is an inflammatory disease of any part of the gastrointestinal tract. This pathology can present systemic and extra-intestinal manifestations. Biological drugs are used in patients with moderate-severe Crohn’s disease refractory to previous therapies. Paradoxical psoriasiform reactions have been associated with biological treatments with an anti-tumor necrosis factor (anti-TNF α) mechanism, such as adalimumab. On the other hand, ustekinumab has been described as an effective therapeutic alternative with a favorable safety profile in patients with comorbidities and/or hypersensitivity reactions to other drugs. The multidisciplinary collaboration of different healthcare professionals allows the identification of infrequent adverse events –such as paradoxical psoriasiform reaction– and therapeutic optimization of complex patients. This case describes the clinical and therapeutic experience of a multidisciplinary collaboration in a complicated patient diagnosed with Crohn’s disease and a paradoxical psoriasiform reaction secondary to adalimumab.
Key words: Ustekinumab, comorbidity, adverse reaction, psoriasiform reaction.
____
INTRODUCCIÓN
La enfermedad de Crohn es una patología inflamatoria que afecta al tracto gastrointestinal, pudiendo tener manifestaciones sistémicas y extraintestinales1. Su gravedad suele valorarse mediante los sistemas Crohn’s Disease Activity Index y Harvey-Bradshaw Index2,3. Los pacientes con alto riesgo de padecer enfermedad de Crohn moderada-grave suelen presentar diagnóstico temprano (<30 años), tabaquismo, enfermedad perianal, úlceras intestinales y niveles elevados de proteína C-reactiva (PCR).
Los fármacos biológicos se usan en pacientes sin respuesta a corticoesteroides y/o inmunosupresores, o con contraindicaciones para dichos tratamientos4,5. Adalimumab es un anticuerpo que neutraliza al factor de necrosis tumoral (anti-TNF α). Se han descrito reacciones psoriasiformes paradójicas asociadas a tratamientos biológicos anti-TNF α6. Se distinguen dos tipos de este evento adverso: psoriasis de novo y el empeoramiento en pacientes con psoriasis. Esta reacción adversa es un efecto de clase infrecuente descrito ante tres anti-TNF α clásicos (infliximab, adalimumab y etanercept)7, afectando a la calidad de vida de los pacientes.
Ustekinumab es un anticuerpo que se une a las interleuquinas IL-12 e IL-235. Este fármaco se presenta como alternativa terapéutica con favorable perfil de seguridad, escasa inmunogenicidad y actividad antiinflamatoria sistémica8. Se usa en pacientes refractarios a tratamientos anti-TNF α y pacientes jóvenes con otras enfermedades inmunomediadas. Además, ustekinumab puede emplearse de forma segura en pacientes con neoplasias previas, a diferencia de los fármacos anti-TNF α, asociados con varios tipos de tumores (como leucemia, linfomas, etc).
La displasia es una proliferación celular anómala que puede preceder a una neoplasia invasiva del tracto digestivo9. La displasia se divide en dos categorías: bajo y alto grado. La consideración de la displasia epitelial tiene gran relevancia en la enfermedad inflamatoria intestinal, influyendo en la toma de decisiones terapéuticas. Este caso describe el manejo clínico multidisciplinar de una paciente con comorbilidades y enfermedad de Crohn, que presentó reacción psoriasiforme paradójica secundaria a adalimumab.
DESCRIPCIÓN DEL CASO
Paciente exfumadora de 54 años diagnosticada de enfermedad de Crohn hace más de 20 años. También presenta enfermedad de Parkinson y migraña. Se trató inicialmente con azatioprina, pero refirió vómitos y diarreas. En 2014 se cambia el tratamiento por 6-mercaptopurina.
En 01/2016 acudió a Urgencias por dolor abdominal generalizado, aumento del número y consistencia de deposiciones, y presencia de sangre. En la colonoscopia se determinó actividad leve-moderada y signos inflamatorios en sigma. En colon izquierdo se detectó displasia de bajo grado y proctitis crónica en el recto. Se inició adalimumab 160 mg en semana 0,80 mg en semana 2 y posteriormente, 40 mg en semanas alternas por brote de enfermedad de Crohn ileocolónica activa e intolerancia a inmunomoduladores. Comenzó el tratamiento en 04/2016 y dos meses después la paciente refirió lesiones cutáneas en brazo que impresionaron de lunares nuevos.
En 04/2017 apareció abundante exudación purulenta perianal espontánea con curso de aproximadamente mes y medio. En 05/2017 se realizó una tomografía computerizada con contraste y se confirmó hernia pararrectal derecha, que fue intervenida.
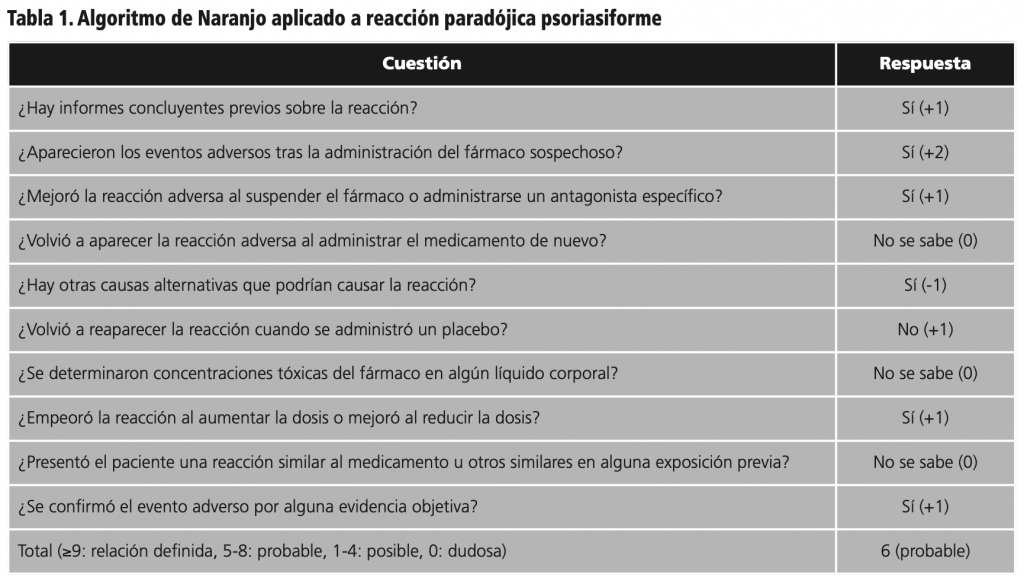
En 06/2017 se observaron lesiones psoriasiformes múltiples en tronco y zona genital. Se realizó interconsulta con Servicio de Dermatología, pautándose corticoides tópicos y sugiriéndose como reacción secundaria a adalimumab. El especialista en farmacia hospitalaria aplicó algoritmo de Naranjo, estableciéndose relación “probable” entre adalimumab y la reacción paradójica psoriasiforme10. Los resultados de esta herramienta son mostrados en la tabla 1. En 08/2017 persistieron las lesiones psoriasiformes múltiples en tronco, miembros superiores e inferiores y genitales. En la exploración física se impresionó de abdomen depresible, doloroso a palpación profunda en epigastrio e hipocondrio derecho, y signo de Murphy negativo. En 09/2017 se valoró cambio de tratamiento biológico a ustekinumab por efecto adverso asociado al anti-TNF α.
La colonoscopia de 03/2018 mostró ausencia de actividad endoscópica y contexto inflamatorio en recto. En 04/2018 se inició la dosis de inducción de ustekinumab intravenoso (390 mg). Las dosis posteriores fueron 90 mg vía subcutánea a las 8 semanas de la primera dosis, posteriormente fueron cada 12 semanas según evolución clínica. En 09/2018 se alcanza remisión clínica, bioquímica y endoscópica. En 11/2019 se realiza resonancia magnética con trayecto fistuloso en pliegue interglúteo izquierdo con trayecto lineal fino y homogéneo. La hipointensidad de señal marcada en secuencias potenciadas fue sugerente de tejido fibrótico con escasa actividad inflamatoria.
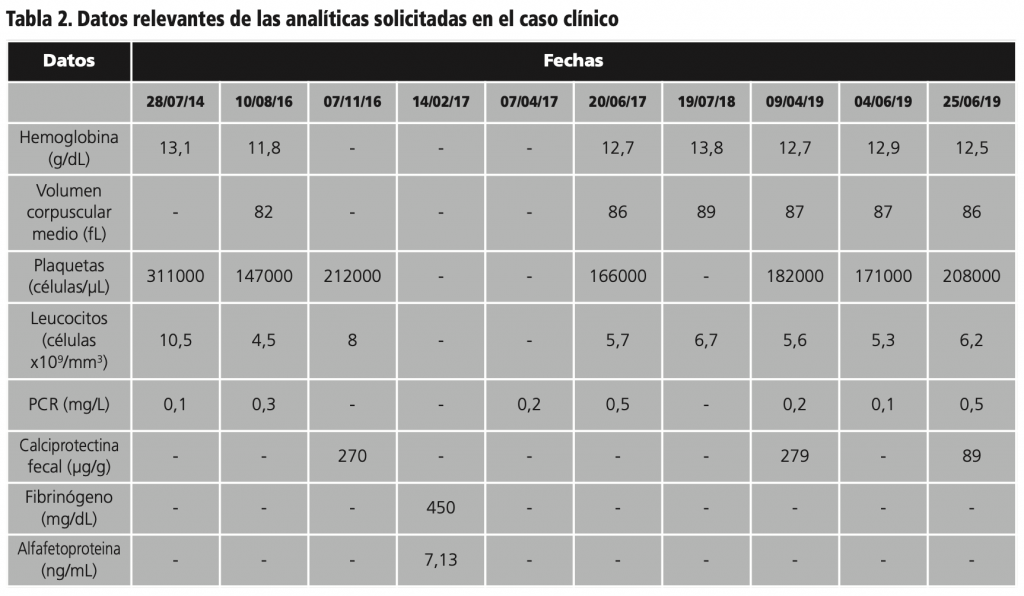
Hasta 09/2020 la paciente no ha presentado exudación de orificio fistuloso, así como rectorragia ni melenas. La paciente recibe ustekinumab cada 12 semanas alcanzando la remisión completa (clínica, bioquímica y endoscópica). No se han descrito reacciones adversas ni progresión de la displasia tras casi dos años y medio de tratamiento. Los datos relevantes de las analíticas realizadas pueden consultarse en la tabla 2.
DISCUSIÓN
Nuestra paciente alcanzó remisión clínica, bioquímica y endoscópica al ser tratada con ustekinumab, a diferencia de la respuesta observada a adalimumab. Asimismo, ustekinumab ha obtenido una tolerancia adecuada en una paciente con antecedentes de efectos adversos cutáneos a tratamiento previo. Tal y como afirman algunos expertos, ustekinumab es un fármaco adecuado para pacientes de alto riesgo, con comorbilidades y enfermedad perianal activa8.
Por otra parte, la displasia observada no presentó progresión. Esta estabilización permitió un abordaje más sencillo9. La monitorización de la evolución de las displasias es esencial para la detección temprana de un posible carcinoma en contexto de enfermedad de Crohn, que podría desembocar en la llamada “cancerización de campo” y colectomía.
Asimismo, se ha podido apreciar como el trabajo multidisciplinar de diferentes profesionales sanitarios (especialistas en aparato digestivo, dermatología y en farmacia hospitalaria) ha permitido identificar un evento adverso poco común, como es la reacción psoriasiforme paradójica6,7. La derivación del paciente por parte del facultativo especialista en aparato digestivo al dermatólogo garantizó un tratamiento adecuado de la reacción adversa cutánea. Por otra parte, la aplicación del algoritmo de Naranjo, llevada a cabo por el farmacéutico especialista en farmacia hospitalaria, permitió establecer mediante una herramienta sistemática la relación de causalidad entre la administración de adalimumab y la aparición de reacción psoriasiforme paradójica10. Todo ello favoreció un buen manejo del paciente y la selección de una alternativa terapéutica con relación de beneficio-riesgo favorable, como es ustekinumab.
Conflictos de intereses: Gil-Sierra MD participó en un advisory board de Janssen Pharmaceutica y en un simposio sobre fármacos onco-hematológicos. El resto de los autores no posee conflictos de interés.
BIBLIOGRAFÍA
1. Burgmann T, Clara I, Graff L, Walker J, Lix L, Rawsthorne P, et al. The Manitoba Inflammatory Bowel Disease Cohort Study: prolonged symptoms before diagnosis–how much is irritable bowel syndrome? Clin Gastroenterol Hepatol 2006; 4:614. Doi: 10.1016/j.cgh.2006.03.003.
2. Best WR, Becktel JM, Singleton JW, Kern F Jr. Development of a Crohn`s disease activity infex. National Cooperative Crohn`s Disease Study. Gastroenterology. 1976;70(3):439-444.
3. Harvey RF, and Bradshaw JM. A simple index of Crohn’s-disease activity. Lancet 1980;1:514-514. Doi: 10.1016/s0140-6736(80)92767-1.
4. Agencia Española de Medicamentos y Productos Sanitarios. Ficha técnica de adalimumab. [citado 20 septiembre 2020]. Disponible en: https://cima. aemps.es/cima/dochtml/ft/103256017/FT_103256017.html.
5. Agencia Española de Medicamentos y Productos Sanitarios. Ficha técnica de ustekinumab. [citado 20 septiembre 2020]. Disponible: https://cima.aemps. es/cima/pdfs/ft/108494004/FT_108494004.pdf.
6. Navarro R, Daudén E. Clinical management of paradoxical psoriasiform reactions during TNF- α therapy. Actas Dermosifiliogr. 2014;105(8):752-61. Doi: 10.1016/j.ad.2013.05.007.
7. Ko JM, Gottlieb AB, Kerbleski JF. Induction and exacerbation of psoriasis with TNF-blockade therapy: a review and analysis of 127 cases. J Dermatolog Treat. 2009;20:100-8. Doi: 10.1080/09546630802441234.
8. Armuzzi A, Ardizzone S, Biancone L, Castiglione F, Danese S, Gionchetti P, et al. Ustekinumab in the management of Crohn`s disease: Expert opinión. Dig Liver Dis. 2018;50(7):653-660. Doi: 10.1016/j.dld.2018.02.017
9. Salas Caudevilla A. Evaluation of displasia in gastrointestinal diseases. Gastroenterol Hepatol. 2007; 30(10):602-11. Doi: 10.1157/13112598
10. Naranjo CA, Busto U, Sellers EM, Sandor P, Ruiz I, Roberts EA, et al. A method for estimating the probability of adverse drug reactions. Clin Pharmacol Ther. 1981;30(2):239-45.
____
