Toja Camba FJ1, Rodríguez Rodríguez MP2, Grandío Leivas L1
1 Residente en Farmacia Hospitalaria
2 Facultativo Especialista en Farmacia Hospitalaria
Servicio de Farmacia. Complejo Hospitalario Universitario de Ourense (España)
Fecha de recepción: 13/05/2020 – Fecha de aceptación: 27/06/2020
Correspondencia: Francisco José Toja Camba – Ramón Puga, 52 – Ourense 32005 (España)
kikotoja@gmail.com
____
RESUMEN
Las infecciones oportunistas en pacientes sometidos a trasplante de órgano sólido (TOS) son una causa de morbimortalidad muy importante. Entre ellas las infecciones fúngicas, aunque menos frecuentes, destacan por su alta mortalidad. Una de las infecciones por hongos más usual es la ocasionada por Aspergillus. El tratamiento de elección de aspergilosis invasiva en un paciente con TOS es voriconazol.
Presentamos el caso de un paciente inmunodeprimido tras trasplante renal con cuadro de sepsis grave de origen respiratorio en probable contexto de una aspergilosis invasiva. El interés del caso radica en la intervención farmacéutica en el complejo manejo farmacológico del paciente a lo largo de su estancia en la Unidad de Críticos y en la terapia antimicrobiana satisfactoria con isavuconazol, un nuevo antifúngico.
Palabras clave: Aspergillus, transplante, sepsis.
Therapeutic management of invasive aspergillosis in a transplant patient and isavuconazole as a new antifungal alternative
SUMMARY
Opportunistic infections in patients undergoing solid organ transplantation (TOS) are a very important cause of morbidity and mortality. Among them, fungal infections, stand out for their higher mortality. One of the most frequent fungal infections is caused by Aspergillus. There are more than 150 species of Aspergillus, being Aspergillus fumigatus the most common agent of invasive fungal infections in human. Gold standard treatment for invasive aspergillosis in a patient with TOS is voriconazole.
We present the case of a kidney transplanted and immunocompromised patient with severe sepsis of respiratory origin in context of invasive aspergillosis. Interest of this case lies on the multiple pharmaceutical interventions in the patient’s complex pharmacological management throughout his stay in the critics unit and satisfactory treat-ment with isavuconazole, a new antifungal.
Key words: Aspergillus, transplants, sepsis.
____
DESCRIPCIÓN DEL CASO
Varón de 58 años, con antecedentes de:
– Enfermedad renal crónica (ERC) estadío 5 por glomerulonefritis focal y segmentaria en diálisis peritoneal. Trasplante renal de donante cadáver 7 meses antes del ingreso actual, a tratamiento inmunosupresor con tacrolimus 4 mg/día y prednisona 15 mg/día.
– Hemorragia intraparenquimatosa.
– Infección por citomegalovirus (CMV) con clínica digestiva alta, finalizado tratamiento con ganciclovir.
Ingresa por insuficiencia respiratoria en contexto de neumonía comunitaria, iniciando tratamiento con levofloxacino y oseltamivir. A las 24h, tras empeoramiento clínico-radiológico (SOFA score=2) se activa código sepsis e ingresa en la UCI. Se amplía tratamiento antimicrobiano empírico a meropenem, linezolid, sulfame-toxazol/trimetropim y ganciclovir por el estado de inmunosupresión, a pesar de que el paciente se mantiene afebril y con procalcitonina (PCT) 0,4 ng/mL. Resultados microbiológicos: antigenurias Legionela y neumococo negativas, VRS+, gripe negativa. Se suspende oseltamivir.
El día 4 en UCI empeoramiento radiológico compatible con micosis oportunista, se solicita antígeno galactomanano en muestra de lavado broncoalveolar y se amplía cobertura empírica con voriconazol IV.
El día 7, deterioro de la función renal (creatinina (Cr)=2,1 mg/dL) de probable origen multifactorial. Se realiza una determinación predosis de nivel plasmático de tacrolimus con resultado de sobredosificación (40 ng/mL), relacionado muy probablemente con el inicio de voriconazol. Se realiza terapia secuenial de voriconazol a vía oral (no indicada la formulación IV con valor de aclaramiento de creatinina inferior a 30ml/min).
El día 10, mala tolerancia oral y necesidad de utilizar la vía intravenosa, función renal similar a previa. Se recomienda sustituir voriconazol por isavuconazol.
El día 13, se filia la sepsis como aspergilosis pulmonar invasora. La analítica muestra una trombopenia severa cuya causa más probable se atribuye al tratamiento con ganciclovir y linezolid.
El día 21, se recomienda cambio de ganciclovir intravenoso a valganciclovir oral.
El día 30, episodio de temblor generalizado que requiere tratamiento anticomicial. Se desaconseja fenitoína por interacción farmacocinética con tacrolimus e isavuconazol. Ante sospecha de aspergilosis cerebral, se decide ampliar terapia antifúngica a anfotericina B liposomal más isavuconazol.
Los niveles plasmáticos de tacrolimus son fluctuantes e infraterapéuticos para el tiempo post-trasplante (8 meses), por lo que se decide utilizar la vía intravenosa administrando en perfusión continua la quinta parte de la dosis oral.
El día 46, RMN cerebral muestra lesiones compatibles con Aspergillus. Se retiran corticoesteroides y resto de inmunosupresores.
A día 67, se realiza nueva RMN cerebral objetivándose una evidente desaparición de las lesiones.
El día 106, traslado a la Unidad de Enfermedades Infecciosas y el día 118 tras resolución completa de las lesiones cerebrales, alta a domicilio.
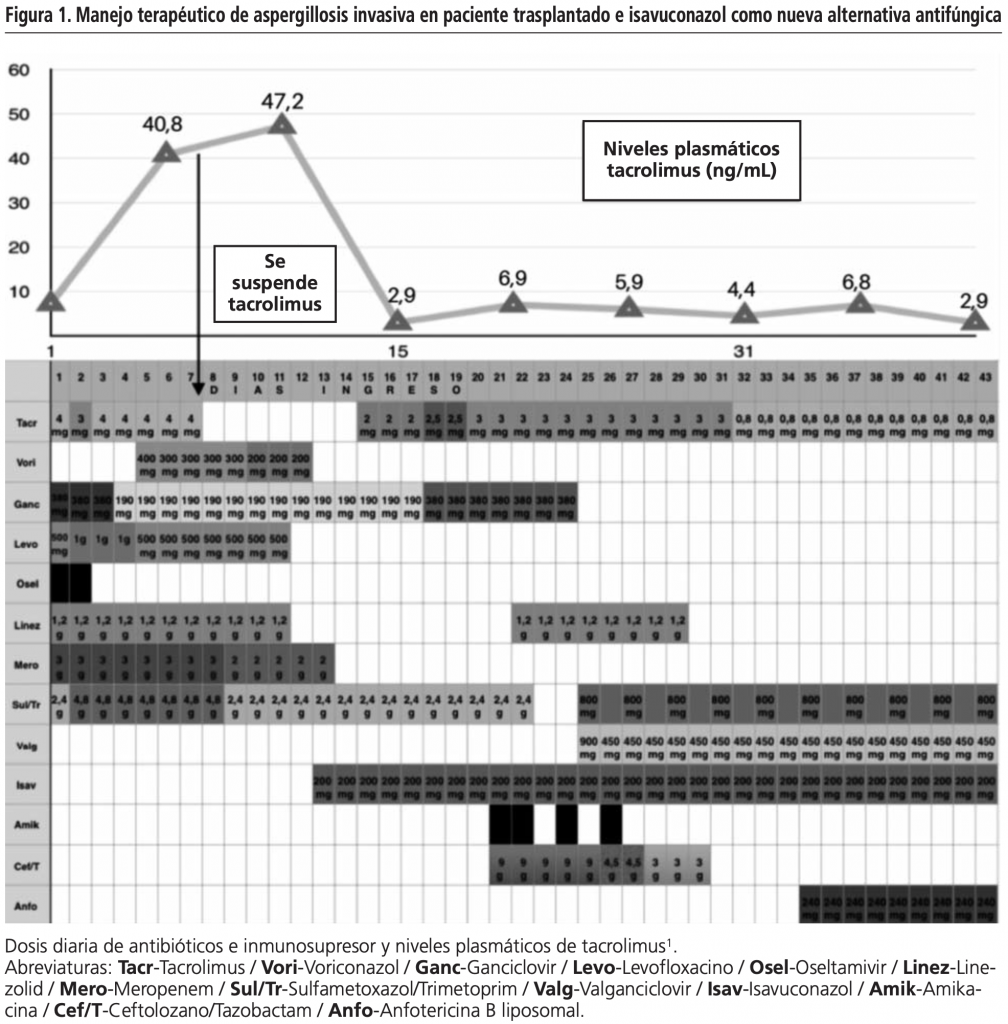
El paciente continúa en tratamiento oral con isavuconazol hasta completar 9 meses, sin manifestar reacciones adversas (Figura 1).
Discusión y aportación farmacéutica
La colaboración del farmacéutico en la resolución de este caso ha sido de suma importancia, aportando una visión global a la optimización del tratamiento. Relatamos a continuación las principales intervenciones realizadas:
1. Interacción voriconazol-tacrolimus
Voriconazol es el tratamiento de elección de aspergilosis invasora en pacientes con patología no hematológica2. Su administración concomitante con inmunosupresores no está exenta de riesgos debido a interacciones farmacocinéticas.
Voriconazol es un potente inhibidor del CYP3A4 que incrementa de manera importante el área bajo la curva (AUC) de niveles plasmáticos de tacrolimus. Diversos estudios sitúan este incremento en un 300%. En nuestro caso se propone al inicio de la terapia antifúngica reducir un 50% la dosis de tacrolimus. Esta recomendación fue rechazada por el facultativo responsable hasta disponer del nivel plasmático solicitado, que se obtiene tres días más tarde y que confirma dicha interacción. Se suspende tratamiento con tacrolimus hasta normalización de nivel.
2. Cambio de terapia antifúngica
Ante la mala tolerancia oral del paciente, deterioro de la función renal e interacción voriconazol-tacrolimus se propone tratamiento con isavuconazol en base a:
– Formulación intravenosa exenta de ciclodextrina. Diversas publicaciones alertan sobre la acumulación de este oligosacárido cíclico en pacientes con deterioro de la función renal.
– Menor interacción antifúngico-inmunosupresor. Diversos estudios señalan a isavuconazol como el triazol con menos influencia en la actividad del CYP3A4.
Además de la aportación farmacéutica en la elección de una nueva alternativa de tratamiento, se instruyó a enfermería en la administración intravenosa de isavuconazol que requiere un equipo de perfusión con filtro en línea3-5.
3. Pancitopenia por linezolid y ganciclovir
La pancitopenia producida por linezolid y con mayor frecuencia por ganciclovir ha sido descrita ampliamente en la literatura. Nuestro paciente presentó una clara trombopenia (33.000/mcL) y una leucopenia (3670/mcl) menos acentuada, que se atribuyó como causa más probable la administración de estos antimicrobianos. Se suspende linezolid pero se mantiene la profilaxis con ganciclovir debido al riesgo elevado de infección por citomegalovirus (CMV) en pacientes con TOS.
4. Interacción anticomicial y antifúngico
Fenitoína es un potente inductor enzimático del CYP3A4/5 por lo que las concentraciones plasmáticas de isavuconazol y tacrolimus se verían disminuidas de forma importante. Se propone levetiracetam como tratamiento anticomicial alternativo.
5. Cambio de profilaxis para CMV
Tras 21 días de tratamiento con ganciclovir se propone el cambio a valganciclovir ajustando la dosis a función renal. El valganciclovir ha demostrado no inferioridad en cuanto a actividad frente a CMV en comparación con ganciclovir.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
BIBLIOGRAFÍA
1. Xiao, A. J., Miller, B. W., Huntington, J. A., Nicolau, D. P. Ceftolozane/tazobactam pharmacokinetic/pharmacodynamic-derived dose justification for phase 3 studies in patients with nosocomial pneumonia. The Journal of Clinical Pharmacology. 2016;56(1):56-66.
2. Patterson, T. F., Thompson III, G. R., Denning, D. W., Fishman, J. A., Hadley, S., Herbrecht, R et al. Practice guidelines for the diagnosis and management of aspergillosis: 2016 update by the Infectious Diseases Society of America. Clinical Infectious Diseases. 2016;63(4):e1-e60.
3. Fichas técnicas. Centro de Información de Medicamentos. Agencia Española de Medicamentos y Productos Sanitarios. Disponible en: hup://www.aemps.gob. es/cima/fichasTecnicas.do?metodo=detalleForm.
4. Wilson, D. T., Dimondi, V. P., Johnson, S. W., Jones, T. M., Drew, R. H. Role of isavuconazole in the treatment of invasive fungal infections. 2016;12:1197-1206.
5. Garcia-Vidal, C., Alastruey-Izquierdo, A., Aguilar-Guisado, M., Carratalà, J. Executive summary of clinical practice guideline for the management of invasive diseases caused by Aspergillus: 2018 Update by the GEMICOMED-SEIMC/REIPI. Documento de consenso del GEMI-COMED perteneciente a la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica (SEIMC) sobre el tratamiento de las infecciones invasoras producidas por Aspergillus. 2018.
____
