Morgado S1, Morgado M2, Fonseca O3
1 Mestre em Ciências Farmacêuticas. Especialista em Farmácia Hospitalar
2 Licenciado em Ciências Farmacêuticas. Mestre em Biotecnologia. Doutor em Biomedicina. Especialista em Farmácia Hospitalar
3 Licenciada em Ciências Farmacêuticas. Especialista em Farmácia Hospitalar. Diretora dos Serviços Farmacêuticos. Centro Hospitalar Cova da Beira – Hospital Universitário. Covilhã (Portugal)
____
Rev. OFIL 2016, 26;3:205-212
Fecha de recepción: 021/09/2015 – Fecha de aceptación: 14/10/2015
____
RESUMO
Objetivo: Identificar e obter informações acerca dos medicamentos que possuem autorização de introdução no mercado (AIM) em Portugal e que podem ser administrados por via intratecal.
Material e métodos: Consulta à base de dados da Autoridade Nacional do Medicamento e Produtos de Saúde (INFARMED), o Infomed, realizada em Maio de 2015, foi possível identificar e obter informações, através dos Resumos das Características do Medicamento (RCM), acerca dos medicamentos que possuem AIM em Portugal e que podem ser administrados por via intratecal.
Resultados e discussão: Os medicamentos encontrados foram: baclofeno, morfina, bupivacaína, levobupivacaína, ropivacaína, metotrexato, citarabina, iopamidol e iodixanol. Os cinco primeiros atuam deprimindo o sistema nervoso central, promovendo analgesia ou anestesia. O metotrexato e a citarabina são antineoplásicos e imunomoduladores e os dois últimos são fármacos utilizados como meios de contraste para diagnóstico. A administração intratecal é muito útil para a distribuição do fármaco no fluido cerebroespinal, com redução dos efeitos secundários sistémicos.
Palavras chave: INFARMED, administração intratecal, fluido cerebroespinal, medicamentos.
____
Correspondencia:
Sandra Morgado
Serviços Farmacêuticos do Centro Hospitalar Cova da Beira
Hospital Universitário, Quinta do Alvito
6200-251 Covilhã (Portugal)
Correo electrónico: sandracristinamorgado@gmail.com
____
INTRODUÇÃO
Lo conceito de barreira hematoencefálica (BHE) surgiu no final do século XIX, na Alemanha, através de experiências do cientista Paul Ehrlich onde, após injeções de corantes em animais, tanto na circulação arterial como na venosa, todos os órgãos, excepto o cérebro e a medula espinal, se coravam, conduzindo à hipótese da existência de dois compartimentos1. Para que um fármaco atue no sistema nervoso central é necessário que o mesmo alcance o fluido cerebroespinal. A barreira hematoencefálica dificulta a passagem de fármacos do sangue para o sistema nervoso central e uma das formas de facilitar o acesso de medicamentos a este local é por meio da sua administração por via intratecal, que consiste em injetar o fármaco no espaço subaracnoideu2. Tal via de administração é muito eficiente na promoção da analgesia e anestesia, apresentando vantagens como um rápido início de ação, ausência de bloqueio motor, baixa exposição materno/fetal a fármacos, diminuição dos efeitos secundários sistémicos e facilidade de realização da técnica. Também é utilizada para medicamentos que funcionem como meios de contraste para diagnóstico, imunomoduladores e antineoplásicos.
Em Portugal, o INFARMED constitui a autoridade nacional do medicamento e a tal instituto compete “Autorizar o fabrico, a importação, a introdução no mercado de medicamentos de uso humano”3. Dessa forma nenhum medicamento pode ser comercializado nem utilizado sem que o mesmo tenha sido previamente autorizado pelo INFARMED. Neste âmbito, temos disponíveis no mercado, naturalmente com autorização do INFARMED, os fármacos: baclofeno, bupivacaína, levobupivacaína, citarabina, iodixanol, iopamidol, morfina, metotrexato e ropivacaína.
MATERIAL E MÉTODOS
Na pesquisa pelos medicamentos passíveis de administração intratecal com autorização de introdução no mercado (AIM) em Portugal os autores recorreram primeiramente às fontes electrónicas da Base de Dados de Medicamentos de Uso Humano da Autoridade Nacional do Medicamento e Produtos de Saúde4 e ao Prontuário Terapêutico Online, também através do site electrónico do INFARMED5. A referida pesquisa foi realizada em Maio de 2015. Nenhuma das fontes dispunha de mecanismos de busca adequados para identificação imediata dos medicamentos em questão, mas a utilização de um motor de busca externo permitiu a identificação de nove medicamentos com autorização para administração via intratecal, nomeadamente: baclofeno, bupivacaína, levobupivacaína, ropivacaína, citarabina, iodixanol, iopamidol, morfina e metotrexato.
Com o intuito de descrever os aspectos terapêuticos mais importantes dos medicamentos mencionados, a principal fonte utilizada foram os Resumos das Características do Medicamento (RCM), obtidos diretamente do site electrónico do INFARMED4.
A informação recolhida é de considerável importância para a prática dos farmacêuticos hospitalares, tendo em vista a utilização eficaz e segura dos medicamentos supramencionados e da via de administração intratecal. Contribui, além disso, para evitar erros graves de medicação, potencialmente fatais, através da sinalização dos medicamentos para os quais a via de administração intratecal está autorizada.
RESULTADOS E DISCUSSÃO
Baclofeno
O baclofeno é um agonista do ácido gama-aminobutírico (GABA), estruturalmente idêntico. É um dos fármacos antiespásticos mais utilizados, estando comercializado na forma oral desde 19746.
A dificuldade de atravessar a BHE pelo baclofeno implica, em alguns casos, na necessidade de administração de doses orais elevadas para obtenção de concentrações eficazes a nível do liquor, dando origem a efeitos secundários excessivos, por vezes não tolerados. Nesse contexto, a administração por via intratecal surge como uma alternativa válida para a terapêutica com baclofeno7. A administração por esta via foi proposta em 1985, por Richard Penn6. Em Portugal, encontrase autorizada pelo INFARMED para administração intratecal, sendo, comercializado pelo nome comercial de “Lioresal Intratecal®”, em ampolas de 0,05 mg/1 mL e 10 mg/5 mL4.
Indicações
O baclofeno intratecal está indicado em doentes com espasticidade crónica grave de origem espinal ou de origem cerebral que não respondam à administração oral de antiespásticos e/ou que apresentam efeitos indesejáveis intoleráveis com doses eficazes por via oral. O início da terapêutica é recomendado apenas após estabilização dos sintomas de espasticidade, ou seja, pelo menos um ano após o traumatismo. Em pediatria, o baclofeno intratecal apenas está indicado em crianças acima dos 4 anos7.
Posologia
O estabelecimento do regime posológico ótimo requer que cada doente seja submetido a uma fase inicial de determinação da dose eficaz com um bólus intratecal, seguindo-se uma titulação muito cuidadosa da dose individual antes da terapêutica de manutenção.
A individualização posológica é de grande importância devido à grande variabilidade da dose terapêutica eficaz7.
A administração de baclofeno intratecal em bólus (por cateter espinal ou punção lombar) é a primeira abordagem para o estabelecimento do regime terapêutico, precedendo a perfusão crónica. A dose teste usualmente administrada inicialmente, em adultos e pediátricos (≥4 anos), é de 25 ou 50 microgramas, elevando-se gradualmente em incrementos de 25 microgramas com intervalos mínimos de 24 horas até se observar uma resposta com a duração entre 4 e 8 horas. Esta dose é administrada no espaço subaracnoideu durante, pelo menos, um minuto; é necessário dispor de equipamento de reanimação para utilização imediata7.
Se o doente não responder a uma dose teste de 100 microgramas, não deve ser submetido a incrementos de dose adicionais, nem a perfusão intratecal contínua. Considera-se que os doentes responderam ao tratamento quando evidenciam uma redução significativa do tónus muscular e/ou da frequência e/ou gravidade dos espasmos7.
A dose de teste inicial por punção lombar em doentes com idades compreendidas entre os 4 e os 18 anos deve ser 25-50 microgramas por dia, tendo em conta a idade e o tamanho da criança/jovem. Os doentes que não respondam ao tratamento podem receber um escalonamento da dose de 25 microgramas/dia em cada 24 horas. A dose máxima da fase de determinação da dose eficaz não deve exceder 100 microgramas por dia em doentes pediátricos.
Após o estabelecimento da dose eficaz, pode considerar-se a implantação de bombas apropriadas para administração contínua no espaço intratecal (bombas certificadas pela União Europeia). Para doentes com espasticidade de origem espinal, a dose diária pode ser gradualmente aumentada 10 a 30% de modo a manter-se o controlo adequado da sintomatologia, regulando a velocidade de administração da bomba e/ou a concentração de baclofeno no reservatório. Para doentes com espasticidade de origem cerebral, a dose diária pode ser gradualmente aumentada 5 a 20%, mas não mais de 20%, de modo a manter-se o controlo adequado da sintomatologia, regulando a velocidade de administração da bomba e/ou a concentração de baclofeno intratecal no reservatório. Em ambos os casos, a dose diária pode igualmente ser reduzida 10 a 20% se os doentes evidenciarem efeitos indesejáveis7.
A dose de manutenção da perfusão contínua, a longo prazo em doentes com espasticidade de origem espinal, varia entre 12 e 2003 microgramas por dia, sendo a maioria dos doentes mantidos com doses entre 300 e 800 microgramas por dia7.
Em doentes com espasticidade de origem cerebral, a dose varia entre 22 e 1.400 microgramas por dia, com uma média diária de 276 microgramas por dia aos 12 meses e 307 microgramas por dia aos 24 meses. Em crianças/jovens com idades compreendidas entre os 4 e os 18 anos com espasticidade de origem cerebral e de origem espinal, a dose inicial de manutenção para perfusão contínua a longo prazo de baclofeno intratecal varia de 25 a 200 microgramas/dia (dose mediana: 100 microgramas/dia)7.
Observações
O baclofeno demonstrou possuir propriedades depressoras gerais sobre o SNC, provocando sedação, sonolência e depressão respiratória e cardiovascular7.
Para a dose teste, existem à disposição ampolas de baixa concentração, contendo 0,05 mg/ml7.
O fármaco não deve ser administrado por via intravenosa, intramuscular, subcutânea ou epidural7.
No caso de doentes que requeiram outras concentrações, não disponíveis por ampolas, estas podem ser diluídas, em condições asséticas, com cloreto de sódio isento de conservantes para uso injetável7.
O sistema de bomba só deve ser implantado após conveniente avaliação da resposta do doente à titulação da dose. A recarga do reservatório deve ser efetuada por pessoal devidamente treinado e qualificado de acordo com as instruções facultadas pelo fabricante da bomba. Os intervalos de recarga devem ser cuidadosamente calculados de modo a evitar a depleção do reservatório, que pode induzir recidiva da espasticidade grave ou potencial risco de vida devido a sintomas associados a uma interrupção repentina7.
Os doentes que sofrem de perturbações psicóticas, esquizofrenia, estados confusionais ou doença de Parkinson devem ser tratados, com precaução, com baclofeno intratecal e serem mantidos sob rigorosa vigilância médica, dado terem sido observados casos de exacerbação destas patologias durante a administração oral de baclofeno7.
A sobredosagem grave provoca depressão respiratória, apneia e coma7.
Bupivacaína
Composta por uma mistura racémica de seus isómeros R e S, a bupivacaína é um anestésico local com alta potência e duração, que possui um efeito de bloqueio senso-motor diferencial8. Assim como outros fármacos para tal efeito, a bupivacaína desempenha a sua ação ao impedir o fluxo iónico membranar de sódio para as células do sistema nervoso, bloqueando a propagação do impulso nervoso9. Estudos clínicos demonstraram que o isómero dextrogiro é o principal responsável pelo mais importante efeito adverso do fármaco, que é a cardiotoxicidade10. A bupivacaína para administração intratecal é comercializada em Portugal pelo nome comercial de “Marcaína Espinal Pesada®” em ampolas de dosagem de 20 mg/4 ml9.
Indicações
A anestesia por bupivacaína está indicada em: anestesia intratecal (subaracnoideia, espinal) para procedimentos cirúrgicos e obstétricos e para cirurgia abdominal inferior (incluindo cesariana), urológica e dos membros inferiores, incluindo cirurgia da anca, com duração de 1,5-3 horas9.
Posologia
Adultos e crianças com idades superiores a 12 anos (Tabela 1).
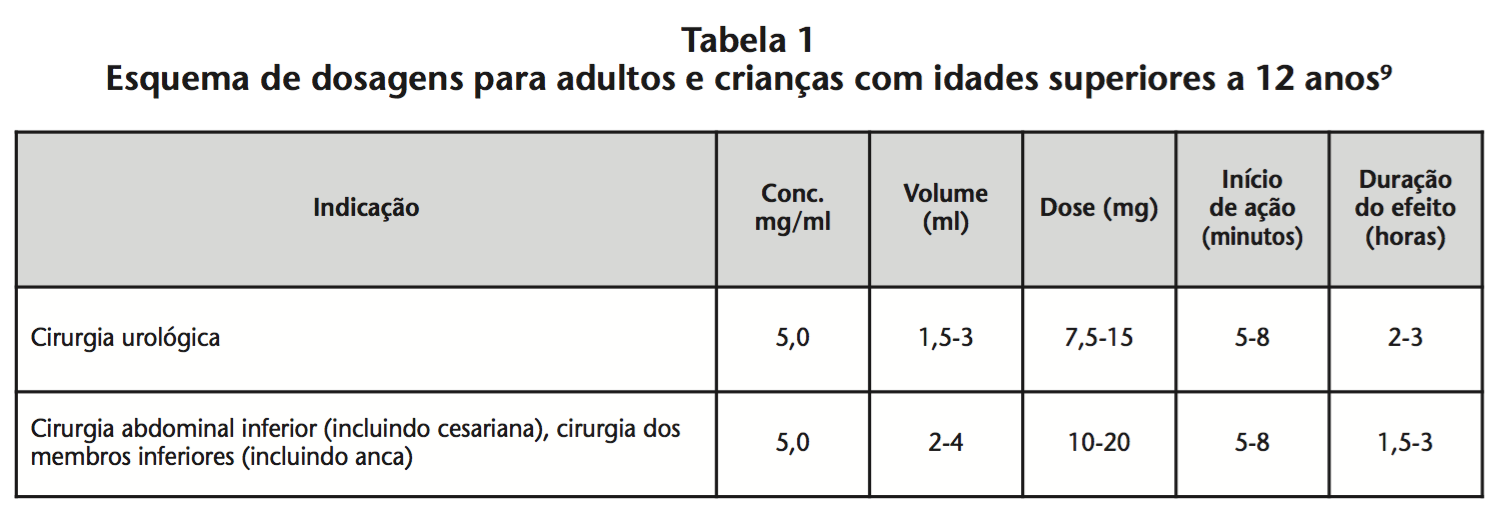
As dosagens indicadas na tabela são as consideradas necessárias para a produção de um bloqueio eficaz e devem ser consideradas como uma orientação para um adulto de estatura média. Os valores indicam a gama esperada de doses médias necessárias. O estado físico do doente e o uso de terapêutica concomitante devem ser tidos em consideração na determinação da dose, devendo usar-se a dose mais baixa que permita obter uma anestesia eficaz. Ocorrem variações individuais no início e na duração do efeito.
A dose deverá ser reduzida nos idosos e em doentes nos estadios finais da gravidez.
Crianças com peso até 40 kg (Tabela 2).
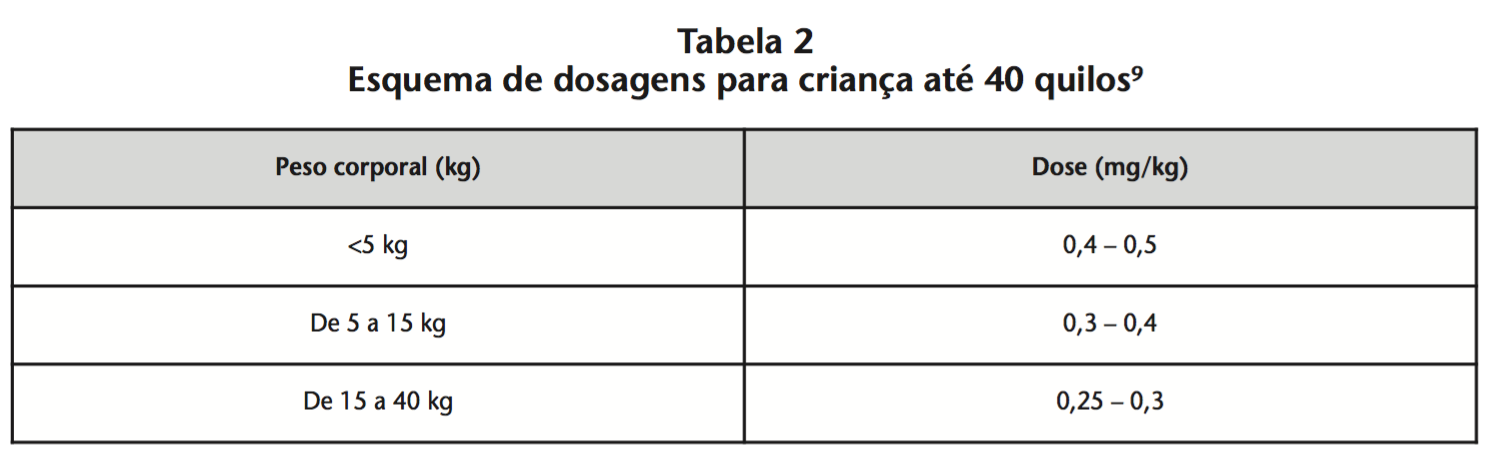
A Marcaína Espinal Pesada pode ser usada em crianças.
Uma das diferenças entre crianças pequenas e adultos é que o volume de líquido cerebroespinal é relativamente superior em crianças e recém-nascidos, sendo necessárias doses/kg relativamente superiores para produzir o mesmo nível de bloqueio que nos adultos9.
Observações
Os efeitos adversos muito frequentes da bupivacaína são hipotensão, bradicardia e náuseas9.
Não se considera que a anestesia intratecal afete adversamente os distúrbios neurológicos, tais como esclerose múltipla, hemiplegia, paraplegia e distúrbios neuromusculares, mas estas situações requerem precaução9.
A bupivacaína é um anestésico local do tipo amida. Administrada como anestésico intratecal tem um rápido início de ação e uma duração de ação média a longa. A duração da ação anestésica é dependente da dose9.
Citarabina
A citarabina é um efetivo agente de quimioterapia bastante utilizado no tratamento da leucemia. A citarabina para administração intratecal é comercializada em Portugal na forma de soluções injectáveis 20 mg/mL com os nomes de “ARA-Cell®” e “Citaloxan®”11.
Indicações
A citarabina pode ser utilizada em monoterapia ou em associação, sendo indicada para indução da remissão e/ou tratamento de manutenção em doentes com leucemia mielóide aguda, leucemia aguda não-linfoblástica, leucemias linfoblásticas agudas, leucemia linfocítica aguda, eritroleucemia, crises blásticas da leucemia mieloide crónica, linfomas histiocíticos difusos (linfomas não-Hodgkin de elevada malignidade), leucemia meníngica e neoplasmas meníngicos11.
Posologia
A quimioterapia intratecal deve idealmente ser prescrita num contexto de ensaios clínicos ou protocolos estabelecidos, e apenas por clínicos com experiência no tratamento de neoplasias hematológicas. A dose intratecal não deve ser calculada com base na área de superfície corporal (BSA). As crianças com menos de 3 anos de idade recebem habitualmente doses de 50 mg três vezes por semana no caso de meningite leucémica. Embora tenham sido utilizadas doses até 100 mg, como a incidência de efeitos secundários tóxicos são dose dependentes, a utilização de doses relativamente elevadas deve ser efetuada com cautela. Como alternativa devem ser considerados esquemas de citarabina e metotrexato11.
A duração do tratamento é variável com a situação clínica e com o protocolo seguido pelo médico.
Observações
Os principais efeitos indesejáveis da citarabina são de ordem hematológica. A mielossupressão manifesta-se por megaloblastose, reticulocitopenia, trombocitopenia e anemia. Parecem ser mais evidentes após doses elevadas e perfusões contínuas; a gravidade depende da dose de fármaco e esquema de administração11.
Podem ocorrer náuseas e vómitos, geralmente mais frequentes após administração I.V. rápida do que I.V. contínua. Podem ainda ocorrer outros sintomas como diarreia, anorexia, inflamação ou ulceração oral e anal11.
Iodixanol
Iodixanol é um agente de contraste não-iónico, hidrofílico, dimérico e iso-osmolar. Tem a mesma eficácia diagnóstica que os outros meios de contraste iodados, sendo esperado que os efeitos adversos produzidos tenham menor incidência que os demais contrastes. Estudos farmacodinâmicos indicaram que iodixanol tem baixos efeitos cardiovasculares, causa menos danos a nível renal e é associado a menos alterações na barreira hematoencefálica e nas funções neurológicas do que os outros meios de contrastes não iónicos12.
Em Portugal, o iodixanol é comercializado na forma de solução injetável. Está disponível com o nome comercial de “Visipaque® 270” e “Visipaque® 320”, com 270 e 320 mg de I/mL, respetivamente4.
Indicações
Este medicamento é apenas para uso em diagnóstico. É utilizado em adultos como meio de contraste radiológico para cardioangiografia, angiografia cerebral convencional, arteriografia periférica convencional, angiografia abdominal, urografia, venografia e tomografia axial computorizada (TAC). É, ainda, utilizado em mielografia lombar, torácica e cervical, artrografia, histerosalpingografia (HSG) e estudos do trato gastrointestinal.
Em crianças está indicado para cardioangiografia, urografia, TAC e estudos do trato gastrointestinal13.
Posologia
A dosagem pode variar dependendo do tipo de exame, da idade, do peso, do rendimento cardíaco, do estado geral do doente e da técnica utilizada. Normalmente, é usada a mesma concentração e volume aproximados de iodo que se utilizam com outros meios de contraste radiológico iodados utilizados atualmente, embora tenha sido igualmente obtida informação diagnóstica adequada em diversos estudos realizados com o iodixanol injetável com concentração inferior de iodo. Na tabela 3, estão expressas dosagens que podem servir como guia para a administração intratecal de iodixanol. As doses para idosos são iguais às dos adultos13.
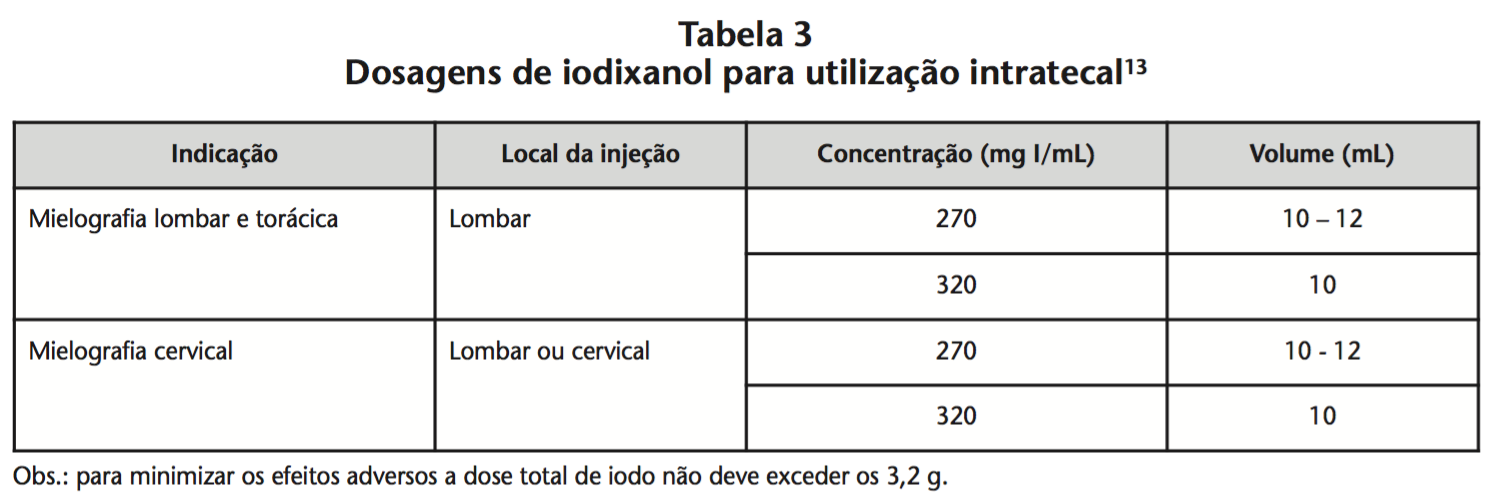
Observações
Uma história clínica de alergia, asma ou reações adversas aos meios de contraste iodados, indica a necessidade de cuidados especiais. A pré-medicação com corticosteroides ou com antagonistas dos recetores de histamina H1 e H2 pode ser considerada nestes casos13.
O risco de reações graves relacionadas com o uso de Visipaque é considerado mínimo. No entanto, os meios de contraste iodados podem provocar reações anafiláticas ou outras manifestações de hipersensibilidade13.
Após administração do meio de contraste, o doente deverá ser observado, pelo menos, durante 30 minutos, uma vez que a maioria dos efeitos secundários graves ocorre durante esse período13.
A seguir à mielografia o doente deverá ficar deitado com a cabeça e o tórax elevados a 20º durante 1 hora. A seguir o doente poderá deslocar-se cuidadosamente evitando baixar a cabeça. A cabeça e o tórax deverão ficar elevados durante as 6 horas seguintes se permanecer deitado. Doentes com suspeita de baixo limiar convulsivo deverão ficar em observação durante esse período. Doentes externos nunca deverão ficar completamente sozinhos durante as primeiras 24 horas13.
Os efeitos indesejáveis associados à utilização de Visipaque são normalmente ligeiros a moderados e de natureza transitória. É extremamente raro haver reações graves, tais como a morte13.
As reações de hipersensibilidade apresentam-se como sintomas cutâneos ou respiratórios moderados, tais como dispneia, erupção, eritema, urticária, prurido, reações cutâneas graves, edema angioneurótico, hipotensão, febre, edema laríngeo, broncoespasmo ou edema pulmonar13.
Não há antídoto específico, o tratamento da sobredosagem é sintomático13.
Iopamidol
Iopamidol é um composto não iónico iodado utilizado como meio de contraste14.
Está disponível em Portugal sob o nome comercial “Iopamiro® 300”, na concentração de 612,4 mg/ mL4.
Indicações
Este medicamento é apenas para uso em diagnóstico, nomeadamente em neuroradiologia (mieloradoculografia, cisternografia e ventriculografia), em angiografia (arteriografia cerebral, arteriografia visceral selectiva, arteriografia periférica e flebografia), em urografia (urografia intravenosa) e em outros tipos de investigações (potencialização do contraste em tomografia computorizada, artrografia e fistulografia)14.
Posologia
Em neurorradiologia, nos exames de cisternografia e ventriculografia a dose aconselhada vai de 3 a 10 ml, nos exames de mieloradoculografia a dose aconselhada vai de 5 a 10 ml14.
Em angiografia, nos exames de arteriografia cerebral a dose é de 5 a 10 ml por toma, nos exames de arteriografia visceral selectiva e arteriografia periférica a dose varia conforme a exploração e nos exames de flebografia a dose é de 30 a 50 ml14.
Em urografia, a dose aconselhada para este tipo de exame é de 30 a 50 ml14.
Outros tipos de investigações: em exames de potencialização do contraste em tomografia computorizada a dose é de 0,5-2,0 ml/kg; em exames de artrografia e fistulografia a dose varia consoante a exploração14.
Observações
Uma história clínica de alergia, asma ou reação de intolerância associada a exames do mesmo tipo realizados anteriormente, implica a necessidade de adoptar medidas de precaução adicionais, devendo o benefício compensar largamente o risco que correm os doentes nessa situação. Devem ser disponibilizadas de imediato medidas de ressuscitação adequadas14.
O exame de raios-X em mulheres, se possível, deve ser efectuado durante a fase de pré-ovulação do ciclo menstrual e deve ser evitado durante a gravidez14.
Durante a realização de exames a crianças ou bebés, não se deve limitar a ingestão de fluidos antes da administração da solução de contraste hipertónica. Alterações no equilíbrio hidro-electrolítico devem ser corrigidas antes da utilização14.
Os doentes com insuficiência hepato-renal grave não devem ser examinados, a menos que seja absolutamente necessário. Os doentes só devem ser re-submetidos a um novo exame ao fim de 5-7 dias14.
O iopamidol deve ser administrado com precauções especiais em doentes idosos, em doentes com pressão intracraneana elevada ou no caso de suspeita de um tumor intracraneano, abcesso ou hematoma e nos doentes com história de epilepsia, doença cardiovascular grave, insuficiência renal, alcoolismo crónico ou esclerose múltipla. Doentes nestas condições têm um risco aumentado de complicações neurológicas14.
Deve ser utilizado com precaução em doentes com hipertiroidismo. É possível ocorrer recorrência de hipertiroidismo em doentes previamente tratados para a doença de Graves14.
Metotrexato
O metotrexato é um antagonista do ácido fólico. O metotrexato inibe de forma reversível a dihidrofolato reductase, enzima que reduz o ácido fólico a ácido tetrahidrofólico.
O metotrexato pode ser administrado por via intramuscular, intravenosa, intra-arterial ou intratecal4. O medicamento encontra-se em Portugal sob diversas marcas comerciais, estando disponível para administração intratecal em ampolas de 2,5 mg/mL e 25 mg/mL4.
Indicações
O metotrexato tem indicação para o tratamento da leucemia aguda, sobretudo das leucemias linfoblásticas agudas, linfomas malignos não-Hodgkin de alto e médio grau de malignidade, doença de Hodgkin refractária, certas formas de micose fungóide, coriocarcinoma e noutros tumores do trofoblasto e ainda, na terapêutica de tumores das células germinais do ovário, tratamento do cancro da mama, do pulmão, da bexiga, nos carcinomas epidermóides da cabeça e do pescoço e do sarcoma estrogénico. Relativamente às doenças não neoplásicas é muito útil no controlo da psoríase, na terapêutica da artrite reumatóide e, ainda, na profilaxia das doenças enxerto-versus-hospedeiro, nos transplantes da medula óssea15.
Posologia
A maioria das dosagens são dadas em mg/kg mas podem ser convertidas em doses relacionadas com a área corporal (mg/m2), através da utilização de factores de conversão, que variam com a idade e respectivo tipo somático do doente15.
A posologia e o método de administração do metotrexato variam com o protocolo de tratamento utilizado. As posologias seguintes são indicadas como referência, devendo o médico consultar os protocolos para as dosagens de metotrexato e outros agentes antineoplásicos15.
Na terapêutica da meningite leucémica é administrado por via intratecal, na dose de 0,2 a 0,5 mg/kg. A administração é feita a intervalos de tempo de 2-5 dias e é repetida, a maior parte das vezes, até que o número de células do LCR seja normal15.
O metotrexato, quando administrado por via intratecal pode ocasionar toxicidade neurológica e sistémica15.
Nos idosos usam-se os esquemas posológicos usuais, mas o metotrexato deve ser usado com muito cuidado nesta faixa etária devido à sua toxicidade15.
Observações
A excreção de metotrexato é incompleta e a acumulação ocorre mais rapidamente, nos doentes com função renal diminuída15.
O metotrexato é excretado primariamente pelos rins. O seu uso na presença de função renal insuficiente pode resultar em acumulação de quantidades tóxicas ou mesmo de dano renal adicional15.
O metotrexato tem como efeito indesejável frequente a supressão hematopoiética, que pode ocorrer repentinamente, mesmo com uma dosagem aparentemente segura do fármaco, por esta razão é imperiosa a realização de estudos hematológicos antes e durante o tratamento15. Os doentes submetidos ao tratamento com metotrexato deverão estar sob avaliação clínica constante e monitorização apropriada15.
O metotrexato mostrou ser teratogénico, tendo causado morte fetal e/ou anomalias congénitas15. Não utilizar metotrexato em mulheres grávidas ou que possam vir a engravidar15.
Morfina
A nível do sistema nervoso central, a morfina tem uma ação analgésica dose-dependente. Pode actuar sobre o comportamento psicomotor e provocar, consoante a dose e o doente, sedação ou excitação16.
A morfina, mesmo em concentrações terapêuticas, exerce no centro respiratório e no centro da tosse, uma ação depressora. O efeito depressor respiratório é atenuado pela administração crónica16.
A nível da musculatura lisa a morfina diminui o tónus e o peristaltismo das fibras longitudinais e aumenta o tónus das fibras circulares, provocando um espasmo dos esfíncteres (pilórico, válvula ileocecal, esfíncter anal, esfíncter de Oddi, esfíncter vesical)16.
A morfina está disponível no mercado português em diversas formas farmacêuticas. Em solução injetável para via intratecal, é comercializada em Portugal por diversos laboratórios, estando disponível nas formas de 10 mg/mL, 20 mg/mL, 20 mg/2mL e 40 mg/2mL4. Esta via exige que a morfina seja usada sem conservantes e que seja filtrada antes da injeção através de um filtro de 0,22 μm (para prevenir uma eventual contaminação após a abertura da ampola)16.
Indicações
Dores intensas e/ou resistentes a analgésicos mais fracos16.
Posologia
Por via intratecal, em adultos: 0,1 a 0,3 mg cada 12 a 24 horas16. Na tabela 4 está representada a equivalência posológica entre as diferentes vias de administração16.
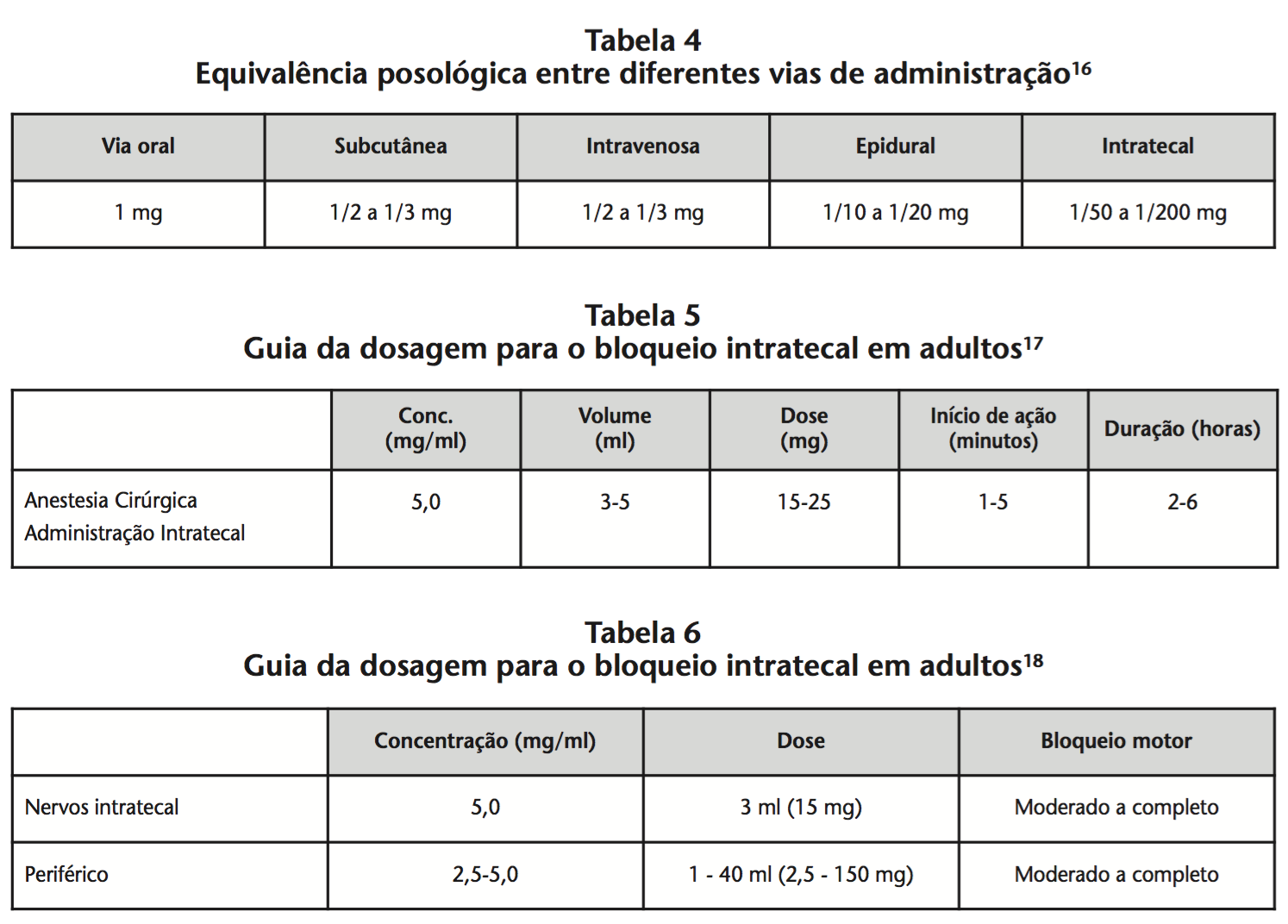
Observações
Os efeitos indesejáveis mais comuns após o início do tratamento são sonolência, confusão, náuseas e vómitos16.
A sonolência é um sinal de alerta precoce do início de uma descompensação respiratória16.
Está contra-indicada a sua utilização em caso de: hipersensibilidade à morfina ou a qualquer um dos excipientes; insuficiência respiratória descompensada (na ausência de ventilação artificial); insuficiência hepatocelular grave (com encefalopatia); situações agudas: traumatismo craniano e hipertensão intracraniana na ausência de ventilação controlada; epilepsia não controlada; associação com buprenorfina, nalbufina e pentazocina; aleitamento, no caso de iniciação ou continuação de um tratamento a longo prazo após o nascimento16.
Contra-indicações associadas às vias epidural e intratecal: problemas de hemostase no momento da injeção; infeções cutâneas locais, regionais ou generalizadas, em evolução; hipertensão intracraniana evolutiva16.
Ropivacaína
O perfil de reações adversas da ropivacaína é semelhante ao de outros anestésicos locais de ação prolongada de tipo amida17.
Está disponível em Portugal sob o nome comercial “Naropeine®” em ampolas de 5 mg/mL4.
A ropivacaína é um anestésico local de longa ação de tipo amida que exerce efeitos tanto anestésicos como analgésicos. Em doses elevadas, produz anestesia cirúrgica, enquanto que em doses mais baixas produz bloqueio sensorial com bloqueio motor limitado e não progressivo17.
Indicações
Está indicado para administração intratecal em anestesia cirúrgica17.
Posologia
Na tabela 5 constitui um guia da dosagem para o bloqueio intratecal em adultos. Deve utilizarse a dose mínima necessária para obter um bloqueio eficaz. A experiência do clínico e o conhecimento do estado físico do doente são importantes para decidir a dose17.
As doses na tabela são as consideradas necessárias para produzir um bloqueio eficaz e devem ser entendidas como linhas de orientação para utilização em adultos. Podem ocorrer variações individuais no início da ação e na duração17. A nível da população pediátrica a administração intratecal não foi investigada em recém-nascidos, bebés ou crianças17.
Observações
Pode ocorrer o bloqueio espinal total se for administrado uma elevada dose intratecal17.
A principal característica da ropivacaína é a sua longa duração de ação17.
Naropeine® 5 mg/ml não contém conservantes e destina-se exclusivamente para uma única utilização. Deve rejeitar-se qualquer solução não utilizada17.
Levobupivacaína
A levobupivacaína é um anestésico e analgésico local de ação prolongada. Bloqueia a condução nervosa nos nervos sensitivos e motores, em grande parte por interação com os canais de sódio da membrana celular dependentes da voltagem, mas bloqueia também os canais de potássio e cálcio18.
A levobupivacaína interfere também com a transmissão do impulso nervoso e com a condução em outros tecidos, sendo os efeitos a nível do sistema cardiovascular e sistema nervoso central os mais importantes para a ocorrência de reações adversas clínicas18.
Está disponível em Portugal sob o nome comercial “Chirocaine®” e “Levobupivacaína Normon®” em ampolas de 25 mg/10 ml, 50 mg/10 ml e 75 mg/10 ml4.
Indicações
Utilizado para anestesia cirúrgica, em grande cirurgia, por exemplo no bloqueio epidural (incluindo para cesarianas), intratecal e de nervos periféricos e em pequena cirurgia, por exemplo para infiltração local, bloqueio peribulbar em cirurgia oftalmológica. Em gestão da dor por perfusão epidural contínua, administração única ou múltipla de bólus epidural, especialmente no pós-operatório ou analgesia no trabalho de parto18.
Posologia
As doses para administração intratecal estão representadas na tabela 6.
Observações
A administração de anestésicos locais pela via de administração intratecal ou epidural no sistema nervoso central, em doentes com doenças pré-existentes do SNC, pode exacerbar potencialmente algumas destas situações clínicas. Consequentemente, deve proceder-se a uma avaliação clínica quando se considerar uma anestesia epidural ou intratecal nesses doentes18.
As reações adversas mais frequentemente descritas são hipotensão, náuseas, anemia, vómitos, tonturas, cefaleias, pirexia, dor resultante da técnica anestésica, dor lombar e síndrome de sofrimento fetal quando usado em obstetrícia18.
A injeção intratecal acidental de anestésicos locais pode originar uma anestesia espinal muito alta18.
CONCLUSÃO
Tendo em vista a relevância da administração intratecal de medicamentos na área da saúde, o INFARMED, como autoridade nacional do medicamento em Portugal, concedeu AIM para os seguintes fármacos que podem ser administrados pela via referida: baclofeno, morfina, bupivacaína, levobupivacaína, ropivacaína, metotrexato, citarabina, iopamidol e iodixanol. A administração intratecal dos referidos princípios ativos vem tornar possível a obtenção de uma eficiente ação antiespática, analgésica e anestésica, com as vantagens de um rápido início de ação, ausência de bloqueio motor, baixa exposição fetal e diminuição dos efeitos secundários sistémicos. Torna também possível a administração, com as mesmas vantagens, de medicamentos que atuam como meios de contraste para diagnóstico, imunomoduladores e antineoplásicos, conduzindo a uma maior eficácia e segurança na sua utilização.
Conflito de interesses: Os autores declaram não haver conflitos de interesse.
BIBLIOGRAFÍA
1. Rojas H, Ritter C, Pizzol FD. Mechanism of dysfunction of the blood-brain barrier in critically ill patients: emphasis on the role of matrix metalloproteinases. Revista Brasileira de Terapia Intensiva. 23:2(2011)222-227.
2. Loch-Neckel G, Koepp J. The blood-brain barrier and drug delivery in the central nervous system. Rev Neurol. 2010 Aug;51(3):165-74.
3. Decreto Lei n.º 46/2012. D.R. I Série. 40 (24-02-12) 884-890.
4. Autoridade Nacional do Medicamento e Produtos de Saúde (INFARMED) – Base de Dados de Medicamentos de Uso Humano (INFOMED). Lisboa: INFARMED. [Consult. 29 julho de 2015]. Disponível em WWW. <URL: http://www.infarmed.pt/infomed/inicio.php>.
5. Autoridade Nacional do Medicamento e Produtos de Saúde (INFARMED) – Prontuário Terapêutico Online. Lisboa: INFARMED. [Consult. 29 julho 2015]. Disponível em WWW. <URL: http://www.infarmed.pt/prontuario/frameprimeiracapitulos.html>.
6. Penn RD, Kroin JS. Continuous intrathecal Baclofen for severe spasticity. Lancet. 2:1(1985)125-127.
7. Resumo das Características do Medicamento Lioresal Intratecal® (baclofeno), Novartis Farma, aprovado em 14 de julho de 2014.
8. Nogueira CS, Lima LC, Paris, VC Neiva, PM Otani ET, Couceiro RO, et al. A Comparative Study between Bupivacaine (S75-R25) and Ropivacaine in Spinal Anesthesia for Labor Analgesia. Revista Brasileira de Anestesiologia. 60:5(2010)484-494.
9. Resumo das Características do Medicamento Marcaína Espinal Pesada® (bupivacaína), AstraZeneca, aprovado em 16 de fevereiro de 2007.
10. Imbelloni LE, Beato L. Comparação entre Bupivacaína Racêmica (S50-R50) e Mistura Enantiomérica de Bupivacaína (S75-R25), ambas Isobáricas, a 0,5% em Raquianestesia. Estudo em Cirurgias Ortopédicas. Revista Brasileira de Anestesiologia. 51:5(2001)369-376.
11. Resumo das Características do Medicamento Citaloxan® (citarabina), Hospira, aprovado em 26 de maio de 2014.
12. Spencer CM, Goa KL. Iodixanol: A Review of its Pharmacodynamics and Pharmacokinetic Properties and Diagnostic Use as an x-Ray Contrast Medium. Drugs. 52:6(1996)899-927.
13. Resumo das Características do Medicamento Visipaque® (iodixanol), Satis-Radioisótopos e Protecções Contra Sobretensões Eléctricas Unipessoal, Lda., aprovado em 5 de novembro de 2013.
14. Resumo das Características do Medicamento Iopamiro® (iopamidol), Bracco Imaging, S.p.A., aprovado em 11 de setembro de 2009.
15. Resumo das Características do Medicamento Fauldexato® (metotrexato), Hospira, aprovado em 14 de julho de 2014.
16. Resumo das Características do Medicamento Morfina Basi® (morfina), Laboratórios Basi, aprovado em 30 de maio de 2014.
17. Resumo das Características do Medicamento Naropeine® (ropivacaína), AstraZeneca, aprovado em 26 de novembro de 2013.
18. Resumo das Características do Medicamento Chirocaine® (levobupivacaína), Abbvie, aprovado em 19 de setembro de 2013.
____
Descargar documento PDF: Medicamentos com autorização de introdução no mercado em Portugal que podem ser administrados por via intratecal: indicações, posologia e observações
