Fecha de recepción: 21/12/2017 – Fecha de aceptación: 05/03/2018
Martín Blas C1, Díez Fernández R1, Chica Gullón E2, Sánchez-Rubio Ferrández J1
1 Servicio de Farmacia
2 Servicio de Hematología
Hospital Universitario de Getafe. Madrid (España)
____
Correspondencia:
Cristina Martín Blas
Hospital Universitario de Getafe
(Servicio de Farmacia)
Ctra. Toledo Km. 12,500 s/n
28905 Getafe (Madrid)
Correo electrónico: cmblas@salud.madrid.org
____
RESUMEN
La trombocitopenia primaria inmune (TPI) es un trastorno autoinmune caracterizado por la destrucción plaquetaria y trombopoyesis anormal, asociados a la presencia de auto-anticuerpos que desializan las glicoproteínas de superficie de las plaquetas GP Ib/IX y/o GP IIb/IIIa. Oseltamivir actúa como inhibidor selectivo de sialidasas y se piensa que podría ser utilizado en estos pacientes. Se describe un caso de una mujer de 68 años, con psoriasis crónica y TPI refractaria a diferentes tratamientos (corticoides, inmunoglobulina intravenosa, rituximab, esplenectomía y análogos de los receptores de la trombopoyetina (TPO-RA)), en la que se utilizó oseltamivir (75 mg cada 12 horas durante 4 semanas) en combinación con romiplostim y corticoides a dosis intermedias consiguiendo respuesta de hasta 184×103/µL plaquetas, mantenida con recuentos en rango normal durante 42 días. Posteriormente, un segundo ciclo de 3 semanas de duración con oseltamivir no indujo respuesta. El estudio plaquetario del paciente mostraba sólamente una discreta mejoría en la pérdida de ácido siálico tras 14 días de tratamiento con oseltamivir. Por otro lado, el suero del paciente no producía desialización de plaquetas control, lo que puede sugerir que no existieran anticuerpos antiGPIb/IX de superficie plaquetaria en este paciente, indicando que oseltamivir puede no ser una terapia válida para este perfil de pacientes.
Palabras clave: Oseltamivir, trombocitopenia primaria inmune, sialidasa.
____
INTRODUCCIÓN
La trombocitopenia primaria inmune (TPI) es un trastorno autoinmune caracterizado por la destrucción plaquetaria y trombopoyesis anormal, asociados a la presencia de auto-anticuerpos contra la glicoproteína de superficie plaquetaria GP Ib/IX y/o GP IIb/IIIa. Algunos estudios sugieren la asociación de anticuerpos contra GPIb/IX con trombocitopenia severa al inducir desialización de glicoproteínas de membrana, lo que se relaciona con una mayor destrucción hepática de plaquetas. Por ese motivo, la TPI podría ser tratada con inhibidores de sialidasa1 como oseltamivir, un inhibidor selectivo de sialidasas del virus influenza A y B. Se han descrito varios casos de pacientes refractarios al tratamiento convencional en los que se utilizan inhibidores de neuraminidasa.
CASO CLÍNICO
Paciente de 68 años, con psoriasis crónica, diagnosticada de TPI en 2009. Se inicia tratamiento de primera línea con corticoides e inmunoglobulinas intravenosas (IGsIV). Se realiza tratamiento erradicador para Helicobacter pylori, sin que esto modifique la cifra de plaquetas. Dado que no hay buena respuesta, se opta por otros tratamientos (Figura 1): 2 ciclos de rituximab (375 mg/m2 semanalx4) y esplenectomía, con buena respuesta hasta el siguiente episodio, coincidiendo con un brote psoriásico y el inicio de tratamiento con retinoides (acitretina sólo dos días); análogos de los receptores de la trombopoyetina (TPO-RA), eltrombopag y romiplostim hasta dosis máximas, e incluso, tratamiento combinado, siempre asociando tratamientos de rescate tras múltiples reagudizaciones.
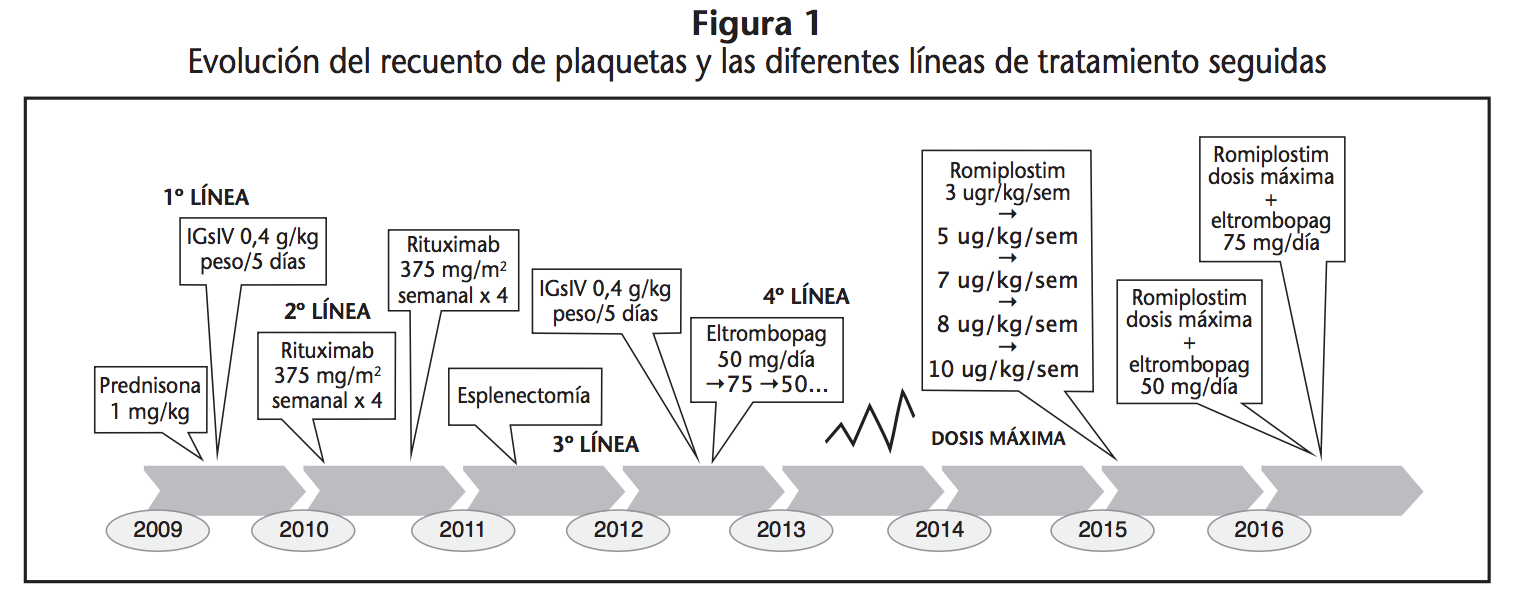
Dada la multirrefractariedad al tratamiento, y descartando la existencia de posibles interacciones con su medicación o una adherencia subóptima, se solicita la utilización de oseltamivir como tratamiento fuera de indicación. En junio de 2016, en base a información encontrada en la literatura biomédica, se inicia tratamiento con oseltamivir 75 mg cada 12 horas (Figura 2).
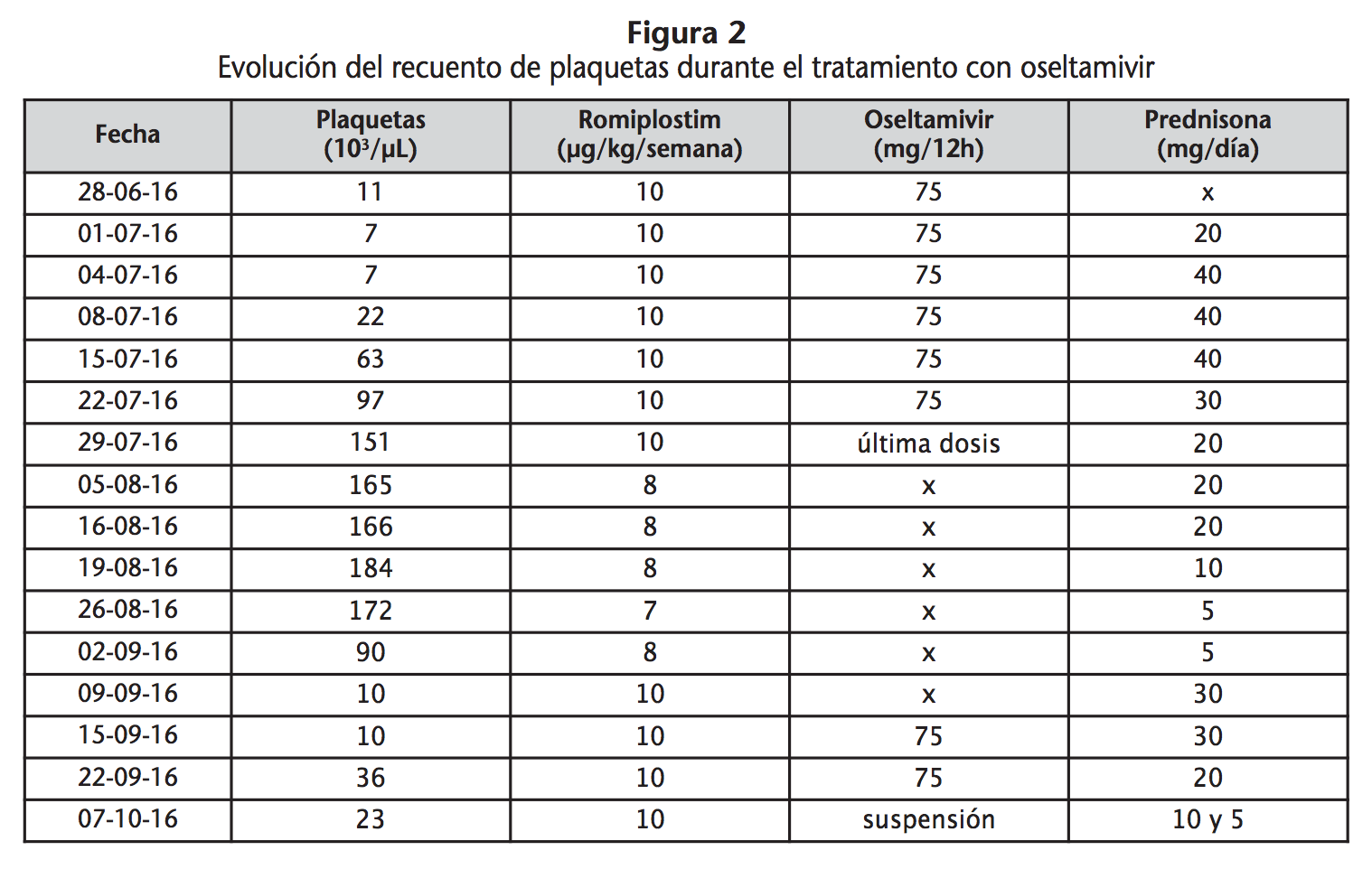
Simultáneamente se realiza un estudio de activación plaquetaria, grado de desialización y expresión de glicoproteínas de membrana para averiguar si la paciente se pudiera beneficiar de tratamiento con oseltamivir. El ensayo de expresión de unión de lectina-RCA, que estudia la desialización de las plaquetas, mostró una discreta mejoría en la pérdida de ácido siálico tras 14 días de tratamiento con oseltamivir. Se vio un tamaño plaquetario inicial aumentado con una mayor expresión de granulosfisina y selectina P, de glicoproteínas de membrana, principalmente GPIba y una desialización ligeramente aumentada. No se objetiva una clara desialización pero a pesar de ello, el centro de referencia recomienda mantener la pauta hasta alcanzar las 4 semanas de tratamiento. El ensayo del suero del paciente con plaquetas control no producía desialización de éstas. La respuesta alcanzada fue de 151×103 plaquetas/µL al mes de tratamiento simultáneo con oseltamivir, romiplostim y corticoides a dosis intermedias.
Tras suspensión del oseltamivir y los corticoides, la cifra de plaquetas alcanza 184×103/µL, pero los recuentos caen drásticamente apareciendo un nuevo bache trombopénico severo con 10×103 plaquetas/µL (42 días después de la suspensión de oseltamivir, manteniendo romiplostim a 8 µg/Kg/semana y prednisona a 5 mg/día).
Posteriormente, se intenta otro ciclo de tratamiento con oseltamivir durante un periodo de 3 semanas, pero esta vez sin respuesta, por lo que se suspende.
DISCUSIÓN DEL CASO
Se ha demostrado que el hígado y el bazo son lugares críticos de aclaramiento de plaquetas en TPI. El secuestro hepático de plaquetas aumenta significativamente en pacientes con TPI esplenectomizados. Diferentes estudios en pacientes y modelos murinos han sugerido la asociación de auto-anticuerpos contra GPIb/IX con trombocitopenia severa2. Un reciente estudio de un modelo murino sugirió que estos anti- anticuerpos pueden inducir desialización de plaquetas1,3. La desialización de las plaquetas consiste en la escisión del ácido siálico terminal de las glicoproteínas de superficie produciéndose la exposición de residuos de beta-galactosa que son reconocidos por los receptores Ashwell-Morell hepáticos. Las plaquetas desializadas son fagocitadas por los hepatocitos y es muy posible que esta desialización contribuya a una mayor destrucción de plaquetas. Es una destrucción independiente de la unión al fragmento Fc del anticuerpo, y puede influir en la respuesta con ciertas terapias4.
Oseltamivir actúa como inhibidor selectivo de enzimas neuraminidasas (sialidasas) del virus influenza A y B. Estas enzimas escinden moléculas de ácido siálico, involucradas en la entrada del virus y la liberación de viriones. Se ha descrito que oseltamivir puede reducir tanto la actividad neuraminidasa de los virus como la sialidasa homóloga humana5, de modo que se evitaría la destrucción hepática de las mismas.
Existen pocos casos publicados de tratamiento de TPI con oseltamivir. Tres de ellos hacen referencia a una elevación de plaquetas tras 5 días de tratamiento con oseltamivir 75 mg cada 12 horas en pacientes con TPI que presentaban síntomas de la gripe6-8. El último caso, con una TPI refractaria a corticoides, IGsIV, TPO-RA y rituximab, presentaba una desialización muy incrementada y consiguió una respuesta mantenida después 6 meses8. Un reciente estudio, en el que se utilizó oseltamivir junto con TPO-RA, refiere aumento del recuento de plaquetas tras varios ciclos de tratamiento y una ligera mejoría en el grado de sialización9.
En nuestro caso, la combinación inicial de romiplostim y oseltamivir normalizó el recuento de plaquetas y permitió la reducción de dosis del TPO-RA e incluso la suspensión del tratamiento corticoideo. Una vez suspendido el oseltamivir, se consiguió respuesta mantenida durante 42 días hasta un nuevo bache trombopénico, debido también en parte al descenso de dosis de prednisona. Según reporta Crook et al., en estados trombopénicos la medula ósea intenta mantener la hemostasia y produce mayor proporción de plaquetas con mayor tamaño y con mayor grado de sialización10. Tras los 14 días, este tamaño se vio disminuido, debido a que probablemente la vida media de las plaquetas era mayor por el menor grado de destrucción periférica. Por otro lado, que el suero del paciente no indujera desialización de plaquetas control puede sugerir la inexistencia de anticuerpos anti GP de superficie plaquetaria, no analizados en práctica habitual. Todo esto puede sugerir que la terapia no es válida para este perfil de pacientes.
Son necesarios más estudios para evaluar el uso de oseltamivir en pacientes TPI refractarios y seleccionar biomarcadores que permitan identificar qué pacientes se pueden beneficiar de esta terapia.
Agradecimientos: Dra. María Luisa Lozano, Hematóloga del Hospital Morales Messenger de Murcia.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
BIBLIOGRAFÍA
1. Van Der Wal E, Li J, Zhu G, Vadasz,B, Ma L, Yougbare I. Anti-GPIb antibody induces platelet desialylation: a novel mechanism of Fc-independent immune thrombocytopenia, and a potential new diagnosis and therapy against refractory ITP. J Int Soc Thromb Haemost. 2013;11:204-5.
2. Hou M, Stockelberg D. Antibodies against platelet GPIb/IX, GPIIb/IIIa, and other platelet antigens in chronic idiopathic thrombocytopenic purpura. Eur J Haematol. 1995;55(5):307-14.
3. van Der Wal DE, Zhu G, Li J, Vadasz, B, Issaka Y, Lang S. Desialylation: A Novel Platelet Clearance Mechanism and a Potential New Therapeutic Target in Anti-GPIb Antibody Mediated Thrombocytopenia. Blood (ASH Annu Meet Abstr. 2012;120(21):265.
4. Qiu J, Liu X, Li X, Zhang X, Han P, Zhou H, et al. CD8+ T cells induce platelet clearance in the liver via platelet desialylation in immune thrombocytopenia. Sci Rep [Internet]. Nature Publishing Group; 2016;6 (January): 27445.
5. Li CY, Yu Q, Ye ZQ, Sun Y, He Q, Li XM, et al. A non synonymous SNP in human cytosolic sialidase in a small Asian population results in reduced enzyme activity: potential link with severe adverse reactions to oseltamivir. Cell Res. 2007;17:357-62.
6. Alioglu B, Tasar A, Ozen C, Selver B, Dallar Y. An Experience of Oseltamivir Phosphate (TamifluTM) in a Pediatric Patient with Chronic Idiopathic Thrombocytopenic Purpura: A Case Report. Pathophysiol Haemost Thromb. [Internet]. 2010;10-3.
7. Bigot P, Auffret M, Gautier S, Weinborn M, Ettahar N-K, Coupé P. Unexpected platelets elevation in a patient with idiopathic thrombocytopenia treated with oseltamivir for influenza infection. Fundam Clin Pharmacol. [Internet]. 2016;30(5):483-5.
8. Shao L, Wu Y, Zhou H, Qin P, Ni H, Peng J, et al. Successful treatment with oseltamivir phosphate in a patient with chronic immune thrombocytopenia positive for anti-GPIb/IX autoantibody. Platelets [Internet]. Informa UK Ltd; 2014;0(0):1-3.
9. Álvarez-Román MT, Pollmar MIR., Bernardino JI, Lozano ML, Martín-Salces M, Fernández-Bello I. Thrombopoietin receptor agonists in conjunction with oseltamivir for immune thrombocytopenia. AIDS. 2016;30(7):1141-2.
10. Crook M, Chin MA CN. Electrokinetic properties and surface membrane siálico acid status of platelets in idiopathic thrombocytopenic purpura (ITP). Br J Haematol. 1991;77:209-14.
____
Descargar artículo en PDF: Oseltamivir en paciente con trombocitopenia primaria inmune refractaria
