Rev. OFIL 2017, 27;4:341-345
Fecha de recepción: 02/02/2017 – Fecha de aceptación: 29/03/2017
Díaz Rangel M, Lerma Gaude V, Domingo Chiva E, Sánchez Rubio F, Monteagudo Martínez N, Marco del Río J
Servicio de Farmacia Hospitalaria. Gerencia de Atención Integrada de Albacete (España)
____
Correspondencia:
Marca Díaz Rangel
Complejo Hospitalario Universitario de Albacete
C/Hermanos Falcó, 37
02008 Albacete
Correo electrónico: marca_dr@hotmail.com
____
Resumen
Objetivos: Analizar la utilización, efectividad y seguridad de pirfenidona en el tratamiento de fibrosis pulmonar idiopática.
Métodos: Estudio observacional retrospectivo en un hospital terciario. Se incluyeron los pacientes en tratamiento con pirfenidona entre diciembre 2012 y abril 2015. Se recogieron datos demográficos y clínicos.
Resultados: Se incluyeron 11 pacientes con fibrosis pulmonar idiopática leve-moderada. Los efectos adversos más frecuentes fueron: fotosensibilidad (45,5%), anorexia (36,4%) y astenia (36,4%). Se suspendió el tratamiento por toxicidad en dos pacientes. De los datos disponibles de efectividad se observó que la capacidad vital forzada en unos pacientes aumentó y en otros disminuyó. El porcentaje de pacientes con una disminución en la capacidad vital forzada no superior al 10% ni muerte fue del 63,6% en la semana 24 y del 54,5% en la semana 52.
Conclusiones: La utilización de pirfenidona ha sido adecuada a recomendaciones, salvo que el diagnóstico, por la dificultad del mismo, en algunos casos fue determinado como posible o probable. La efectividad de pirfenidona se considera moderada en la disminución del deterioro pulmonar y el perfil de seguridad y tolerabilidad según nuestros datos es aceptable. No obstante, se necesita mayor número de pacientes y un seguimiento más completo de los mismos para obtener conclusiones más sólidas.
Palabras clave: Pirfenidona, fibrosis pulmonar idiopática, seguridad, efectividad.
____
INTRODUCCIÓN
La fibrosis pulmonar idiopática (FPI) se define como una neumonía intersticial fibrosante crónica, limitada al pulmón, asociada al patrón radiológico y/o histológico de la neumonía intersticial usual (NIU)1. Es una enfermedad rara y progresiva de etiología desconocida que carece de un tratamiento curativo. La mediana del tiempo de supervivencia para los pacientes con FPI es alrededor de 3 años, su tasa de mortalidad es mayor que la de la mayoría de los tipos de cáncer2. La incidencia estimada de esta enfermedad es de entre 4,6 y 7,4 por cada 100.000 habitantes y la prevalencia de 13/100.000 en mujeres y 20/100.000 en hombres. La prevalencia aumenta con la edad, siendo mayor en pacientes de 75 años3. Se calcula que actualmente esta enfermedad podría estar afectando a unas 7.500 personas en España1. La FPI cumple con los criterios de clasificación como enfermedad huérfana3.
La FPI es una NIU de difícil diagnóstico, el cual requiere la exclusión de otras entidades clínicas definidas o enfermedades parenquimatosas pulmonares difusas de causa conocida y la presencia de un patrón histológico de NIU en el examen del tejido pulmonar obtenido mediante biopsia pulmonar quirúrgica, o bien la evidencia radiológica de patrón NIU en la tomografía axial computarizada de alta resolución (TCAR), o ambas1. Se debe tener en cuenta la historia clínica detallada del paciente, que incluya factores ambientales como el tabaquismo (>20 paquetes/año) y la exposición al sílice, al latón, al acero, al plomo y al polvo de madera, las actividades laborales en ganadería y en agricultura, y la construcción de casas de madera, considerados factores de riesgo de esta enfermedad1. Los factores asociados a peor evolución de la enfermedad son: edad superior a 70 años; comorbilidades asociadas (hipertensión pulmonar, enfisema y carcinoma broncogénico); capacidad de transferencia pulmonar de monóxido de carbono (DLCO) basal <40%, descenso ≥10% de la capacidad vital forzada (CVF) y ≥15% de la DLCO (porcentaje del valor predicho) en 6-12 meses; en la prueba de la marcha de los 6 minutos (PM6M) saturación arterial periférica de oxígeno ≤88% y <200m4; y extensión de la fibrosis en la TCAR1.
Una característica de la manifestación patológica de esta enfermedad es la presencia de focos fibroblásticos en el pulmón fibrótico. El factor de crecimiento transformante beta (TGF-β) es un estimulador central de la producción de colágeno en la patogénesis de la fibrosis pulmonar. Además, el estrés oxidativo contribuye a la patogénesis de la FPI y puede colaborar con el TGF-β durante la progresión de la enfermedad5.
Durante años el tratamiento con glucocorticoides y/o azatioprina y/o N-acetilcisteína (NAC) ha sido considerado una opción de tratamiento, si bien en la actualidad no se recomienda su uso debido a su falta de eficacia demostrada en el estudio PANTHER6.
En estadios evolucionados de la FPI, el trasplante pulmonar es el único tratamiento que consigue una importante mejoría funcional e incremento de la supervivencia a 1, 5 y 10 años del 74%, 45% y 22%, respectivamente7.
Recientemente se han comercializado dos nuevos fármacos para FPI, pirfenidona y nintedanib, en 2014 y 2016 respectivamente. De esta manera, se abre un nuevo camino con respecto al tratamiento de esta patología. Estos fármacos han mostrado efectos positivos sobre la ralentización de la progresión de la enfermedad8.
Los primeros estudios clínicos prospectivos de pirfenidona han demostrado retardar el deterioro de la función pulmonar medida como el cambio en la CVF y la supervivencia libre de progresión (SLP)9,10.
Pirfenidona (5 metil-1-fenil-2-(1H) piridona) es un agente que combina efecto antiinflamatorio y antifibrótico, actuando sobre la regulación de la actividad del TGF-β5, de las vías del factor de necrosis tumoral alfa y beta y también sobre la oxidación celular11. Está indicado para el tratamiento de la FPI leve-moderada (CVF>50% Y DLCO>35%)8.
La utilización de medicamentos de reciente comercialización sin apenas estudios de seguridad post comercialización hace necesaria la estrecha monitorización de los pacientes que se encuentran en tratamiento en nuestros centros. De esta manera se persigue obtener el máximo beneficio clínico garantizando la mayor seguridad posible.
El presente estudio tiene como objetivo describir las condiciones de utilización, la efectividad y la seguridad de pirfenidona en el tratamiento de FPI en la práctica clínica habitual.
MÉTODOS
Estudio observacional retrospectivo que incluye los pacientes tratados con pirfenidona entre diciembre de 2012 y abril de 2015 en un hospital universitario de tercer nivel. Hasta la fecha de comercialización de pirfenidona en España el tratamiento de los pacientes incluidos fueron autorizados previamente por la Agencia Española del Medicamento.
Se recogieron datos demográficos (sexo, edad), exposiciones a distintos factores de riesgo de la enfermedad (exposición a distintos metales, aleaciones y/o polvo de madera; actividades laborales en ganadería, agricultura y/o en la construcción de casas de madera y tabaquismo), diagnóstico de FPI, tratamiento previo para FPI, tratamiento concomitante a pirfenidona, pauta posológica y duración del tratamiento con pirfenidona, parámetros de la función respiratoria, alteraciones hepáticas y efectos adversos (EA) del tratamiento, los cuales se clasificaron según la Common Terminology Criteria for Adverse Events version 4.012. Los parámetros de la función respiratoria estudiados fueron la CVF basal, a la semana 24 y 52; la DLCO basal y la PM6M basal. Las variables utilizadas para la evaluación de la efectividad fueron la CVF, medida como la diferencia entre situación basal y a la semana 24 y 52; y la SLP, esta última definida como tiempo hasta la muerte y/o disminución de ≥10% en los valores de CVF desde el inicio hasta la semana 24 y 52. Se define mortalidad como todas las muertes ocurridas durante el estudio, independientemente de que el paciente hubiera finalizado o no el tratamiento. El tipo de análisis de la efectividad se realiza por intención de tratar. Las fuentes de información para la recogida de datos fueron el programa informático Farmatools® y la historia clínica electrónica Mambrino XXI®. El tratamiento estadístico de los datos se realizó con el programa STATA® v.13.
RESULTADOS
Se incluyó en el estudio un total de 11 pacientes (5 hombres), con una mediana de edad de 74 años (rango 61-80). Las características generales de los pacientes con FPI se resumen en la tabla 1.
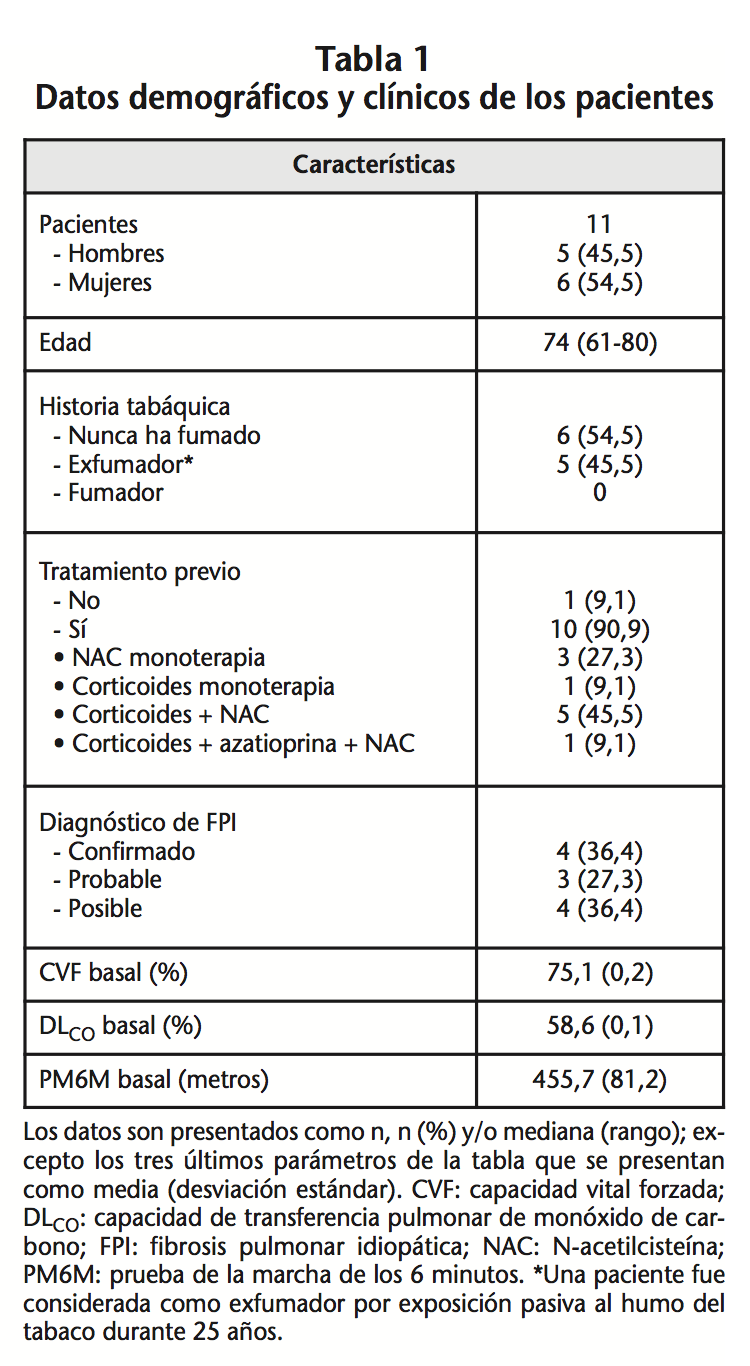 En cuanto a las exposiciones a factores de riesgo, el 36,4% de los pacientes había estado expuesto a metales, aleaciones y/o polvo de madera, el 18,2% trabajaba en ganadería, agricultura y/o construcción de casas de madera y el 45,5% eran exfumadores (una paciente estuvo expuesta de forma pasiva al humo del tabaco durante 25 años). El diagnóstico de FPI en el 36,4% de los pacientes estaba confirmado radiológicamente, en el 27,3% FPI probable y en el 36,4% FPI posible. El 90,9% de los pacientes había recibido tratamiento previo para FPI, el más frecuente NAC más corticoides. En cuanto al tratamiento concomitante con pirfenidona de interés, cabe destacar que el 54,5% (6 pacientes) al inicio de pirfenidona se encontraban en tratamiento con omeprazol y un paciente con fluoxetina. En todos los casos, previo al inicio del tratamiento con pirfenidona, el omeprazol se sustituyó por ranitidina o pantoprazol y en el paciente en tratamiento con fluoxetina se cambió de tratamiento antidepresivo por mirtazapina que no interacciona con pirfenidona. Todos los pacientes fueron tratados de forma inicial con pirfenidona 267 mg/8h, la segunda semana 534 mg/8h y desde la tercera en adelante 801 mg/8h. La duración media de tratamiento fue de 19,1 meses (DE 12,9). En cuanto a las variables de efectividad se resumen en la tabla 2.
En cuanto a las exposiciones a factores de riesgo, el 36,4% de los pacientes había estado expuesto a metales, aleaciones y/o polvo de madera, el 18,2% trabajaba en ganadería, agricultura y/o construcción de casas de madera y el 45,5% eran exfumadores (una paciente estuvo expuesta de forma pasiva al humo del tabaco durante 25 años). El diagnóstico de FPI en el 36,4% de los pacientes estaba confirmado radiológicamente, en el 27,3% FPI probable y en el 36,4% FPI posible. El 90,9% de los pacientes había recibido tratamiento previo para FPI, el más frecuente NAC más corticoides. En cuanto al tratamiento concomitante con pirfenidona de interés, cabe destacar que el 54,5% (6 pacientes) al inicio de pirfenidona se encontraban en tratamiento con omeprazol y un paciente con fluoxetina. En todos los casos, previo al inicio del tratamiento con pirfenidona, el omeprazol se sustituyó por ranitidina o pantoprazol y en el paciente en tratamiento con fluoxetina se cambió de tratamiento antidepresivo por mirtazapina que no interacciona con pirfenidona. Todos los pacientes fueron tratados de forma inicial con pirfenidona 267 mg/8h, la segunda semana 534 mg/8h y desde la tercera en adelante 801 mg/8h. La duración media de tratamiento fue de 19,1 meses (DE 12,9). En cuanto a las variables de efectividad se resumen en la tabla 2. 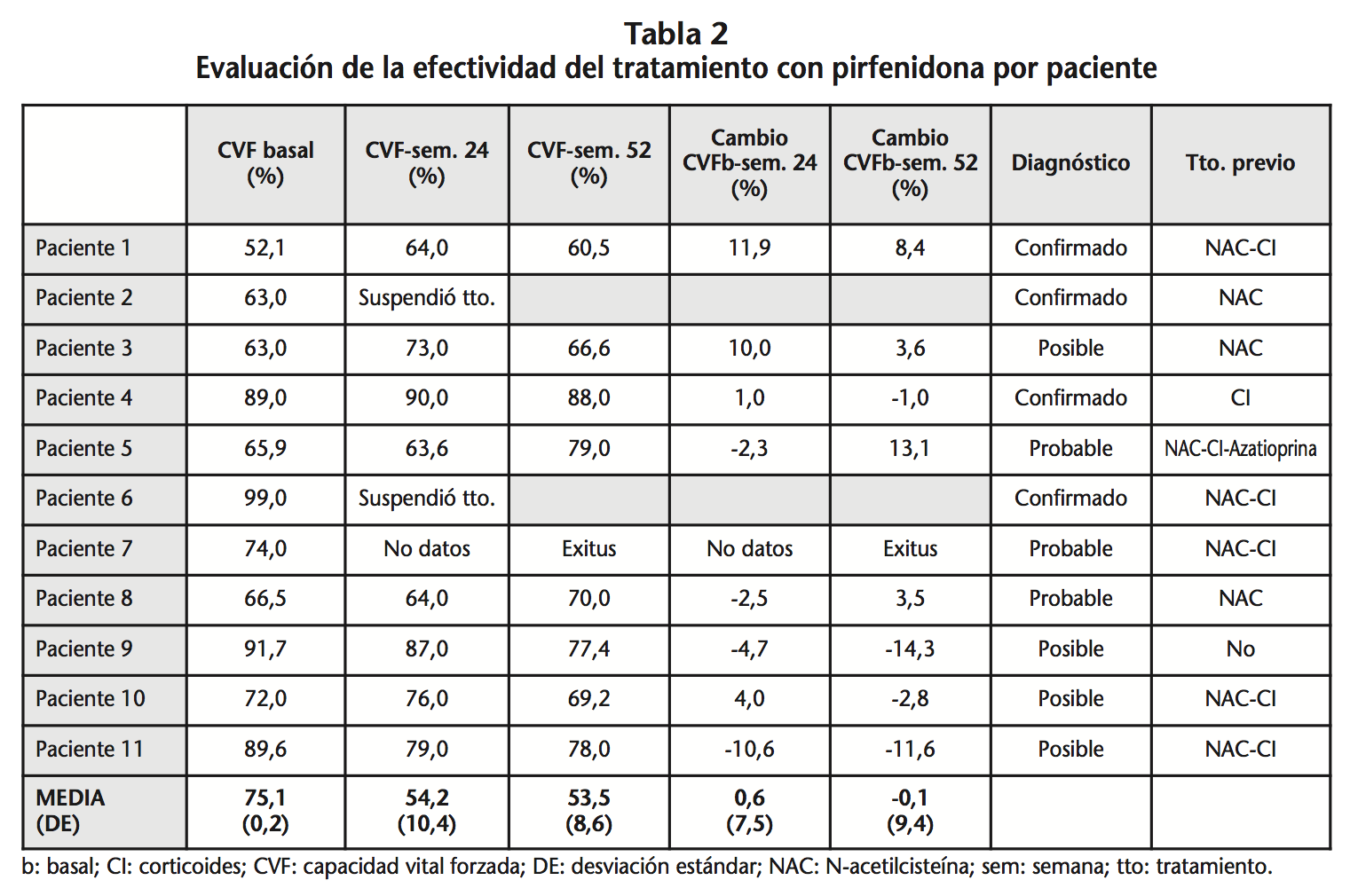
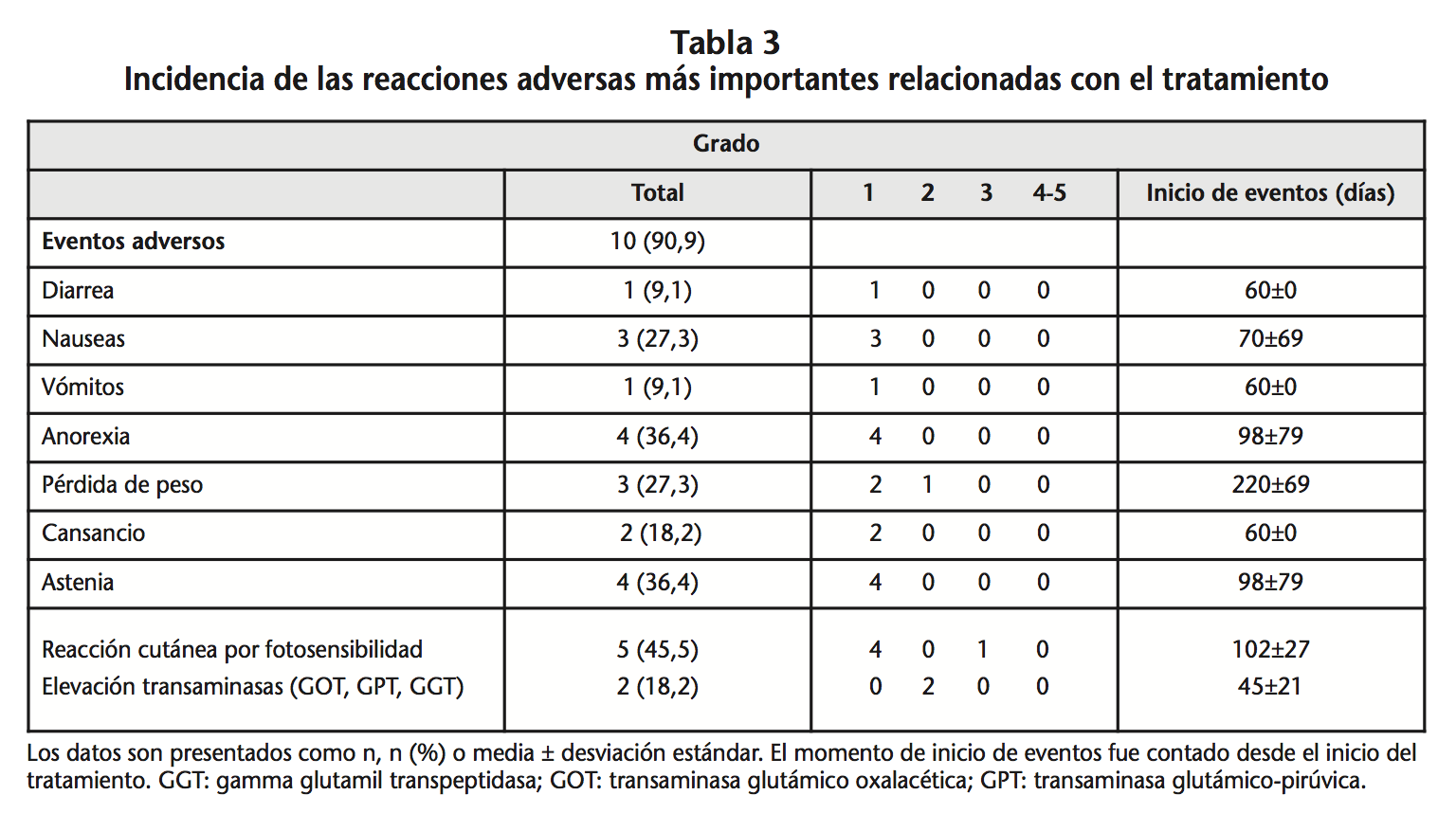
Cabe destacar que se dispone de datos de CVF basal de 11 pacientes y a la semana 24 y 52 de 8 pacientes. A la semana 24 cuatro pacientes (36,4%) sufrieron disminución de la CVF, siendo en uno de ellos la disminución mayor del 10% y en los otros cuatro (36,4%) la CVF aumentó. El 63,6% de los pacientes presentaron SLP a la semana 24. A la semana 52, de los ocho pacientes cuatro presentaron aumento de CVF y los otros cuatro disminución. Dicha disminución fue mayor del 10% en dos pacientes y hubo un exitus. El 54,5% de los pacientes presentaron SLP a la semana 52. Un 90,9% de los pacientes presentó EA, los más frecuentes fueron: reacción cutánea por fotosensibilidad (45,5%), anorexia (36,4%), astenia (36,4%), nauseas (27,3%) y pérdida de peso (27,3%). La tabla 3 incluye la incidencia y el momento de inicio de los EA. Se suspendió el tratamiento con pirfenidona al tercer mes en dos pacientes, en uno por reacción de fotosensibilidad y en otro por elevación de las enzimas hepáticas.
DISCUSIÓN
La utilización de pirfenidona ha sido adecuada a recomendaciones de ficha técnica y de normativa de tratamiento de la Sociedad Española de Neumología y Cirugía Torácica, en cuanto a posología y el carácter leve-moderado de la FPI. Salvo que el diagnóstico no pudo ser en todos los casos confirmado y se ha determinado como posible o probable1,8.
La población estudiada es comparable en cuanto a edad, sexo y función pulmonar al inicio del tratamiento a los pacientes de los ensayos clínicos (EC): the CAPACITY program9 (PIPF-004 [CAPACITY 1] y PIPF-006 [CAPACITY 2]), Assessment of Pirfenidone to Confirm Efficacy and Safety in Idiopathic Pulmonary Fibrosis13 (ASCEND) y el realizado en Japón14. Asimismo también son similares en edad y sexo a los pacientes tratados con pirfenidona en vida real del estudio del registro del Named Patient Program15 (NPP), patrocinado por Intermune para facilitar el acceso al tratamiento con pirfenidona antes de su comercialización. Sin embargo, no son similares al estudio del registro del NPP en la función pulmonar al inicio, ya que en un 14% de los pacientes la CVF era menor del 50% y en un 25% la DLCO era menor del 35%. Estas diferencias respecto a la población de los EC han ocurrido en otros pacientes tratados con pirfenidona en la vida real, debido en parte, a la imperiosa necesidad de tratamiento ante la gravedad de esta patología y la ausencia de alternativas terapéuticas, aunque no cumplieran estrictamente los criterios de inclusión15.
En cuanto a la efectividad del tratamiento, con los datos disponibles de nuestro estudio a la semana 52 la función pulmonar en algunos pacientes mejoró y en otros empeoró, podemos decir que es comparable a lo descrito en el estudio del registro NPP15. En el estudio ASCEND13 a la semana 52 el 16,5% de pacientes en el grupo de pirfenidona frente al 31,8% de pacientes en el grupo de placebo presentó un descenso de la CVF mayor del 10% o fallecieron, lo que supone una reducción relativa del riesgo de progresión o muerte de casi un 50%. Aunque el diseño del estudio no tiene potencia estadística significativa para demostrar el efecto sobre la mortalidad un análisis preespecificado, de los datos conjuntos de los EC CAPACITY y ASCEND, demostró una reducción del riesgo de muerte por cualquier causa al año de un 48% en los pacientes tratados con pirfenidona13. En un metaanálisis realizado por la Cochrane Collaboration de los tres EC fase 3 publicados se mostró una reducción del riesgo de progresión de la enfermedad y de muerte en un 30%16. En nuestro estudio el porcentaje de pacientes con deterioro no superior al 10% de la CVF y/o muerte fue del 63,6% en la semana 24 y del 54,5% en la semana 52. Si bien aunque no es la variable estudiada de efectividad la CVF a la semana 52 respecto a la 24, cabe destacar que en 6/8 pacientes la CVF empeoró.
Los EA observados con más frecuencia fueron los trastornos del metabolismo y nutrición (anorexia y pérdida de peso), astenia, nauseas y reacción cutánea por fotosensibilidad. Las molestias gastrointestinales de nuestros pacientes fueron menores que en los EC, la incidencia de vómitos fue de un 9,1% y en los EC CAPACITY9 14,0% y en el ASCEND13 12,9%. Cabe mencionar que tanto el neumólogo como el farmacéutico insistían en que la administración de pirfenidona se realizase con alimentos, para reducir la posibilidad de nauseas y mareos. Por otra parte, más del 50% de los pacientes del presente estudio estaban en tratamiento concomitante con pantoprazol o ranitidina hecho que puede haber contribuido a esta menor incidencia de molestias gastrointestinales. La incidencia de anorexia observada (36,4%) fue superior a la descrita en los EC (CAPACITY 11,1%9, ASCEND 15,8%13 y japonés 16,5%14). En este estudio, la incidencia de reacción por fotosensibilidad fue del 45,5%, ligeramente inferior al ensayo japonés (51,4%)14; sin embargo, fue muy superior a la incidencia obtenida en el CAPACITY (12,0%)9. Esta mayor incidencia de reacción por fotosensibilidad en nuestros pacientes fue en la mayoría de carácter leve, con la excepción de un paciente en el que fue necesario suspender el tratamiento. Se trata de una incidencia elevada, a pesar del esfuerzo por el equipo médico y farmacéutico de la información aportada en relación a la importancia del uso de protectores solares y otras medidas de protección. La reacción de fotosensibilidad tiene un marcado patrón estacional, siendo más frecuente en los meses con mayor radiación solar17.
La tasa de discontinuación del tratamiento con pirfenidona debido a EA en este estudio fue del 18,2%, cifra ligeramente superior que las obtenidas en los EC CAPACITY9 (14,8%) y ASCEND13 (14,4%), y similar a la del EC japones14 (18,3%).
El tratamiento con pirfenidona fue en general seguro y con un perfil de efectos secundarios aceptables, estos resultados son acordes con los de estudios previos9,13-16.
Este estudio presenta las limitaciones propias del diseño retrospectivo, que ha ocasionado la pérdida de datos no recogidos e impide la medición de la calidad de vida. Además, como limitación cabe mencionar que incluye un bajo número de pacientes, lo que impide tener potencia para obtener resultados significativos.
En el momento del estudio pirfenidona era la única opción de tratamiento de FPI en España. Recientemente se ha comercializado nintedanib, por lo que sería conveniente un estudio de comparación directa para optimizar el posicionamiento terapéutico de ambos fármacos en esta patología. Pues, tal como concluye el informe de posicionamiento terapéutico de nintedanib, no se puede establecer si existen diferencias con pirfenidona, y recomienda que la elección entre nintedanib y pirfenidona se base fundamentalmente en criterios de eficiencia18.
En conclusión, la utilización de pirfenidona ha sido adecuada a recomendaciones, aunque por la dificultad del diagnóstico de FPI, éste ha sido definido como probable o posible en algunos casos. El perfil de seguridad y tolerabilidad del fármaco de acuerdo a nuestros datos es aceptable. La efectividad se considera modesta en la disminución del deterioro pulmonar en pacientes con FPI de leve a moderada. No obstante, se necesita un mayor número de pacientes y un seguimiento más completo de los mismos para obtener conclusiones más sólidas.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
BIBLIOGRAFÍA
1. Xaubet A, Ancochea J, Bollo E, Fernández-Fabrellas E, Franquet T, Molina-Molina M, et al. Normativa sobre el diagnóstico y tratamiento de la fibrosis pulmonar idiopática. Arch Bronconeumol. 2013;49(8):343-353.
2. Raghu G, Collard HR, Egan JJ, Martinez FJ, Behr J, et al. ATS/ERS/JRS/ALAT Committee on Idiopathic Pulmonary Fibrosis. An official ATS/ERS/JRS/ALAT statement: idiopathic pulmonary fibrosis: evidence-based guidelines for diagnosis and management. Am J Respir Crit Care Med. 2011;183:788-824.
3. Nalysnyk L, Cid-Ruzafa J, Rotella P, Esser D. Incidence and prevalence of idiopathic pulmonary fibrosis: review of the literature. Eur Respir Rev. 2012;21:126, 355-61.
4. Ramos M, Ussetti P, Benítez M, Tapiador N, Gotor P, Millán I. El test de seis minutos de marcha como predictor de mortalidad en lista de espera para trasplante pulmonar. Rehabilitación (Madr). 2011;45(2):122-126.
5. Hui Huang MD, Hua Ping Dai MD, Jian Kang MD, Bao Yuan Chen MD, Tie Ying Sun, Zuo Jun Xu, MD. Double-Blind Randomized Trial of Pirfenidone in Chinese Idiopathic Pulmonary Fibrosis Patients. Medicine (Baltimore) 2015 Oct;94(42):e1600.
6. The Idiopathic Pulmonary Fibrosis Clinical Research Network. Prednisone, Azathioprine, and N-Acetylcysteine for pulmonary fibrosis. N Engl J Med. 2012;366: 1968-77.
7. George TJ, Arnaoutakis GJ, Shah AS. Lung transplant in idiopathic pulmonary fibrosis. Arch Surg. 2011;146: 1204-9.
8. Ficha técnica Esbriet® (pirfenidona). Última actualización 28 febrero 2011. Disponible en: http://www.ema. europa.eu/docs/es_ES/document_library/EPAR_Product_Information/human/002154/WC500103049.pdf.
9. Noble PW, Albera C, Bradford WZ, Costabel U, Glassberg MK, Kardatzke D, et al. Pirfenidone in patients with idiopathic pulmonary fibrosis (CAPACITY): two randomized trials. Lancet 2011;377:1760-9.
10. nice.org.uk (2011) Disponible en: http://www.nice. org.uk/guidance/ta282/documents/idiopathic-pulmonaryfibrosis-pirfenidone-pre-meeting-briefing2.
11. Aravena C, Labarca G, Venegas C, Arenas A, Rada G. Pirfenidone for Idiopathic Pulmonary Fibrosis: A Systematic Review and Meta-Analysis. PLoS ONE 2015 Aug; 10(8):e0136160.
12. National Cancer Institute Common Toxicity Criteria for Adverse Events (CTCAE) v 4.0: Junio 2010, (acceso Junio 2016). Disponible en: http://evs.nci.nih.gov/ ftp1/CTCAE/CTCAE_4.03_2010-06-14_QuickReference_5x7.pdf.
13. King TE, Bradford WZ, Castro-Bernardini S, Fagan EA, Glaspole I, Glassberg MK, Gorina E, et al. 016 – Phase 3 Trial of Pirfenidone in Patients with Idiopathic Pulmonary Fibrosis. N Engl J Med. 2014;370:2083-92. PIPF-016.
14. Taniguchi H, Ebina M, Kondoh Y, Ogura T, Azuma A, Suga M, et al. Pirfenidone in idiopathic pulmonary fibrosis. Eur Respir J. 2010;35:821-9.
15. Nieto A, Valenzuela C. Tratamiento de la fibrosis pulmonar idiopática: de la teoría a la vida real. Monogr Arch Bronconeumol. 2015;2(1):23-30.
16. Spagnolo P, Del Giovane C, Luppi F, Cerri S, Balduzzi S, Walters EH, et al. Non-steroid agents for idiopathic pulmonary fibrosis. Cochrane Database Syst Rev. 2010;9: CD003134.
17. Assessment report – Esbriet® (European Medicines Agency) Disponible en: http://www.ema.europa.eu/ docs/en_GB/document_library/EPAR_-_Public_assessment_report/human/002154/WC500103073.pdf [consultado en junio 2016].
18. Informe de Posicionamiento Terapéutico de nintedanib (Ofev®) para el tratamiento de la Fibrosis Pulmonar Idiopática. Fecha de publicación: 18 diciembre 2015. Disponible en: https://www.aemps.gob.es/medicamentosUsoHumano/informesPublicos/docs/IPT-nintedanib-Ofev.pdf.
____
Descargar artículo en PDF: Pirfenidona en el tratamiento de fibrosis pulmonar idiopática: experiencia de uso
