Gil-Sierra MD1,2, Ríos-Sánchez E1, Briceño-Casado MP3, Borrero-Rubio JM1, Armario-Hita JC4
1 Servicio de Farmacia. Hospital Universitario de Puerto Real. Puerto Real. Cádiz (España)
2 Departamento de Farmacología. Facultad de Farmacia. Universidad de Sevilla. Sevilla (España)
3 Servicio de Farmacia. Hospital Universitario de Jerez. Jerez de la Frontera. Cádiz (España)
4 Servicio de Dermatología. Hospital Universitario de Puerto Real. Puerto Real. Cádiz (España)
Fecha de recepción: 24/05/2022 – Fecha de aceptación: 17/06/2022
Correspondencia: María del Pilar Briceño-Casado – Hospital Universitario de Jerez (Servicio de Farmacia) – Ronda de Circunvalación, s/n – 11407 Jerez de la Frontera, Cádiz (España)
pilarbricenocasado@gmail.com
____
RESUMEN
Objetivo: Describir el desarrollo e implementación de un protocolo de optimización de omalizumab en urticaria crónica espontánea, mostrando resultados en vida real.
Métodos: Estudio descriptivo retrospectivo de pacientes con urticaria crónica espontánea incluidos en el programa de optimización de omalizumab entre 01/10/2020-01/06/2021. La efectividad fue valorada mediante Urticaria Activity Score durante 7 días (UAS7), a los 6, 12, 18, 24, 30, 36, 42, 48, 54, 60, 66, 72 meses. Se calcularon los pacientes respondedores (UAS7≤15) y no respondedores (UAS7>15), así como con buen control de la enfermedad (UAS7≤6) y respuesta completa (UAS7=0). Se estimó el ahorro obtenido por la optimización mediante reducción de dosis o discontinuación por mejoría clínica.
Resultados: De los 47 pacientes incluidos, se había optimizado omalizumab en 29 (61,7%): 1 (2,1%) paciente presentó sólo reducción de dosis, 11 (23,4%) sólo discontinuación y 17 (36,2%) presentaron ambas. La mayoría de valoraciones de efectividad presentaron entre el 70-90% de respondedores. Sólo a los 12 meses se observó menor proporción de respondedores (66,7%). El ahorro económico total asociado a la optimización fue de 286.150,1€: 172.747,7€ mediante discontinuación de tratamiento y 113.402,4€ mediante reducción de dosis.
Conclusiones: El protocolo de optimización de omalizumab en urticaria crónica espontánea proporcionó una alta eficiencia, manteniendo una adecuada efectividad.
Palabras clave: Omalizumab, protocolo, urticaria crónica espontánea, efectividad, eficiencia.
Protocol for the use of omalizumab in chronic spontaneous urticaria: development and real-life clinical practice data
SUMMARY
Objectives: To describe the development and implementation of an omalizumab optimisation protocol in chronic spontaneous urticaria, showing real-life data.
Methods: A retrospective descriptive study of patients with chronic spontaneous urticaria included in the omalizumab optimisation programme between 01/10/2020-01/06/2021 was conducted. Effectiveness was assessed by Urticaria Activity Score over 7 days (UAS7), at 6, 12, 18, 24, 30, 36, 42, 48, 54, 60, 66, 72 months. Responders (UAS7≤15) and non-responders (UAS7>15), as well as patients with good disease control (UAS7≤6) and complete response (UAS7=0) were estimated. Savings from optimisation by dose reduction or discontinuation due to clinical improvement were calculated.
Results: Forty-seven patients were included. Omalizumab was optimised in 29 patients (61.7%): 1 (2.1%) patient only presented dose reduction, 11 (23.4%) only treatment discontinuation and 17 (36.2%) had both interventions. Most effectiveness assessments presented between 70-90% of responders. Only the effectiveness valoration presented a lower proportion of responders (66.7%) at 12 months. The total economic savings associated with optimisation were 286,150.1€: 172,747.7€ through treatment discontinuations and 113,402.4€ through dose reductions.
Conclusions: The optimisation protocol for omalizumab in chronic spontaneous urticaria provided high efficiency, maintaining an adequate effectiveness.
Key words: Omalizumab, protocol, chronic spontaneous urticaria, effectiveness, efficiency.
____
INTRODUCCIÓN
La urticaria crónica espontánea (UCE) es una enfermedad con persistencia de sintomatología cutánea durante más de 6 semanas. La presencia de habones se presenta sin una causa identificable en este desorden dermatológico. La prevalencia de UCE es de aproximadamente el 1% de la población1. La liberación patógena de mediadores proinflamatorios por mastocitos y basófilos lidera la generación de UCE. Asimismo, en esta patología parecen estar involucrados autoanticuerpos específicos de inmunoglobulina G (IgG) y de inmunoglobulina E (IgE) contra una amplia gama de antígenos que pueden encontrarse fuera de mastocitos y basófilos2. La escala Urticaria Activity Score (UAS) es ampliamente utilizada para medir la actividad de la UCE. El UAS diario valora la intensidad del picor y número de habones con una escala de puntuación creciente de 0-6, donde las puntuaciones más altas indican una mayor intensidad de la enfermedad. UAS7 se define como el sumatorio de puntuaciones de UAS diarios durante 7 días consecutivos3.
Omalizumab es un fármaco utilizado en UCE, asma y rinosinusitis crónica con pólipos nasales4. Este anticuerpo se une selectivamente a IgE. Las enfermedades autoinmunes presentan fluctuaciones de la sintomatología, alternándose episodios agudos con momentos de baja actividad de la enfermedad5-7. La evaluación de los resultados en ensayos clínicos de omalizumab para UCE durante más de 6 meses es limitada. La recuperación de la eficacia de omalizumab mediante su reintroducción ante agudizaciones de enfermedad hace posible la discontinuación del tratamiento según criterio clínico. Además, teniendo en cuenta que la administración de mayores dosis del fármaco podría estar asociado a eventos adversos más frecuentes, parece razonable usar la dosis mínima eficaz de omalizumab. Por otra parte, el impacto económico de este medicamento en UCE podría ser considerable8.
El desarrollo e implementación de protocolos que permitan optimizar el uso de medicamentos biológicos se presenta como una herramienta interesante para la sostenibilidad de los sistemas sanitarios9. Por otra parte, la colaboración multidisciplinar entre facultativos y farmacéuticos es imprescindible para combinar los datos de medicina basada en evidencia y la experiencia clínica durante la implementación de estos protocolos. Teniendo en cuenta todo lo anterior, omalizumab es un candidato ideal para la aplicación de una estrategia multidisciplinar que favorezca la eficacia, seguridad y eficiencia del tratamiento para UCE. Este trabajo describe el proceso de desarrollo e implementación de un protocolo de optimización de uso de omalizumab en UCE, además de mostrar resultados de la práctica clínica en vida real.
MÉTODOS
Valoración del punto de partida
Para la valoración del punto de partida, se llevó a cabo un estudio de dispensaciones desde el 1 de octubre de 2020 hasta el 1 de junio de 2021.
Población a estudio
Se desarrolló un estudio descriptivo retrospectivo durante el período de estudio de dispensaciones, comprendido entre el 1 de octubre de 2020 hasta el 1 de junio de 2021, de los pacientes con UCE tratados con omalizumab que habían recibido previamente antihistamínicos H1 a dosis 4 veces superior a la habitual, presentando respuesta inadecuada. Se usaron tanto la dosis recomendada por ficha técnica de 300 mg de omalizumab por inyección subcutánea cada cuatro semanas4, como otras dosis inferiores o superiores según criterio clínico.
Extracción de datos
El módulo de dispensación de paciente externos Dominion Farmatools® y la historia clínica digital fueron usados para el registro de datos de los pacientes del estudio descriptivo retrospectivo. Se recogieron características poblacionales (género, edad), datos de tratamientos (uso de corticoides previos, duración del tratamiento con omalizumab, optimización por discontinuación de tratamiento o reducción de dosis, tratamiento activo antes de implantación de protocolo, pauta de omalizumab actual) y escala basal de UAS7.
Variables y análisis de datos
La intensidad de la UCE fue medida mediante UAS7. La efectividad fue valorada mediante UAS7 a los 6, 12, 18, 24, 30, 36, 42, 48, 54, 60, 66, 72 meses. Se calcularon los porcentajes de pacientes respondedores (UAS7≤15) y no respondedores (UAS7>15)5,6. También fueron estimados los porcentajes de pacientes con buen control de la enfermedad (UAS7=1-6) y respuesta completa (UAS7=0)10,11. Los pacientes con suspensión de tratamiento debido a falta de efectividad en un determinado mes fueron categorizados como no respondedores en los siguientes. Aquellos pacientes que presentaron un seguimiento insuficiente en alguna de las valoraciones de efectividad se definieron como no valorables. Los porcentajes de pacientes con diferentes respuestas fueron estimados teniendo en cuenta los datos de pacientes valorables.
Estimación del ahorro económico
Posteriormente, se estimó el ahorro obtenido por la optimización del tratamiento de UCE con omalizumab, ya sea mediante reducción de dosis o la discontinuación por mejoría clínica. Para ello, se estimaron los costes asociados a omalizumab durante el período a estudio con respecto a la hipotética administración continuada de omalizumab 300 mg cada cuatro semanas, siendo ésta la dosis recomendada por ficha técnica4.
Diseño del algoritmo de decisión
El diseño del protocolo de optimización de UCE fue desarrollado teniendo en cuenta los diferentes tipos de respuesta a omalizumab según valores de UAS73,5,6,10,11, así como la posibilidad de aparición de respondedores lentos. Por este motivo, omalizumab no fue retirado de los pacientes no respondedores hasta, al menos, el sexto mes de tratamiento. Por otra parte, se consideró la escasa experiencia con omalizumab en ensayos clínicos de UCE más allá de seis meses4. Asimismo, se tomaron como base otros algoritmos de decisión ajustándolos al sistema de citas del centro12,13. Los pacientes fueron valorados periódicamente en el hospital cada 3 meses.
RESULTADOS
Resultados del punto de partida
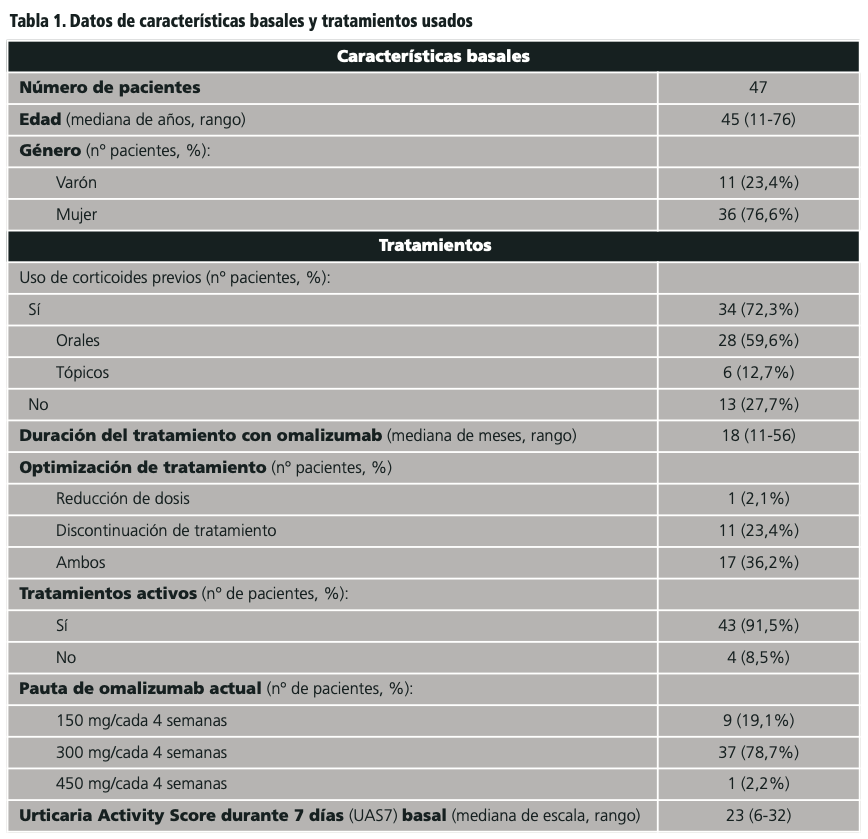
Fueron incluidos 47 pacientes en el estudio, siendo el 76,6% mujeres. El 72,3% de los pacientes recibieron previamente corticoides. La mediana de duración de tratamiento con omalizumab fue de 18 (11-56) meses. Se había realizado optimización del tratamiento de omalizumab en 29 (61,7%) pacientes: 17 (36,2%) pacientes tuvieron tanto suspensión como reducción de dosis; 1 (2,1%) paciente sólo reducción de dosis y 11 (23,4%) pacientes sólo discontinuación de tratamiento. Las discontinuaciones de tratamiento se llevaron a cabo por criterio clínico individual de los facultativos, en aquellos pacientes que presentaban un adecuado control de la enfermedad. Antes de la implantación de protocolo, el 91,5% de los pacientes incluidos en el estudio tenían tratamiento activo con omalizumab. El 78,7% de los pacientes recibían una dosis de 300 mg cada cuatro semanas. El valor basal de UAS7 presentó una mediana de 23 (6-32). La tabla 1 resume las características poblacionales y datos de tratamientos previos.
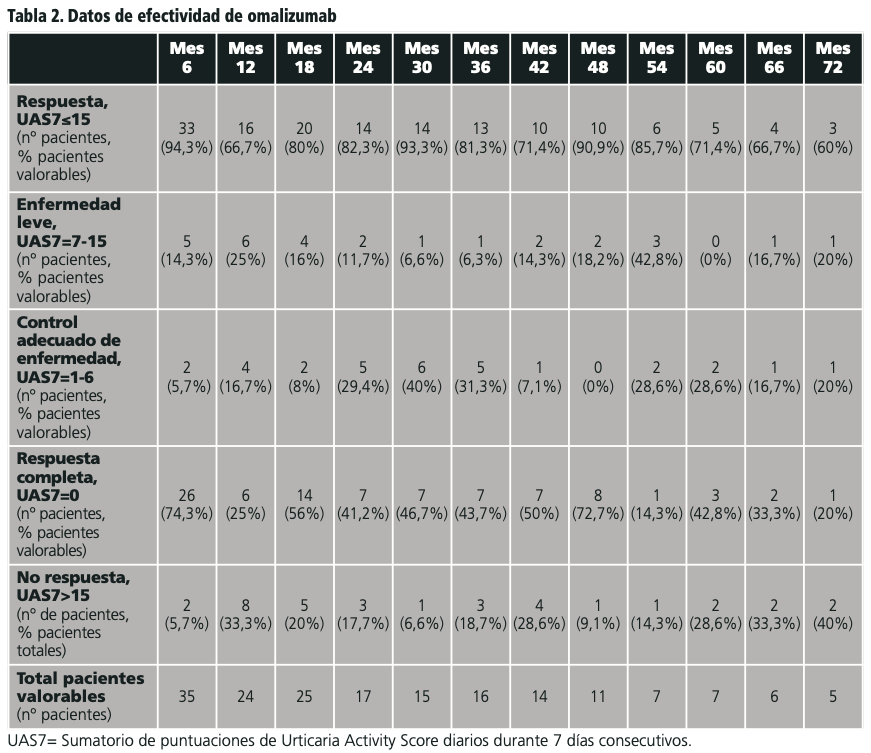
Los datos de efectividad de omalizumab se recogen en la tabla 2. La mayoría de las valoraciones en los meses establecidos presentaron unos porcentajes entre el 70-90% de respondedores. Sólo a los 12 meses se observó una proporción de respondedores menor (66,7%). El ahorro económico total asociado a la optimización del tratamiento con omalizumab en UCE en los pacientes revisados fue de 286.150,1 euros. Del total, 172.747,7 euros fueron ahorrados mediante discontinuación de tratamientos y 113.402,4 euros mediante reducción de dosis.
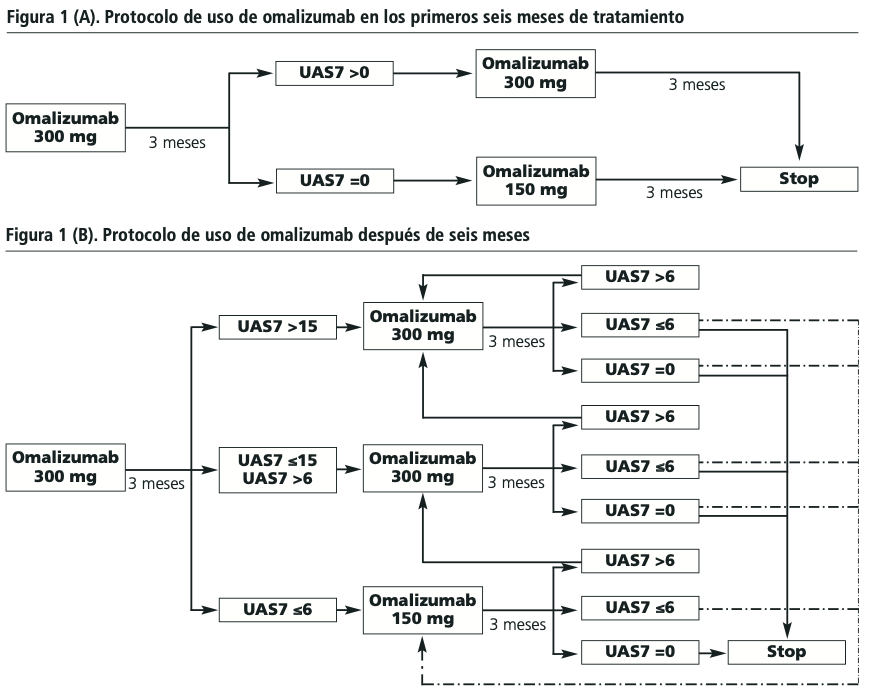
Algoritmo de decisión
Se diseñó un algoritmo de decisión dividido en dos partes: tratamiento con omalizumab en los primeros seis meses y tratamiento en meses posteriores. Se aplicó una discontinuación de tratamiento tras los primeros 6 meses, considerando la escasa evidencia científica posterior a este período4. Posteriormente, se reintrodujo el tratamiento ante empeoramiento clínico. Se consensuó con el equipo facultativo la posibilidad de reducción de dosis a omalizumab 150 mg/cada 4 semanas tras tres meses de tratamiento según clínica, como se ha recomendado en pacientes con respuesta completa (UAS7=0)14. Esta propuesta por parte del Servicio de Farmacia fue aceptada por los médicos. El algoritmo de decisión de omalizumab en UCE puede consultarse en la figura 1.
DISCUSIÓN
Este trabajo ha descrito el proceso de desarrollo e implementación de un protocolo del uso de omalizumab en UCE, mostrando además resultados de la práctica clínica en vida real. La elaboración de protocolos de optimización de medicamentos permite la colaboración multidisciplinar de diferentes profesionales sanitarios en aras del uso racional de los fármacos. En este caso, la integración del farmacéutico y de especialistas de dermatología en equipos multidisciplinares es una oportunidad para la mejora de la eficiencia sin que se resientan los resultados en salud. El diseño de algoritmos de decisión supone un proceso de formalización del trabajo multidisciplinar y una herramienta de apoyo para la toma de decisiones clínicas diarias. Asimismo, este proyecto podría ser un primer paso para mejorar la comunicación entre los especialistas en dermatología y farmacéuticos. La aplicación de protocolos permite una homogeneización de los criterios clínicos sobre el manejo de un fármaco en una determinada patología, en este caso UCE. De esta manera, se minimizan posibles inequidades de tratamiento intrahospitalarias por el mero hecho de la atención de diferentes profesionales sanitarios15.
En este estudio se muestra como la reducción de dosis o discontinuación de tratamiento de omalizumab en pacientes con un adecuado control de UCE puede proveer de una notable mejora de la eficiencia, manteniendo una adecuada efectividad. Los resultados observados en este trabajo son consistentes con otros estudios de datos en vida real en los que se ha descrito un adecuado control de la enfermedad con dosis reducidas de omalizumab16,17. Asimismo, el protocolo diseñado presenta intervenciones en períodos de tiempo (a los 3-6 meses de tratamiento) similares a los descritos en algunos consensos de expertos14. Otras cuestiones importantes para la mejora del algoritmo de decisión desarrollado podrían ser la optimización del manejo de las dosis de corticoides o el desarrollo de circuitos para la detección precoz de recaídas antes de la visita de pacientes a las consultas médicas. Sin lugar a dudas, futuros estudios –o ampliaciones de este mismo– podrían servir para salvar estas limitaciones.
Por otra parte, el protocolo de uso de omalizumab no sólo ha compilado evidencia científica publicada anteriormente, sino que la ha acomodado a los recursos del centro y forma de trabajo, además de proponer puntos de mejora como la reducción de dosis a omalizumab 150 mg/cada 4 semanas tras los tres primeros meses de tratamiento. Finalmente, podemos decir que un seguimiento estrecho del paciente, sumado a una mayor colaboración entre profesionales sanitarios, podría repercutir positivamente no solamente en la eficiencia del tratamiento de omalizumab en UCE, sino en la efectividad y seguridad del fármaco por una mayor detección de pérdida de efectividad y reacciones adversas.
CONCLUSIONES
Este trabajo describe el desarrollo e implementación de un protocolo del uso de omalizumab en UCE. El diseño de algoritmos de decisión supone un proceso de formalización del trabajo multidisciplinar y una herramienta de apoyo para la toma de decisiones clínicas diarias. En este estudio se muestra como la reducción de dosis o discontinuación de tratamiento de omalizumab en UCE puede proveer de una notable mejora de la eficiencia, manteniendo una adecuada efectividad.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
BIBLIOGRAFÍA
1. Saini SS. Chronic spontaneous urticaria: etiology and pathogenesis. Immunol Allergy Clin North Am. 2014;34(1):33-52. Doi: 10.1016/j.iac.2013.09.012.
2. Bracken SJ, Abraham S, MacLeod AS. Autoimmune theories of chronic spontaneous urticaria. Front Immunol. 2019;10:627. Doi: 10.3389/fimmu.2019.00627.
3. Mathias SD, Crosby RD, Rosén KE, Zazzali JL. Evaluating the minimally important difference of the urticaria activity score and other measures of disease activity in patients with chronic idiopathic urticaria. Ann Allergy Asthma Immunol. 2012;108:20-4. Doi: 10.1016/j.anai.2011.09.008.
4. Agencia Española de Medicamentos y Productos Sanitarios. Ficha Técnica de Xolair® 150 mg. 2015 (acceso el 20 de julio 2021). Disponible en: https:// cima.aemps.es/cima/dochtml/ft/05319008/FT_05319008.html.
5. Maurer M, Rosén K, Hsieh H, Saini S, Grattan C, Gimenéz-Arnau A, et al. Omalizumab for the treatment of chronic idiopathic or spontaneous urticaria. N Engl J Med. 2013;368(10):924-35. Doi: 10.1056/NEJMoa1215372.
6. Kaplan A, Ledford D, Ashby M, Canvin J, Zazzali JL, Conner E, et al. Omalizumab in patients with symptomatic chronic idiopathic/spontaneous urticaria despite standard combination therapy. J Allergy Clin Immunol. 2013;132(1): 101-9. Doi: 10.1016/j.jaci.2013.05.013.
7. Saini SS, Bindslev-Jensen C, Maurer M, Grob J, Baskan EB, Bradley MS, et al. Efficacy and safety of omalizumab in patients with chronic idiopathic/spontaneous urticaria who remain symptomatic on H1 antihistamines: a randomized, placebo-controlled study. J Invest Dermatol. 2015;135(1):67-75. Doi: 10.1038/jid.2014.306.
8. Daiki Matsubara, Shunsuke Takahagi, Ryo Saito, Akiko Kamegashira, Akio Tanaka, Michihiro Hide. Analysis of the long-term economic burden of omalizumab on patients with chronic spontaneous urticaria. J Dermatol. 2021;48(1): 56-63. Doi: 10.1111/1346-8138.15630.
9. Wu Y, Lin B, Thilakanathan C, Lehmann P, Xuan W, Mohsen W, et al. Therapeutic drug monitoring in inflammatory bowel disease reduces unnecessary use of infliximab with substantial associated cost-savings. Intern Med J. 2021; 51(5):739-45. Doi: 10.1111/imj.14644.
10. Zuberbier T, Aberer W, Asero R, Bindslev-Jensen C, Canonica GW, Church MK, et al. The EAACI/GA2 LEN/EDF/WAO Guideline for the definition, classification, diagnosis, and management of urticaria: the 2013 revision and update. Allergy 2014; 69: 868-887. Doi: 10.1111/all.12370.
11. Stull D, McBride D, Tian H, Gimenez Arnau A, Maurer M, Marsland A, et al. Analysis of disease activity categories in chronic spontaneous/idiopathic urticaria. Br J Dermatol. 2017;177(4):1093-1101. Doi: 10.1111/bjd.15454. Epub 2017 Sep 24.
12. Uysal P, Eller E, Mortz CG, Bindslev-Jensen C. An algorithm for treating chronic urticaria with omalizumab: dose interval should be individualized. J Allergy Clin Immunol. 2014 Mar;133(3):914-5.e2. Doi: 10.1016/j.jaci.2013.10.015.
13. Spertino J, Curto Barredo L, Rozas Muñoz E, Figueras Nart I, Gimenez Arnau A, Serra Baldrich E, et al. Algorithm for treatment of chronic spontaneous urticaria with omalizumab. Actas Dermosifiliogr (Engl Ed). 2018;109(9):771-6. Doi: 10.1016/j.ad.2018.07.005.
14. Giménez Arnau AM, Valero Santiago A, Bartra Tomás J, Jáuregui Presa I, Labrador Horrillo M, Miquel Miquel FJ, et al. Therapeutic Strategy According to Differences in Response to Omalizumab in Patients With Chronic Spontaneous Urticaria. J Investig Allergol Clin Immunol. 2019;29(5):338-48. Doi: 10.18176/ jiaci.0323.
15. Arcaya MC, Arcaya AL, Subramanian SV. Inequalities in health: definitions, concepts, and theories. Glob Health Action. 2015;8:27106. Doi: 10.3402/ gha.v8.27106.
16. Metz M, Ohanyan T, Church MK, Maurer M. Omalizumab is an effective and rapidly acting therapy in difficult-to-treat chronic urticaria: a retrospective clinical analysis. J Dermatol Sci. 2014;73(1):57-62. Doi: 10.1016/j.jdermsci.2013. 08.011.
17. Sussman G, Hébert J, Barron C, Bian J, Caron-Guay RM, Laflamme S, et al. Real-life experiences with omalizumab for the treatment of chronic urticaria. Ann Allergy Asthma Immunol. 2014;112(2):170-4. Doi: 10.1016/j.anai. 2013.12.005.
____
