Zayas Soriano M, Bernabéu Martínez MA, Bonete Sánchez M, Hernández Guio A, Planelles de Castro M, Aznar Saliente T
Hospital Universitario San Juan de Alicante (España)
Fecha de recepción: 15/12/2021 – Fecha de aceptación: 20/01/2022
Correspondencia: Marta Zayas Soriano – Hospital Universitario San Juan de Alicante – Carretera N-332, s/n – 03550 Sant Joan d’Alacant, Alicante (España)
martazayas@live.com
___
RESUMEN
Objetivo: Evaluar la efectividad de galcanezumab en práctica real mediante la reducción en el número de migrañas al mes y la reducción en la puntuación del cuestionario de calidad de vida especifico de migraña HIT-6, utilizando una variable combinada. Los objetivos secundarios son, establecer correlación entre la disminución en el número de migrañas al mes y el resultado obtenido en el cuestionario HIT-6, evaluar la efectividad de galcanezumab en migraña crónica y migraña episódica, en pacientes con y sin abuso de medicación y en combinación con otros tratamientos preventivos y evaluar la mejoría en la percepción de los pacientes respecto a la intensidad del dolor.
Material y método: Estudio observacional, prospectivo y multidisciplinar, en un hospital de tercer nivel, en pacientes diagnosticados de migraña que inicien tratamiento con galcanezumab en el periodo de un año.
Se incluirán todos los pacientes mayores de edad, con 8 o más días de migraña al mes y tres o más fracasos de tratamientos previos durante al menos 3 meses, siendo uno de estos tratamientos toxina botulínica en el caso de migraña crónica y que hayan recibido al menos una dosis de galcanezumab, según criterios de financiación. Los pacientes deben presentar capacidad funcional para completar correctamente el diario de migrañas y el cuestionario HIT-6.
La variable principal es la efectividad del tratamiento medida como el porcentaje de pacientes con reducción de al menos el 30% en el número de migrañas al mes 3 desde el inicio del tratamiento o reducción de al menos 5 puntos en el cuestionario HIT-6 durante los 3 primeros meses de tratamiento respecto al valor basal.
La recogida de variables se realizará mediante la historia clínica informatizada y un diario de migrañas. El paciente indicará los días de administración, el número de días de migrañas y su intensidad, y el número de días de consumo de tratamiento sintomático.
El análisis estadístico se realizará con el programa informático Stata®. Se utilizará la prueba Chi-cuadrado para la comparación de variables categóricas. En el tratamiento de los datos continuos, si cumplen normalidad, se utilizará ANOVA. Si, por el contrario, no se cumple dicha condición se aplicará la prueba no paramétrica U de Mann-Whitney.
Palabras clave: Migraña, tratamiento preventivo, anticuerpo monoclonal.
Research project protocol: effectiveness and safety of galcanezumab in patients with migraine. Results in habitual clinical practice
SUMMARY
Goals: The main objective of the study is to evaluate the effectiveness of galcanezumab in real practice according to the reduction in the number of migraines per month and the reduction in the score of the HIT-6 an specific quality of life questionnaire for migraine, using a combined variable. The secondary objectives of the study are to establish a correlation between the decrease in the number of migraines per month and the result obtained in the HIT-6 questionnaire, to evaluate the different behavior regarding the effectiveness of galcanezumab in chronic migraine and episodic migraine in patients with and without medication abuse and in combination with other preventive treatments and finally, to evaluate the improvement in the perception of the patients according to the intensity of the pain.
Method: Observational, prospective and multidisciplinary study in patients diagnosed with migraine in a third line hospital who started treatment with galcanezumab within one year period.
All elderly patients diagnosed with migraine will be included, with 8 or more days of migraine per month and three or more failures of previous treatments for at least 3 months, one of these being botulinum toxin in chronic migraine cases and that have received at least one dose of galcanezumab, based on funding criteria. Patients must present functional capacity to correctly complete the migraine diary and the specific HIT-6 migraine quality of life questionnaire.
The main variable of the study is the effectiveness of the treatment measured as the percentage of patients with a reduction of at least 30% in the number of migraines at month 3 from the start of treatment or a reduction of at least 5 points in the HIT-6 questionnaire during the first 3 months of treatment compared to baseline.
The collection of variables will be carried out through the computerized clinical history and a migraine diary, where the patient will indicate the day of administration of all 6 doses of galcanezumab, the number of days of migraines and their intensity, and the number of days of consumption of symptomatic treatment.
Stata® software will be used for statistical analysis. In the comparison of categorical variables, the Chi-square test will be used. In the treatment of continuous data, the normality condition will be checked, if it is fulfilled, ANOVA will be used for comparison. If, on the other hand, this condition is not fulfilled, the non-parametric Mann-Whitney U test will be applied.
Key words: Migraine, preventive treatment, monoclonal antibody.
___
INTRODUCCIÓN
Antecedentes y justificación
La migraña es una cefalea primaria caracterizada por episodios incapacitantes de dolor, con duración de 4h a 72h, que se acompaña de hipersensibilidad a estímulos ambientales y síntomas gastrointestinales y autonómicos. La cefalea suele ser de intensidad moderada a grave, unilateral y pulsátil, empeorando con la actividad física; suele acompañarse de náuseas, fonofobia y fotofobia1.
Con respecto al impacto que tiene tanto a nivel personal como en términos socioeconómicos, la migraña es la sexta enfermedad más prevalente de acuerdo al Estudio de la Carga Global de las Enfermedades 2016, y en términos de años de vida vividos con discapacidad ocupa el segundo lugar, suponiendo una especial carga para las mujeres jóvenes y adultas2. A pesar de ser una enfermedad con síntomas transitorios, representa un importante problema de salud, por su alta prevalencia y por la limitación para la realización de las actividades habituales durante las crisis, tanto en pérdida de días de trabajo y asistencia a la escuela como en la reducción de la productividad en las funciones laborales y pérdida de tiempo en actividades no laborales3,4.
El abordaje terapéutico se fundamental en el tratamiento sintomático de las crisis de migraña y en el tratamiento preventivo. Por un lado, el objetivo del tratamiento sintomático es recuperar el estado funcional del paciente y se puede dividir en inespecífico (analgésicos y AINE), específico (triptanes o ergóticos) y coadyuvante (antieméticos y procinéticos)5. Por otro lado, el tratamiento preventivo tiene como objetivo, reducir la frecuencia, severidad y duración de las crisis, mejorar la respuesta al tratamiento agudo, mejorar la funcionalidad del paciente, reducir la discapacidad y prevenir la progresión de la migraña episódica a la crónica6. Según las últimas guías de práctica clínica, los tratamientos preventivos incluyen, betabloqueantes, antiepilépticos, bloqueantes de canales de calcio, etc.7
Recientemente se han incorporado al arsenal terapéutico disponible para la profilaxis de la migraña tres anticuerpos monoclonales (erenumab8, galcanezumab9 y fremanezumab10) que pertenecen a una nueva familia de fármacos antimigrañosos dirigidos al receptor del péptido relacionado con el gen de la calcitonina (CGRP) o su ligando. Dichos fármacos han sido financiados en casos de 8 o más días de migraña/mes (migraña episódica de alta frecuencia y en pacientes con migraña crónica) y tres o más fracasos de tratamientos previos utilizados a dosis suficientes durante al menos 3 meses, siendo uno de estos tratamientos toxina botulínica en el caso de migraña crónica.
Justificación
Gracias a los nuevos anticuerpos monoclonales, el impacto de la migraña en la capacidad de estos pacientes para desarrollar su trabajo, sus tareas en el hogar o en situaciones sociales puede mejorar considerablemente, según reflejan los estudios pivotales.
El ensayo EVOLVE-111,12 evaluó la eficacia de galcanezumab en migraña episódica y demostró que las puntuaciones de funcionamiento diario (medidos con el cuestionario MSQ (Migraine-Specific Quality of Life Questionnaire)) aumentaron con galcanezumab en un rango de 4,7 a 8,3 puntos en comparación con placebo (un cambio positivo en las puntuaciones refleja una mejora funcional). La media mensual de días de migraña se redujo 4,3 días con galcanezumab 120 mg y 2,3 días con placebo (p<0,001). La migraña crónica se estudió en el ensayo REGAIN13 donde también se demostró una mejoría de los resultados reportados por el paciente cuantificados por los cuestionarios MSQ y MIDAS (Migraine Disability Assessment)14. También se observó una mejoría en la reducción de días de migraña al mes, 4,8 días en el tratamiento con galcanezumab 120 mg frente a 2,7 días con placebo (p<0,001).
Dichos estudios se realizaron en condiciones ideales y bajo estas circunstancias, se les otorga validez universal, no obstante, dichas condiciones no suelen coincidir con las condiciones de uso real y hasta la fecha, los datos en vida real sobre la efectividad y seguridad de los anticuerpos monoclonales que antagonizan la acción del CGRP son limitados e incipientes.
Objetivos del estudio
El objetivo primario del estudio es evaluar la efectividad en práctica real de galcanezumab en el tratamiento preventivo de pacientes diagnosticados de migraña tanto episódica como crónica, mediante una variable combinada que tenga en cuenta tanto la reducción de número de migrañas al mes (NMM) como el incremento de la calidad de vida, mediante el cuestionario Headache Impact Test-6 (HIT-6).
Como objetivos segundarios se desea evaluar la seguridad de galcanezumab, establecer la correlación entre la disminución del NMM y el resultado obtenido el cuestionario HIT-6, el comportamiento diferente respecto a la efectividad del galcanezumab en migraña crónica y migraña episódica, la efectividad del galcanezumab entre los pacientes que presentan abuso a medicación y los que no presentan abuso, y por último la efectividad del galcanezumab en el tratamiento preventivo de la migraña en monoterapia y en combinación con otro tratamiento preventivo.
MATERIAL Y MÉTODOS
Diseño del estudio
Estudio observacional, prospectivo y multidisciplinar, en un hospital universitario de tercer nivel, llevado a cabo en pacientes diagnosticados de migraña según los criterios International Headache Society IHS1, que inicien tratamiento con galcanezumab en el período comprendido desde mayo de 2021 a mayo de 2022. El estudio se ha diseñado para comparar los resultados de las diferentes variables a los 3 y 6 meses de tratamiento con respecto la situación basal de los pacientes.
El seguimiento de los pacientes se realizará durante los seis primeros meses de tratamiento. La administración y/o recogida del fármaco, así como la recogida de variables, se realizará según se detalla en el cronograma presentado en la tabla 1.
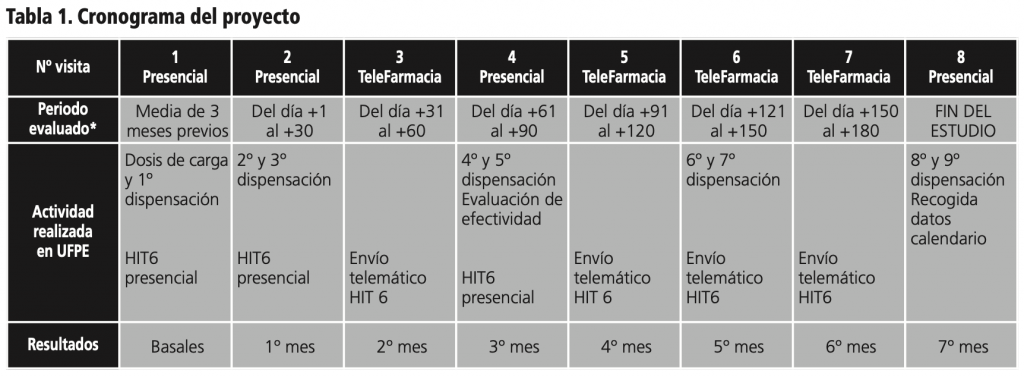
Se programarán 7 visitas de seguimiento, que se realizarán mensualmente. En las visitas 1 y 7, se realiza la valoración inicial y final de forma presencial por parte del servicio de neurología y farmacia. La visita 2 será presencial en la Unidad de Atención Farmacéutica a Pacientes Externos (UFPE) del Servicio de Farmacia, donde se verificará que el paciente registra correctamente las variables en el diario de migrañas. En la visita 4, también presencial, se valorará por el Servicio de Farmacia la efectividad al tercer mes de tratamiento según los criterios definidos por el equipo investigador y se remitirá a Neurología en caso de no respuesta y/o efectos adversos. Además de ello, para autoevaluar la gradación definida, se preguntará al paciente sobre la percepción que él mismo tiene acerca de la efectividad del tratamiento.
Las visitas 3, 5 y 6 se realizarán en Farmacia mediante telefarmacia, de manera que se realizará la consulta y entrevista de forma telefónica. La dispensación se llevará a cabo en la ventanilla de seguridad del Servicio de Farmacia habilitada a tal efecto.
Criterios de inclusión y exclusión
Se incluirán en el estudio todos los pacientes con migraña crónica o episódica que inicien tratamiento con galcanezumab según pauta posológica establecida en ficha técnica dosis de carga inicial de 240 mg subcutáneo, seguido de 120 mg subcutáneo al mes) durante el periodo de reclutamiento, con edad ≥18 años y cumpliendo los criterios definidos por la comisión de farmacia del hospital, que coinciden con las condiciones de financiación establecidas por el Ministerio de Sanidad, Consumo y Bienestar Social9. Además de ello, los pacientes deben presentar buena capacidad funcional y cognitiva para completar correctamente el diario de migrañas y el cuestionario específico de calidad de vida en migraña HIT-6. Se excluirán del estudio los pacientes tratados con galcanezumab en condiciones diferentes a las indicadas anteriormente.
Se ofrecerá participar a todos los pacientes que cumplan los criterios de inclusión. Por los datos históricos se espera incluir aproximadamente 50 pacientes durante el periodo que dura el estudio.
Variables a analizar
La variable principal de estudio es la efectividad del tratamiento, medida a través de una variable combinada que tiene en cuenta el porcentaje de pacientes con reducción de al menos el 30% en el NMM al mes 3 o reducción de al menos 5 puntos en el cuestionario HIT-6 durante los 3 primeros meses de tratamiento respecto al valor basal.
Se establecen los siguientes grados de efectividad, definidos arbitrariamente por consenso en el seno del equipo investigador (tabla 2).

El resto de variables del estudio se recogen en la tabla 3.
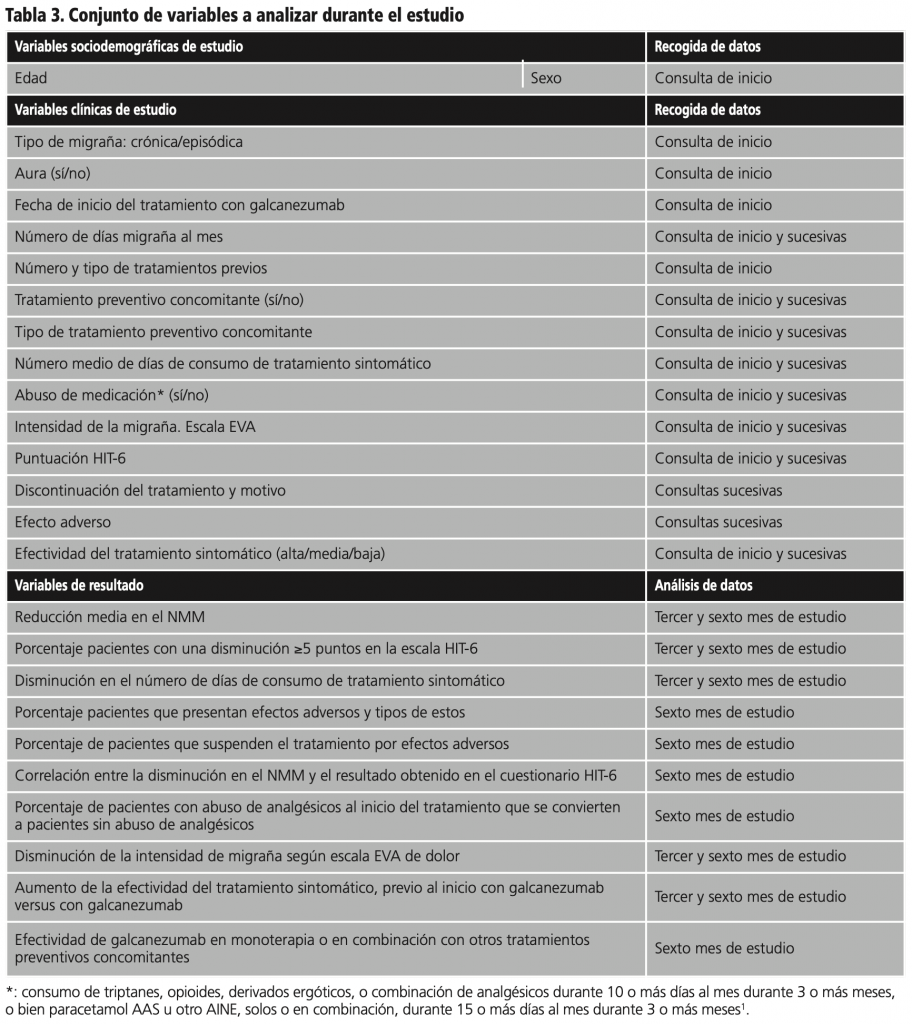
Recogida de información
Las variables clínicas basales (tipo de migraña, presencia de aura, número de tratamientos preventivos previos, descripción de otros tratamientos preventivos, tratamiento preventivo concomitante con galcanezumab) serán valoradas por Neurología y registradas en su historia clínica.
El resto de variables serán recogidas por el Servicio de Farmacia según se detalla en la tabla 3. Para la recogida de variables se hará uso de un diario de migrañas entregado al paciente en la primera visita. Deberá indicar el día de administración de cada una de las 6 dosis de galcanezumab, el NMM y su intensidad, mediante una escala EVA del 1 al 10, así como los días de consumo de tratamiento sintomático. El NMM y el número de días de consumo de analgésicos se recogerá desde los tres meses previos al inicio del tratamiento hasta el mes 6 de tratamiento (día -90 al día +180). El resto de variables se recogerán desde el día del inicio hasta el mes 6 de tratamiento (día 0 al día +180). Los datos se recogerán cada vez que el paciente acuda presencialmente a la consulta de UFPE según se detalla en el cronograma de la tabla 1.
Para la valoración del impacto en la capacidad para desarrollar actividades laborales, domésticas y en el entorno social, se utilizará el cuestionario específico HIT-6 (Anexo I), que se facilitará al paciente en formato electrónico o en papel según preferencia, y que el propio paciente se autoadministrará previo al inicio del tratamiento y durante todos los meses que dura el estudio.
Respecto a la seguridad, se recogerán datos de la entrevista realizada al paciente durante la dispensación del fármaco en la UFPE bien presencial o telefónicamente según práctica asistencial requerida (con periodicidad mensual o bimestral según se especifica en cronograma) (tabla 1), quedándose esta información registrada en el programa de dispensación MDIS-Abucasis. Se accederá a la historia clínica del paciente para consultar el registro de efectos adversos en la valoración por parte de Neurología en cada visita médica.
A los tres meses del inicio del tratamiento, en una consulta presencial, se valorará la eficacia del tratamiento según los criterios establecidos por consenso entre el grupo investigador (tabla 2). Se dejará constancia de ello en la historia clínica del paciente y en caso de que el tratamiento no sea efectivo se realizará interconsulta al Servicio de Neurología para valorar la necesidad de continuación del tratamiento.
El análisis de los datos se realizará por los investigadores, seis meses después de último paciente incluido en el estudio, utilizando para ello las variables recogidas por el propio paciente a través del diario de migrañas.
Métodos estadísticos
Para el análisis estadístico se utilizará el programa informático Stata®.
Las variables cualitativas se expresarán como frecuencia absoluta y relativa (porcentaje). Para las cuantitativas, se obtendrán la media y su desviación estándar, la mediana, el máximo y mínimo y los cuartiles primero y tercero.
Para la comprobación de la normalidad de las variables se utilizará el test de Kolmogorov-Smirnov (con la corrección de Lillieforms). La evaluación en la disminución en el día de migrañas a los 3 y 6 meses respecto al valor basal, se realizará utilizando pruebas no paramétircas de muestras realacionadas (Test U de Mann-Whitney). Para la determinación de la correlación entre la reducción en el número de días de migraña y la puntuación obtenida en el cuestionario HIT-6 se utilizará la prueba de correlación de Spearman.
La compraración de la efectividad entre subgrupos se llevará a cabo mediante el test de Wilcoxon.
El nivel de significación utilizado en todos los contrastes de hipótesis será ≤0,05.
No se plantea cálculo de tamaño muestral ya que se trata de un estudio observacional.
Consideraciones éticas y aprobación ética de la investigación
Este estudio ha sido aprobado y clasificado como estudio post-autorización observacionales de seguimiento prospectivo con medicamentos (EPA-SP) por el Comité Ético de Investigación Clínica en Medicamentos del Hospital Universitario de Elda con fecha del 26 de abril de 2021. Actualmente se encuentra en revisión por el Comité Autonómico de Evaluación de Estudios Post-autorización Observacionales de seguimiento prospectivo con medicamentos (CAEPO) y pendiente de su aprobación.
Se realizará anonimización de datos, asignando un número ordinal a cada número de historia, con el fin de impedir la reidentificación de los pacientes. Los datos se desvincularán de este modo de la identificación de los pacientes y serán tratados estadísticamente. La base de datos se conservará en un ordenador corporativo protegido con contraseña.
Consentimiento informado. En el momento del reclutamiento, se entregará al paciente una hoja de información donde se le explicará el propósito del estudio y cómo se pretende llevar a cabo, debiendo firmar un consentimiento informado antes de ser admitido en el estudio clínico. El paciente podrá retirar el consentimiento en cualquier momento.
DISCUSIÓN
Mediante este estudio, se pretende conocer los resultados de efectividad y seguridad obtenidos en nuestro ámbito y evaluar si son coherentes con los descritos en otros estudios de vida real publicados hasta la fecha15-18 así como los obtenidos en los ensayos clínicos.
Detke y cols.13 establecieron la efectividad como una reducción de al menos el 50% en el NMM. Obtuvieron alrededor de un 50% de pacientes respondedores en tratamiento con galcanezumab tanto a dosis de 120 mg/mes como de 240 mg/mes, coincidiendo con el estudio de Robbins y cols.15
Tanto en los estudios EVOLVE 1-211,12 como en REGAIN13, utilizan como variable secundaria para medir la eficacia los cambios con respecto al valor inicial en el cuestionario de calidad de vida específico para la migraña MSQ y la evaluación de la discapacidad por migraña (MIDAS)11-13. En nuestro caso, hemos optado por utilizar el cuestionario de calidad de vida específico para pacientes con migraña HIT-6, por su menor complejidad. Dicho cuestionario ha sido utilizado en otros estudios en vida real, como el realizado por Vernieri16, Ornello17 y Lambru18.
Otra diferencia importante con los estudios pivotales EVOLVE 1-2 y REGAIN es que, en éstos, los pacientes con más de 3 tratamientos preventivos ineficaces, pacientes en tratamiento con galcanezumab en combinación con otro tipo de tratamientos preventivos y pacientes que presentasen abuso de medicación estuvieron poco representados. Dichos subgrupos sí se han estudiado en otros estudios en vida real como el estudio GARLIT16. Debido a la gran variedad de características que acompañan a los pacientes con migraña, se considera necesario evaluar el impacto de dichas variables para definir qué tipo de pacientes son los que mayor beneficio pueden obtener.
Aunque el objetivo principal de los anticuerpos monoclonales utilizados en la prevención de la migraña es la reducción del número de días de migraña, según nuestra experiencia, existen otros aspectos muy valorados por el paciente (como la reducción en la intensidad de las migrañas que les permita levantarse de la cama o ir al trabajo, en el mejor de los casos) que nos orientan a pensar que la efectividad de estos tratamientos debería medirse no sólo mediante la reducción en el número de días de migraña al mes, sino de una manera más holística, teniendo en cuenta el beneficio que estos tratamientos tienen sobra la funcionalidad, la esfera afectivo-emocional y la percepción de los propios pacientes sobre su estado de salud. De ahí que, en el seno del grupo investigador, se plantease la utilización de una variable combinada que incluya tanto la reducción cuantitativa de los días de migraña como la valoración de la calidad de vida, lo que supone una aproximación novedosa al problema (con todas las limitaciones que pueda conllevar).
Por último, en la bibliografía19 se evidencia que la falta de respuesta temprana predice el curso subsiguiente de la enfermedad, por lo que es necesario evaluar de forma precoz al paciente para decidir la continuación y/o modificación del tratamiento. No obstante, la sobrecarga asistencial hace en muchas ocasiones imposible la valoración de la respuesta temprana por parte de los equipos de neurología, lo que lleva no solo a que un paciente reciba durante meses un tratamiento ineficaz, sino también a la adición de toxicidad y al derroche en el gasto farmacéutico. En este sentido, la cooperación y coordinación entre el Servicio de Neurología y Farmacia es una fortaleza. Dado que el paciente contacta con el Servicio de Farmacia mensual o bimestralmente, bien sea telefónica o presencialmente, se decidió que esta valoración inicial (a los tres meses tras inicio del tratamiento) se hiciese por los farmacéuticos de la UFPE, que ante la incipiente falta de respuesta derivarán al paciente al Servicio de Neurología mediante interconsulta para valorar suspensión o continuación del tratamiento, según sea el caso.
Limitaciones. Una de las principales limitaciones del estudio es que el registro de las variables que nos permiten el cálculo tanto del resultado principal como de los secundarios, las realiza el paciente en su casa, y a pesar de las diferentes visitas programadas que permiten revisar la correcta cumplimentación del diario de migrañas, pensamos que esto llevará a la obtención de datos faltantes a la hora de analizar los resultados. Por otra parte, y dado que se trata de un estudio antes-después, resulta esencial conocer los datos basales, lo que plantea un problema, no tanto en el número de días de migraña medio basal, requisito indispensable a conocer para su financiación, sino para variables como el número de días medio de consumo de analgésicos basal, lo cual imposibilita hacer un cálculo en la reducción de su utilización tras el inicio de tratamiento con galcanezumab en la mayoría de los casos.
Además, el diseño antes-después del estudio, no permite la comparación del impacto de galcanezumab frente al tratamiento estándar (ej. tratamiento preventivo convencional), lo que supone otra importante limitación del trabajo.
Por último, se trata de un estudio unicéntrico, en el que se espera reclutar un número limitado de pacientes, por lo que las conclusiones pueden no ser generalizables.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
BIBLIOGRAFÍA
1. Headache Classification Committee of the International Headache Society (IHS) The International Classification of Headache Disorders, 3rd edition. Cephalalgia. 2018;38(1):1-211.
2. Stovner LJ, Nichols E, Steiner TJ, Abd-Allah F, Abdelalim A, Al-Raddadi RM, et al. Global, regional, and national burden of migraine and tension-type headache, 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. The Lancet Neurology. 2018;17(11):954-76.
3. Reuter U. GBD 2016: still no improvement in the burden of migraine. The Lancet Neurology. 2018;17(11):929-30.
4. Fernández Concepción O, Canuet Delis L. Discapacidad y calidad de vida en pacientes con migraña: Factores determinantes. RevNeurol. 2003;36(12):1105.
5. Macaya Ruiz A, Pozo-Rosich P. Guía práctica diagnóstico terapéutica de la cefalea del adulto y el niño en urgencias. Madrid: Luzán 5; 2016.
6. Lipton RB, Bigal ME, Diamond M, Freitag F, Reed ML, Stewart WF, et al. Migraine prevalence, disease burden, and the need for preventive therapy. Neurology. 2007;68(5):343-9.
7. Ángel Luis Guerrero Peral, Juan Carlos García-Moncó Carrá, Agustín Oterino Durán, Samuel Díaz Insa, Pablo Irimia Sieira. Manual de Práctica Clínica en Cefaleas. Recomendaciones diagnósticoterapéuticas de la Sociedad Española de Neurología en 2020. Luzán 5. Madrid: Sonia Santos Lasaosa, Patricia Pozo Rosich; 2020. 73-137 p.
8. Agencia española de medicamentos y productos sanitarios, Ministerio de sanidad, consumo y bienestar social. Informe de Posicionamiento Terapéutico de erenumab (Aimovig®) en la profilaxis de migraña [Internet]. Madrid; 2019 p. 1-8. Report No.: IPT, 62/2019. V1. Disponible en: https://www.aemps.gob.es/ medicamentosUsoHumano/informesPublicos/docs/IPT-erenumab-Aimovig.pdf?x57618.
9. Agencia española de medicamentos y productos sanitarios, Ministerio de sanidad, consumo y bienestar social. Informe de Posicionamiento Terapéutico de galcanezumab (Emgality®) en la profilaxis de migraña [Internet]. Madrid; 2019 p. 1-11. Report No.: IPT, 63/2019. V1. Disponible en: https://www.aemps. gob.es/medicamentosUsoHumano/informesPublicos/docs/IPT-galcanezumab-Emgality.pdf?x98091.
10. Agencia española de medicamentos y productos sanitarios, Ministerio de sanidad, consumo y bienestar social. Informe de Posicionamiento Terapéutico de fremanezumab (Ajovy®) en la profilaxis de migraña [Internet]. Madrid; 2020 p. 1-10. Report No.: IPT, 11/2020. V1. Disponible en: https://www.aemps.gob. es/medicamentosUsoHumano/informesPublicos/docs/IPT_11-2020-fremanezumab-Ajovy.pdf?x57618.
11. Skljarevski V, Matharu M, Millen BA, Ossipov MH, Kim B-K, Yang JY. Efficacy and safety of galcanezumab for the prevention of episodic migraine: Results of the EVOLVE-2 Phase 3 randomized controlled clinical trial. Cephalalgia. 2018;38(8):1442-54.
12. Stauffer VL, Dodick DW, Zhang Q, Carter JN, Ailani J, Conley RR. Evaluation of Galcanezumab for the Prevention of Episodic Migraine: The EVOLVE-1 Randomized Clinical Trial. JAMA Neurol. 2018;75(9):1080.
13. Holland Detke, Patricia Pozo-Rosich, Uwe Reuter, David Dolezil, Lily Q. Li, Shufang Wang, et al. One-year treatment with galcanezumab in patients with chronic migraine: results from the open-label phase of the REGAIN study. Neurology. 2019;92(15):2.10-010.
14. Martin V, Samaan KH, Aurora S, Pearlman EM, Zhou C, Li X, et al. Efficacy and Safety of Galcanezumab for the Preventive Treatment of Migraine: A Narrative Review. Adv Ther. 2020;37(5):2034-49.
15. Lawrence Robbins. CGRP monoclonal antibodies for chronic migraine: year 1 of clinical use. The author reports on early clinical experience with Emgality and AJOVY, including switching from one CGRP inhibitor to another and future considerations. Pract Pain Manag. 2020;19(6):58-62.
16. Vernieri F, Altamura C, Brunelli N, Costa CM, Aurilia C, Egeo G, et al. Galcanezumab for the prevention of high frequency episodic and chronic migraine in real life in Italy: a multicenter prospective cohort study (the GARLIT study). J Headache Pain. 2021;22(1):35.
17. Ornello R, Casalena A, Frattale I, Gabriele A, Affaitati G, Giamberardino MA, et al. Real-life data on the efficacy and safety of erenumab in the Abruzzo region, central Italy. J Headache Pain. 2020;21(1):32.
18. Lambru G, Hill B, Murphy M, Tylova I, Andreou AP. A prospective real-world analysis of erenumab in refractory chronic migraine. J Headache Pain. 2020;21(1):61.
19. Nichols R, Doty E, Sacco S, Ruff D, Pearlman E, Aurora SK. Analysis of Initial Nonresponders to Galcanezumab in Patients With Episodic or Chronic Migraine: Results From the EVOLVE-1, EVOLVE-2, and REGAIN Randomized, Double-Blind, Placebo-Controlled Studies. Headache: The Journal of Head and Face Pain. 2019;59(2):192-204.
____
