Molina Casabán C1, Sancho Artés A1, Moya-Gil A1, Martín Ureste M2, Maestu Maiques I2, Climente Martí M1
1 Servicio de Farmacia
2 Servicio de Oncología Médica
Hospital Universitario Dr. Peset. Valencia (España)
Fecha de recepción: 04/07/2018 – Fecha de aceptación: 24/07/2018
Correspondencia: Carlos Molina Casabán w Hospital Universitario Dr. Peset (Servicio de Farmacia) w Avda. Gaspar Aguilar, 90 w 46017 Valencia (España)
molinacasaban@gmail.com
____
Resumen
Objetivo: Evaluar efectividad y seguridad de nivolumab en la práctica clínica real y determinar posibles predictores clínicos de una mejor respuesta.
Métodos: Estudio observacional retrospectivo en pacientes con cáncer de pulmón no microcítico en tratamiento con nivolumab en segunda línea o posterior entre agosto-2015 y agosto-2017. Se evaluó la respuesta mediante criterios RECIST v1.1. Variables principales de efectividad: tasa de respuesta objetiva (TRO) y supervivencia global (SG); variables secundarias: supervivencia libre de progresión (SLP), mejor respuesta global (MRG), duración de la respuesta (DR) y tiempo hasta respuesta (TR).
Los posibles factores predictores (edad, sexo, estadío, histología, ECOG-PS y líneas previas) de mejor respuesta se analizaron mediante un modelo de riesgos proporcionales de Cox y TRO mediante odds ratio. Los eventos adversos (EA) se clasificaron según CTCEA v4.3.
Resultados: 29 pacientes, edad mediana 67 años (rango 37-78), hombres (59%), ECOG-PS 0-1 (93%) y estadío IV (83%). TRO=21% (IC95% 10-38). Mediana SG 12,1 meses (IC95% 4,7-19,5) y SLP 4,2 meses (IC95% 1,4-10,5). MRG fue respuesta parcial (RP) para seis pacientes (21%). Medianas de DR y TR fueron 3,6 meses (rango 4,2-16,2+) y 4,4 meses (rango 1,3-4,7), respectivamente. Ninguna de las variables analizadas se identificó como factor predictor de mejor respuesta. Once pacientes (38%) presentaron al menos un EA G3-G4, en tres (10%) fue necesaria la suspensión del fármaco.
Conclusiones: Nivolumab tuvo una eficacia similar a la demostrada en ensayos clínicos, no identificándose variables predictoras de mejor respuesta. La seguridad del tratamiento fue aceptable, suspendiéndose por EA en el 10% de los pacientes.
Palabras clave: Nivolumab, cáncer pulmón no microcítico, efectividad, seguridad.
____
Introducción
El cáncer de pulmón (CP) supone un problema de salud de primer orden por su elevada incidencia y mortalidad. En el año 2012 se diagnosticaron en España 26.715 nuevos casos de CP. La mortalidad de CP ese mismo año fue de 21.118, constituyendo el 21% de todas las muertes por cáncer1.
El cáncer de pulmón no microcítico (CPNM) es el tipo más frecuente de CP2. El tratamiento de elección ha consistido clásicamente en un doblete de quimioterapia basada en platino3. Sin embargo, en los últimos años el mejor conocimiento de la biología molecular de estos tumores ha ampliado el número de dianas y, por tanto, de opciones terapéuticas disponibles4. En este contexto, la inmunoterapia, con distintos fármacos activos, ha supuesto una revolución en la estrategia terapéutica del CPNM. Uno de ellos es nivolumab, un anticuerpo monoclonal humano que se une al receptor de muerte programada PD-1 de linfocitos T y bloquea su interacción con PDL-1 y PDL-2, potenciando así la respuesta antitumoral de los linfocitos T contra las células tumorales5.
Nivolumab fue autorizado por la EMA en 2015 para pacientes con CPNM escamoso, y en 2016 en CPNM no escamoso, para tumores avanzados o metastásicos tras quimioterapia previa, administrándose una dosis de 3 mg/Kg cada 2 semanas6. Las guías de práctica clínica (European Society of Medical Oncology y American Society of Clinical Oncology; ESMO y ASCO) han situado a nivolumab en segunda línea en CPNM para pacientes con determinación negativa de ALK y EGFR y que mantienen un Eastern Cooperative Oncology Group performance status (ECOG-PS) igual a 0-1, incluso si la determinación de PDL-1 es negativa o desconocida3,7. Este posicionamiento terapéutico ha convertido a nivolumab en un fármaco de uso habitual en el abordaje del CPNM.
La eficacia y seguridad clínica de nivolumab fue evaluada frente a docetaxel en CPNM escamoso (CheckMate 017) y no escamoso (CheckMate 057). Se obtuvo una mejora estadísticamente significativa en la supervivencia global (SG), tanto en histología escamosa (9,2 vs. 6,0 meses) como no escamosa (12,2 vs. 9,4 meses). En cuanto a seguridad, nivolumab mostró un buen perfil de toxicidad. En CPNM escamoso solo el 2% de los pacientes presentó eventos adversos (EA) grado 3-4 relacionados con el tratamiento y únicamente un 3% suspendió el tratamiento por EA. Para la histología no escamosa, estos resultados fueron de 15% y 5%, respectivamente8,9.
Sin embargo, estos estudios no incluyeron a pacientes con peor pronóstico al tener criterios de exclusión restrictivos como: ECOG ≥2, metástasis cerebrales activas, cualquier trastorno médico grave y/o no controlado así como valores analíticos anormales. Esta selección de pacientes dificulta la extrapolación de los resultados a la práctica clínica real.
En este contexto, se plantea este estudio con el objetivo de evaluar la efectividad y el perfil de seguridad de nivolumab en la práctica clínica real, así como determinar posibles predictores clínicos de una mejor respuesta.
MATERIAL Y MÉTODOS
Estudio observacional retrospectivo, en el que se incluyeron todos los pacientes diagnosticados de CPNM que fueron tratados con nivolumab entre agosto de 2015 y agosto de 2017 en un hospital terciario. Se excluyeron los pacientes que sólo recibieron un ciclo de nivolumab. El seguimiento de los pacientes finalizó el 28 de diciembre de 2017.
Se registraron características basales asociadas al paciente y a la enfermedad (edad, sexo, estadío de la enfermedad, histología, grado de expresión de PD-L1 del tumor, ECOG PS y número y tipo de líneas previas de tratamiento) así como variables de efectividad y de seguridad. La fuente de información fue la historia clínica electrónica.
Efectividad: Las variables principales de efectividad fueron la tasa de respuesta objetiva (TRO) y supervivencia global (SG). Variables secundarias: supervivencia libre de progresión (SLP), mejor respuesta global obtenida durante el tratamiento (MRG), duración de la respuesta (DR) y tiempo hasta respuesta (TR).
La evaluación de la respuesta tumoral se evaluó según el protocolo del centro mediante pruebas de imagen con una valoración trimestral, y se clasificó en respuesta completa (RC), respuesta parcial (RP), enfermedad estable (EE) o progresión de la enfermedad (PE) según criterios RECIST v1.1. La TRO se calculó como la proporción de pacientes con una MRG correspondiente a RC o RP. La TRO obtenida se comparó con los resultados agrupados de TRO de los ensayos pivotales CheckMate 017 y CheckMate 057. La SG se calculó como el tiempo desde el inicio hasta muerte o fin de seguimiento. La SLP se calculó como el tiempo entre el inicio hasta progresión tumoral, muerte o fin de seguimiento.
Se analizaron TRO, SG y SLP por subgrupos según las características basales (edad, sexo, estadío de la enfermedad, número de líneas previas, ECOG-PS e histología) para determinar posibles predictores clínicos de una mejor respuesta.
Seguridad: Se registraron todos los EA acontecidos y reflejados en la historia clínica electrónica y se clasificaron según los criterios CTCEA v4.3. El seguimiento de EA se realizó hasta 4 semanas después de la última dosis administrada o el inicio de una línea posterior de terapia antineoplásica. También se calculó el número de retrasos en la administración del fármaco y las suspensiones del tratamiento asociados a EA. El registro de los EA se realizó en la consulta médica previa a la administración del siguiente ciclo de tratamiento.
Análisis estadístico: Las variables categóricas se describieron por frecuencias, y las variables cuantitativas con distribución no normal con la mediana como medida de tendencia central y y rango (mínimo-máximo) o intervalo de confianza. El análisis de supervivencia se realizó mediante el método Kaplan-Meier. Para determinar la relación entre factores predictores y mejor respuesta, la SG y SLP se analizaron mediante un modelo de riesgos proporcionales de Cox y la TRO mediante la medida de asociación de odds ratio (OR). También se realizó un análisis post-hoc de la SG según la MRG mediante la prueba de comparación de supervivencias log-rank test. El análisis estadístico se realizó con el software estadístico Stata 14.2. Se consideró como nivel de significación estadística p<0,05.
RESULTADOS
Se incluyeron 29 pacientes en el estudio con una mediana de edad de 67 años (rango 37-78), siendo el 59% hombres. El 93% presentaban ECOG-PS 0-1 y el 83% enfermedad en estadío IV. En todos los casos, nivolumab se administró en segunda línea o posterior. El 69% había recibido una línea previa de tratamiento, mientras que el 17% había recibido dos. Sólo un paciente había sido tratado previamente con inhibidores de la tirosina-quinasa de EGFR y en ningún caso se administró inmunoterapia previa. El 45% de los tumores fueron de histología escamosa y el 55% no escamosa (Tabla 1).
Nivolumab fue administrado a dosis de 3 mg/kg cada dos semanas hasta progresión de la enfermedad, toxicidad inaceptable, muerte o criterio del equipo médico responsable. A los pacientes incluidos en el estudio se les administró una mediana de 10 ciclos de tratamiento (rango 2-41), sin embargo trece pacientes (45%) recibieron menos de 6 ciclos.
Efectividad
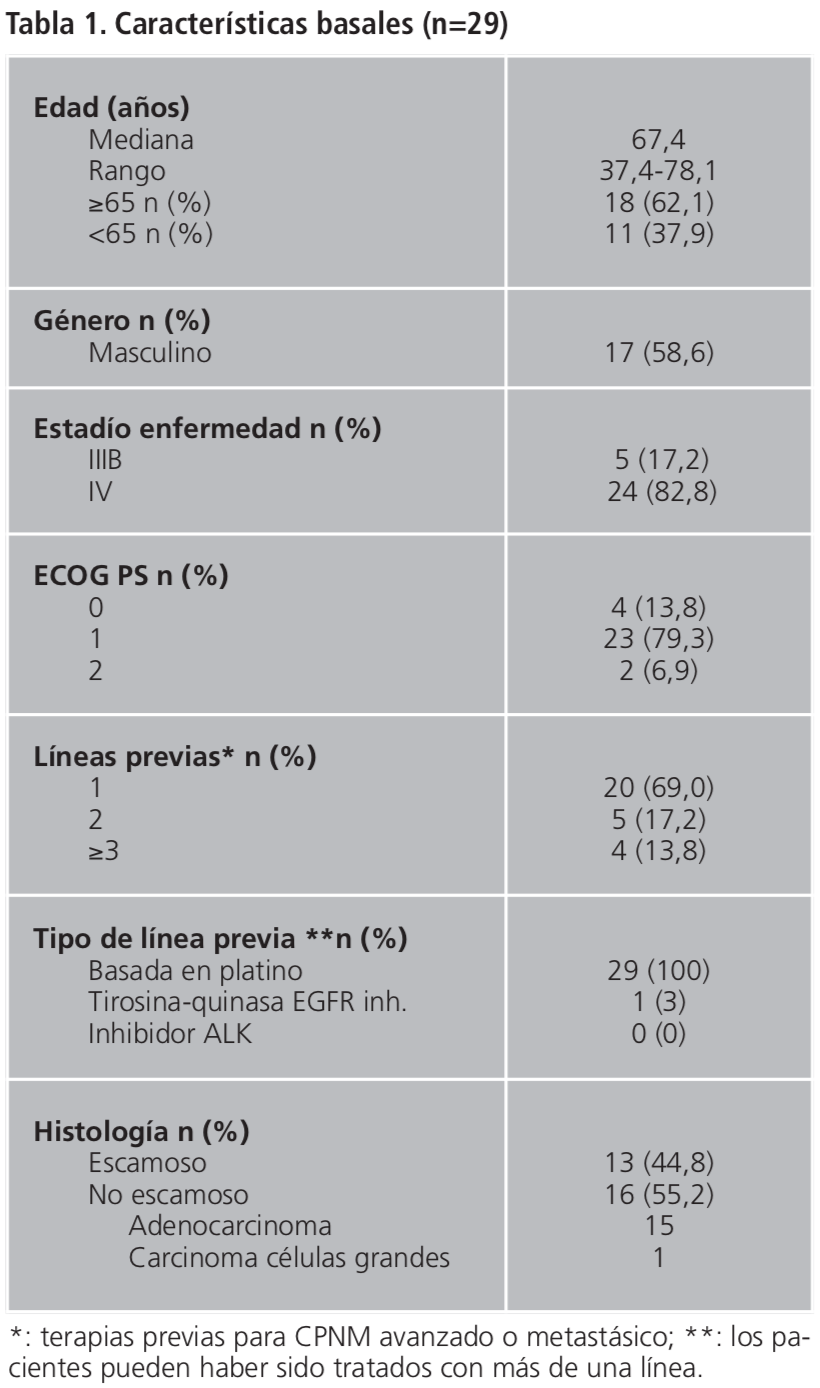
Los resultados de efectividad se muestran en la Tabla 2. La TRO fue de 20,7% (IC95% 10-38). Este resultado no difirió estadísticamente del porcentaje de respondedores obtenido de los datos agrupados de los dos estudios pivotales CheckMate 017 y CheckMate 057 (test χ² p=0,741). La mediana de SG fue de 12,1 meses (IC95% 4,7-19,5) y para SLP resultó de 4,2 meses (IC95% 1,4-10,5) (Figura 1).
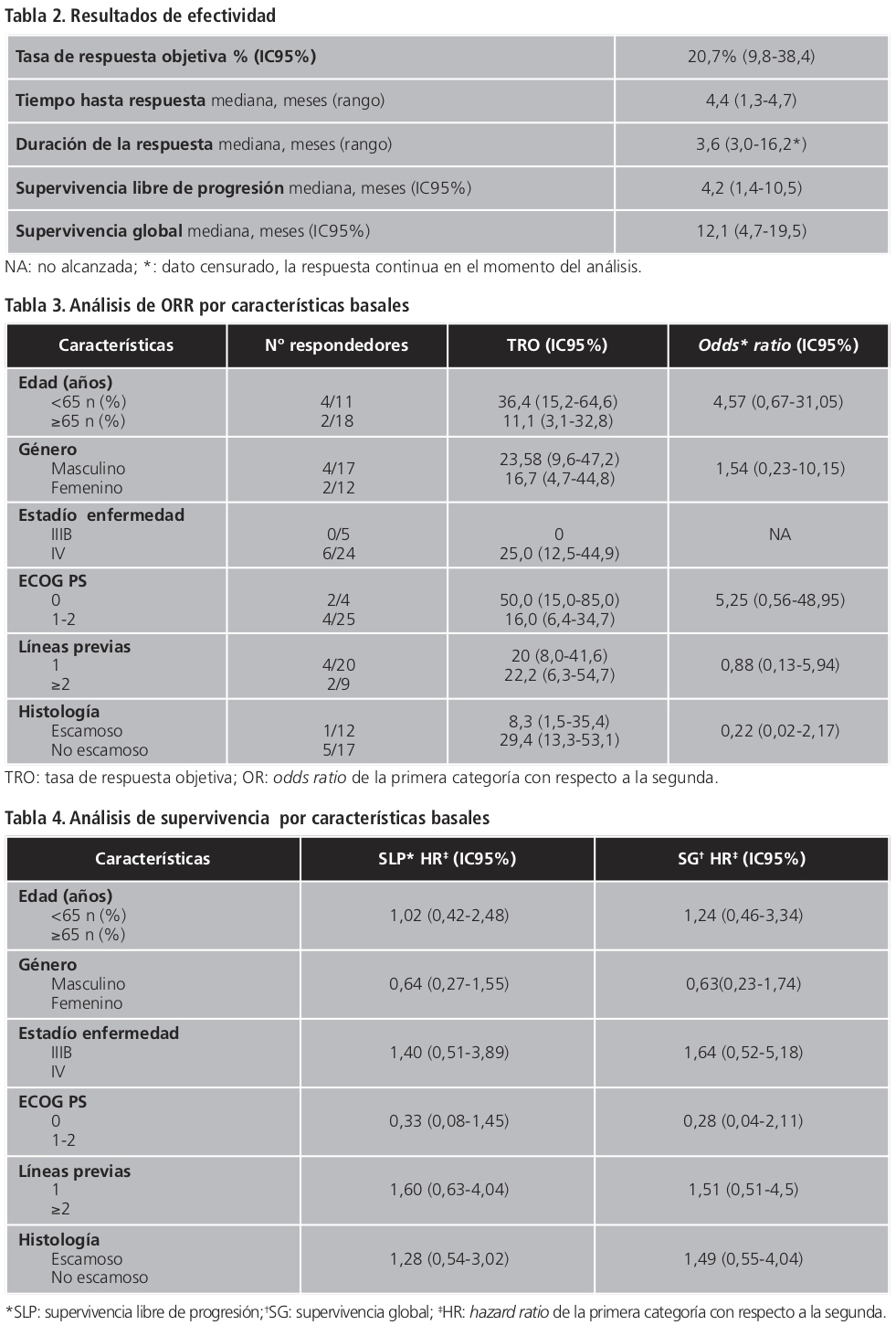
La MRG fue RP para seis pacientes (21%), EE para diez pacientes (35%) y PE para 13 pacientes (45%). Ningún paciente consiguió alcanzar RC. La mediana de DR fue de 3,6 (rango 4,2-16,2+) meses. (El “+” indica dato censurado ya que cuatro de los seis pacientes respondedores mantenían respuesta al finalizar el estudio). La mediana de TR fue de 4,4 meses (rango 1,3-4,7). En la figura 2 se representa la evolución de cada paciente durante el tratamiento.
A cuatro pacientes se les administró nivolumab más allá de la progresión de la enfermedad (rango de administraciones 4-23+), consiguiéndose estabilizar la progresión posteriormente en dos de ellos. (El “+” indica dato censurado porque uno de estos pacientes continuaba en tratamiento).
Al analizar los resultados de efectividad (SG, SLP y TRO) por subgrupos según las características basales (edad, sexo, estadío de la enfermedad, ECOG-PS, histología del tumor y número de líneas previas de tratamiento) no se encontraron diferencias estadísticamente significativas (Tablas 3 y 4). No se realizó análisis exploratorio según grado de expresión de PDL-1 ya que solo se dispuso del dato en tres pacientes, en todos ellos la determinación fue negativa (<1%).
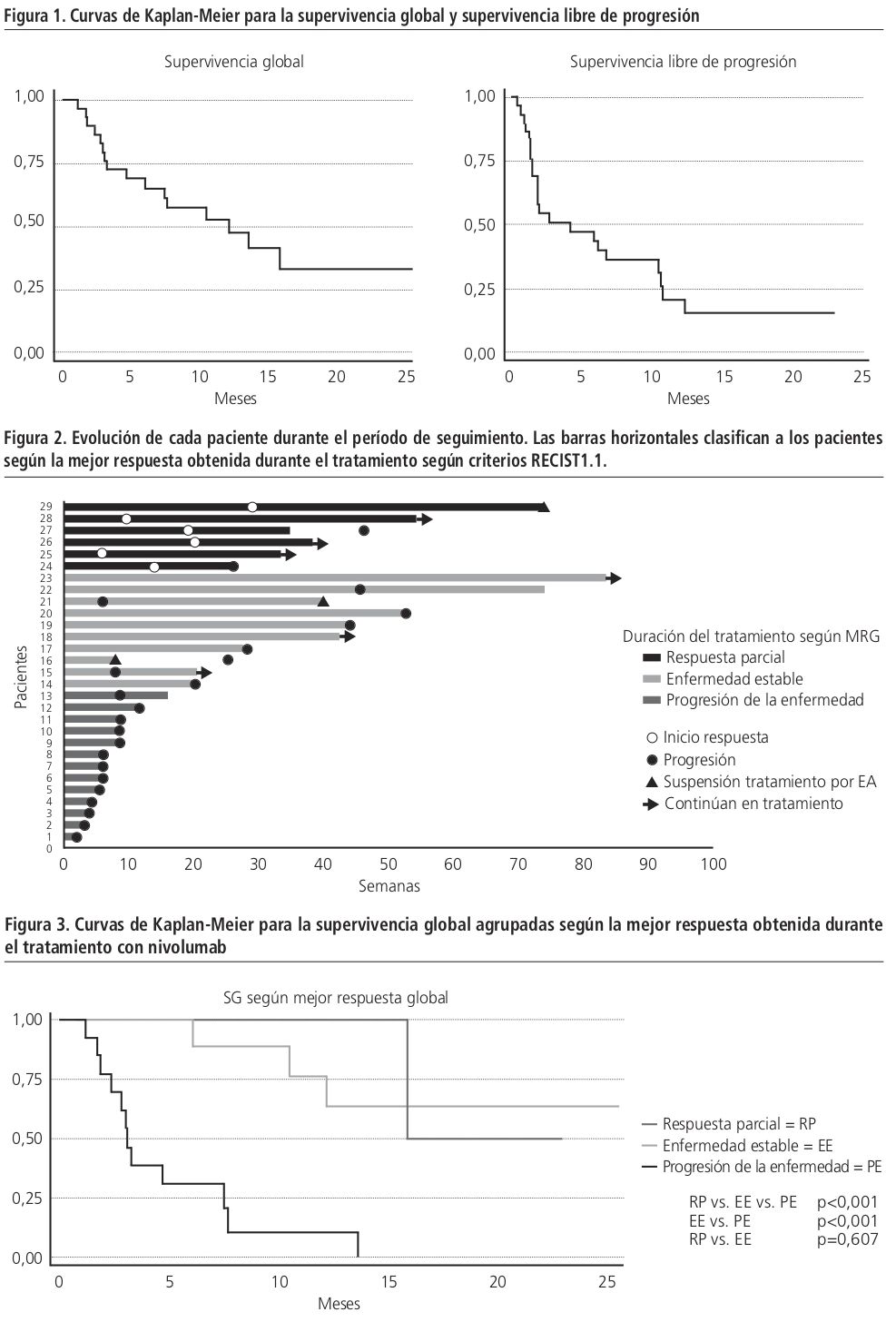
En el análisis post-hoc de la SG en función de la MRG obtenida durante el tratamiento, cuando se estratificaron los pacientes en RP, EE y PE se obtuvieron diferencias estadísticamente significativas (p<0,001). En concreto, el análisis por subgrupos EE y PE fue estadísticamente significativo (p<0,001), a diferencia de EE y RP (p=0,607) (Figura 3).
Seguridad
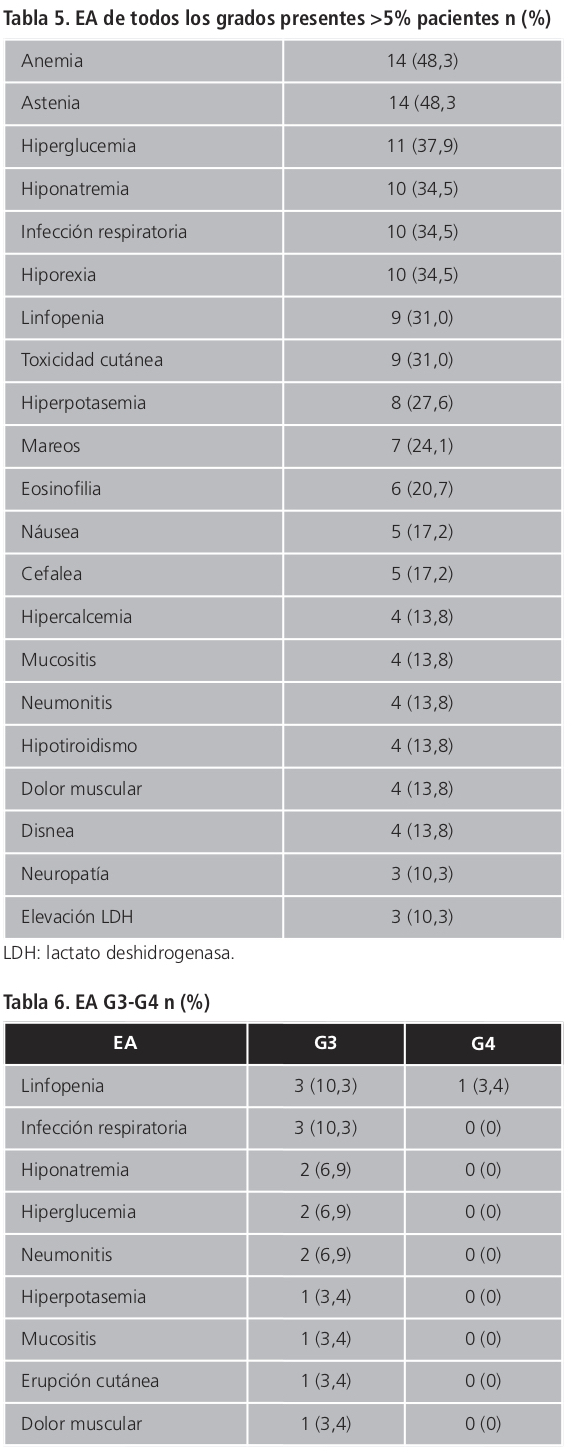
El 97% de los pacientes sufrió algún tipo de EA durante el período de estudio. Astenia y anemia fueron los EA más comunes, ocurriendo en prácticamente la mitad de la población estudiada (48,3%) (Tabla 5). Según la gravedad de los EA, el 90% de los EA fue de grado 1-2, y once pacientes (38%) presentaron al menos un EA G3-4 (Tabla 6). No se registró ningún EA asociado a la infusión. En cuanto a los EA inmunorelacionados, ocurrieron cuatro casos de neumonitis y cuatro casos de hipotiroidismo, siendo necesario iniciar tratamiento con levotiroxina en dos de ellos. De las 379 administraciones, en dieciséis ocasiones (4,2%) se retrasó la administración, correspondiéndose con catorce pacientes (48%). Finalmente, en tres pacientes (10%) fue necesaria la suspensión del tratamiento, dos casos por neumonitis y uno por toxicidad cutánea.
DISCUSIÓN
En nuestra población, la efectividad de nivolumab en pacientes con diagnóstico CPNM fue similar a la obtenida en los ensayos clínicos pivotales randomizados, tanto en SG como en TRO. Esta similitud se relacionó con el CPNM de histología escamosa y no escamosa.
Actualmente, la bibliografía disponible para nivolumab en práctica clínica real muestra gran variabilidad, especialmente en los resultados de SG. Dos estudios multicéntricos en el ámbito europeo mostraron una SG similar a nuestro estudio (15 y 10 meses)10,11. No obstante, en otros estudios de características similares, los resultados en SG fueron inferiores (7,8 y 5,9 meses)12,13, destacando un mayor porcentaje de pacientes con ECOG-PS ≥2 (24% y 46%). En nuestra población, los pacientes con un ECOG-PS ≥2 era tan solo de un 3%, lo que podría explicar la diferencia en SG.
Ninguna de las variables asociadas al paciente o a la enfermedad que se estudiaron en el análisis exploratorio obtuvo significación estadística, probablemente debido al limitado número de pacientes incluidos. A pesar de esta limitación, nuestro estudio parece orientar hacia una mejor SG en pacientes con ECOG-PS=0 frente ECOG-PS ≥1 (HR=0,28). De hecho, varios estudios con mayor número de pacientes (n >200) ya han demostrado la correlación entre un mayor ECOG-PS y una peor SG, sin embargo no consiguieron demostrar relación para otros factores a priori desfavorables como la edad o el número de líneas previas recibidas12-14.
Por otra parte, cabe destacar que en 7 pacientes (24%) a pesar de no alcanzar RP según criterios RECIST obtuvieron beneficio clínico del tratamiento al permanecer la enfermedad estabilizada durante periodos relativamente largos (SLP >20 semanas) (Figura 2). Además en el análisis post-hoc de SG (RP vs. EE) no se obtuvieron diferencias estadísticamente significativas. Esto podría indicar que tanto la RP como la EE podrían ser un objetivo terapéutico en estos pacientes ya que se alcanzan valores en SG similares.
En cuanto a seguridad, nivolumab fue generalmente bien tolerado, siendo la mayor parte de los EA G1-2. No obstante, respecto a los ensayos pivotales, se registró un número mayor de pacientes afectados por EA grado 3-4 (38% vs. 2% en escamoso y 15% en no escamoso) y mayor porcentaje de pacientes que tuvieron que retrasar alguna administración o suspender el tratamiento por toxicidad (10% vs. 3% en escamoso y 5% en no escamoso)8,9.
CONCLUSIONES
Nivolumab tiene una efectividad similar a la mostrada en los ensayos clínicos, con una tasa de respuesta objetiva del 21%, una SG de 12,1 meses y una SLP de 4,2 meses. La respuesta alcanzada con ninguno de los factores predictores alcanzados. Los pacientes que alcanzaron respuesta parcial o enfermedad estable no mostraron diferencias en su supervivencia global. La seguridad del tratamiento fue aceptable, aunque se relaciona con un 10% de suspensiones de tratamiento por EA. Esto sitúa a nivolumab como una opción efectiva frente a CPNM pero con la necesidad de un seguimiento estrecho de los pacientes por los potenciales EA. Sin embargo, nivolumab podría ser una opción inadecuada en pacientes con ECOG ≥2.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
BIBLIOGRAFÍA
1. Globocan 2012: Estimated Cancer Incidence, Mortality and Prevalence Worldwide in 2012. International Agency for Research on Cancer – World Health Organization 2013.
2. Wakelee H, Kelly K, Edelman MJ. 50 Years of progress in the systemic therapy of non-small cell lung cancer. American Society of Clinical Oncology educational book / ASCO. American Society of Clinical Oncology. Meeting 2014:177.
3. Novello S, Barlesi F, Califano R, Cufer T, Ekman S, Levra MG, et al. Metastatic non-small-cell lung cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2016 /09/01;27(suppl_5):v27.
4. Travis WD, Brambilla E, Nicholson AG, Yatabe Y, Austin JHM, Beasley MB, et al. The 2015 World Health Organization Classification of Lung Tumors: Impact of Genetic, Clinical and Radiologic Advances Since the 2004 Classification. Journal of Thoracic Oncology 2015-09-01;10(9):1243-1260.
5. Guo L, Zhang H, Chen B. Nivolumab as Programmed Death-1 (PD-1) Inhibitor for Targeted Immunotherapy in Tumor. J Cancer 2017-2-10;8(3):410-416.
6. Opdivo: EPAR – Procedural steps taken and scientific information after authorisation. 2017; Available at: http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Procedural_steps_taken_and_scientific_information_after_authorisation/human/003985/WC500197949.pdf.
7. Hanna N, Johnson D, Temin S, Baker S, Brahmer J, Ellis PM, et al. Systemic Therapy for Stage IV Non-Small-Cell Lung Cancer: American Society of Clinical Oncology Clinical Practice Guideline Update. J Clin Oncol. 2017 Oct 20;35(30): 3484-3515.
8. Borghaei H, Paz-Ares L, Horn L, Spigel DR, Steins M, Ready NE, et al. Nivolumab versus Docetaxel in Advanced Nonsquamous Non-Small-Cell Lung Cancer. The New England Journal of Medicine. 2015 Oct 22;373(17):1627-1639.
9. Brahmer J, Reckamp KL, Baas P, Crinò L, Eberhardt WEE, Poddubskaya E, et al. Nivolumab versus Docetaxel in Advances Squaous-Cell Non-Small-Cell Lung Cancer. The New England Journal of Medicine. 2015(1):35-38.
10. Geier M, Descourt R, Quéré G, Corre R, Leveiller G, Lamy R, et al. P2.07-030 Real Life Second-Line Nivolumab in Advanced Non-Small-Cell-Lung Cancer: A French Observational Multicenter Study of 259 Patients. Journal of Thoracic Oncology. 2017-11-01;12(11):S2427.
11. Schouten RD, Muller M, Gooijer CJd, Baas P, Heuvel Mvd. Real life experience with nivolumab for the treatment of non-small cell lung carcinoma: Data from the expanded access program and routine clinical care in a tertiary cancer centre-The Netherlands Cancer Institute. Lung Cancer. 2017-11-16;0(0).
12. Tournoy KG, Thomeer M, Germonpré P, Derijcke S, De Pauw R, Galdermans D, et al. Does nivolumab for progressed metastatic lung cancer fulfill its promises? An efficacy and safety analysis in 20 general hospitals. Lung Cancer. 2018 Jan;115:49-55.
13. Dudnik E, Moskovitz M, Daher S, Shamai S, Hanovich E, Grubstein A, et al. Effectiveness and safety of nivolumab in advanced non-small cell lung cancer: The real-life data. Lung Cancer. 2017-11-22;0(0).
14. Fujimoto D, Yoshioka H, Kataoka Y, Kim Y, Tomii K, Ishida T, et al. P2.07-024 Real-World Data of Nivolumab for Previously Treated Non-Small Cell Lung Cancer Patients in Japan: A Multicenter Retrospective Cohort Study. Journal of Thoracic Oncology. 2017 /11/01;12(11):S2425.
____
