Martínez Iturriaga S
Servicio de Farmacia. Hospital García Orcoyen (Servicio Navarro de Salud-Osasunbidea). Estella. Navarra (España)
Fecha de recepción: 28/07/2022 – Fecha de aceptación: 29/08/2022
Correspondencia: Sheila Martínez Iturriaga – Hospital García Orcoyen (Servicio de Farmacia) Servicio Navarro de Salud – Osasunbidea (SNS-O) – C/Sta Soria, 22 – 31200 Estella. Navarra (España)
smiturriaga@gmail.com
____
Resumen
Tocilizumab es un medicamento biológico anti interleucina 6 (IL-6) financiado en su presentación subcutánea para: 1) arteritis de células gigantes (ACG) en adultos, 2) artritis idiopática juvenil poliarticular (AIJp) en mayores de 12 años, 3) AIJ sistémica activa en mayores de 12 años, 4) artritis reumatoide (AR) activa de moderada a grave en adultos con respuesta inadecuada/intolerancia a tratamiento previo o no tratados con MTX, y en intravenosa, además de las patologías reumatológicas definidas, para el síndrome liberación de citoquinas (SLC) en adultos y mayores de 2 años y en infección por COVID-19 en adultos que reciben corticosteroides sistémicos y requieren oxígeno o ventilación mecánica (indicación en estudio)1. El empleo de tocilizumab, se ha extendido por las nuevas indicaciones financiadas y la pandemia COVID, donde se convirtió en uno de los primeros fármacos hospitalarios en pacientes graves.
Es poco frecuente (≥1/1.000 a <1/100) la aparición de diverticulitis. No obstante, la ficha técnica advierte de la precaución en pacientes con historial de infecciones recurrentes o crónicas con procesos subyacentes (diverticulitis) y añade, que se han notificado casos poco frecuentes de perforaciones como complicaciones de una diverticulitis y que los pacientes que presenten síntomas relacionados (dolor abdominal, fiebre), deben ser evaluados para identificación precoz por la gravedad de la reacción2.
Este trabajo describe un caso clínico de sepsis secundaria a diverticulitis aguda con microperforación asociada al uso de tocilizumab en arteritis de células gigantes, que motivó la hospitalización y la suspensión inmediata del fármaco y posterior, cambio de tratamiento.
Palabras clave: Tocilizumab, seguridad, sepsis.
Sepsis secondary to acute diverticulitis associated with the use of tocilizumab
Summary
Tocilizumab is a subcutaneous anti-interleukin 6 (IL-6) biological drug financed for: 1) giant cell arteritis (GCA) in adults, 2) polyarticular juvenile idiopathic arthritis (pJIA) in people over 12 years of age, 3) JIA active systemic arthritis in patients older than 12 years, 4) moderate to severe active rheumatoid arthritis (RA) in adults with inadequate response/intolerance to previous treatment or not treated with MTX, and intravenously, in addition to the defined rheumatological pathologies, for the syndrome release of cytokines (SLC) in adults and older than 2 years and in COVID-19 infection in adults receiving systemic corticosteroids and requiring oxygen or mechanical ventilation (indication under study)1. The use of tocilizumab has spread due to the new financed indications and the COVID pandemic, where it became one of the first hospital drugs in seriously ill patients.
Diverticulitis is rare (≥1/1,000 to <1/100). However, the data sheet warns of caution in patients with a history of recurrent or chronic infections with underlying processes (diverticulitis) and adds that rare cases of perforations have been reported as complications of diverticulitis and that patients who present symptoms, they should be evaluated for early identification, possibly associated with gastrointestinal perforation2.
This work describes a clinical case of sepsis secondary to acute diverticulitis with microperforation associated with the use of tocilizumab in giant cell arteritis, which led to admission to the Intensive Unit and immediate suspension of the drug and subsequent change of treatment.
Key words: Tocilizumab, safety, sepsis.
____
INTRODUCCIÓN
El perfil de reacciones adversas de tocilizumab en ficha técnica define como casos infrecuentes y graves, las perforaciones diverticulares por complicaciones en pacientes con diverticulitis. Se advierte del uso con precaución en antecedentes de ulceración intestinal o diverticulitis2. La bibliografía que correlacione tocilizumab con diverticulitis o ulceración gastrointestinal es escasa. Existe una revisión sistemática que compara el riesgo de perforación diverticular de tocilizumab y el de otros fármacos modificadores de la enfermedad en artritis reumatoide y concluye que el riesgo puede ser ligeramente mayor en pacientes tratados con tocilizumab comparado con FAME o Anti-TNF, pero más bajo que los corticosteroides. El mecanismo de acción del antagonismo de IL-6 en la fisiopatología de la perforación diverticular aún no parece estar claro3.
DESCRIPCIÓN DEL CASO
Mujer de 80 años con arteritis de la temporal diagnosticada en 2007 y en tratamiento con tocilizumab (TCZ) subcutáneo semanal desde mayo 2020 (ultima dosis recibida 3 de febrero de 2021), y con historial previo de diverticulitis informada de divertículos de boca ancha no complicados en colon izquierdo en ultima endoscopia realizada en junio 2020 (en tratamiento con rifaximina).
El 5 de febrero de 2021, acude a Urgencias de este Hospital con cuadro de vómitos alimentarios y tiritona (37,8ºC), TA 140/60, glucemia 104 mg/dl y SatO2 del 98%, con buena función respiratoria y exploración abdominal normal que evoluciona desfavorablemente con aumento de la temperatura (38ºC) y dímero D de 28000 a 65000 ng FEU/ml. Test PCR COVID negativo.
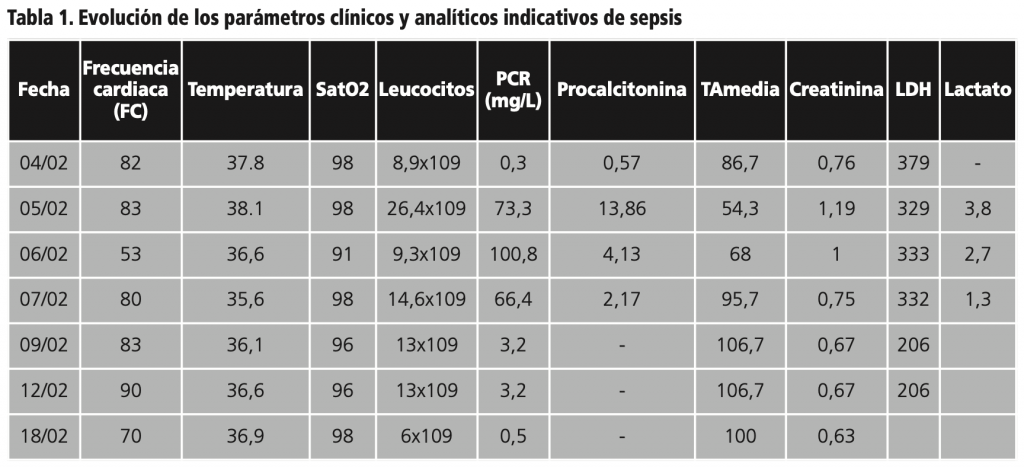
Se ingresa en Medicina Interna: TC tórax normal y ecografía abdominal informada como quistes simples hepáticos y engrosamiento mural diverticular compatible con cambios inflamatorios en relación con diverticulitis. Reactantes de fase aguda (RFA) en aumento, desarrollando leucocitosis importante, neutrofilia, trombopenia, acidosis metabólica con lactato elevado con procalcitonina de 13,86 ng/ml, dimero D de 44175 ng FEU/ml, LDH 329 U/L, PCR 73,3 mg/L, FG: 43 ml/min, lactato 3,8 mmol/L. Parámetros clínicos: TA 77/55, FC=83 lpm, Tª 38,1ºC, saturación O2= 94%. Se aísla E coli en hemocultivo. Se inicia tratamiento de soporte hemodinámico y terapia antibiótica con piperacilina-tazobactam 4g/8h iv. La evolución de los parámetros que definen criterios de sepsis se exponen en la tabla 1. Las variables clínicas y hemodinámicas (frecuencia cardiaca, temperatura e índice de SatO2, TAmedia) permanecen estables, las de inflamación (leucocitos, PCR y procalcitonina) se normalizan a los 7 días, el lactato se estabiliza el día tercero desde el ingreso. A la semana el resultado del TAC abdominal determina diverticulitis aguda complicada con micro perforación contenida y pileflebitis. La paciente evoluciona favorablemente con tratamiento antibiótico basado en piperacilina-tazobactam 4g/8h (sensible a E.coli) desde el día del ingreso hasta el alta hospitalaria (13 días).
Se realiza interconsulta con Reumatología que decide tratar la arteritis del temporal con prednisona comprimidos 5 mg en desayuno y cena y ver su evolución. Posteriormente, metotrexato 15 mg semanal + ácido fólico y pauta de reducción corticoidea. En el PET de octubre de 2021 se muestra resolución del cuadro y no evidencia de arteritis.
En la actualidad, un año más tarde del suceso, está en tratamiento con prednisona 2.5 mg desayuno y 1.25 mg en cena, metotrexato 20 mg oral, ácido fólico, AAS, calcio y vitamina D con buen control.
DISCUSIÓN
Se describe una reacción adversa grave, informada en ficha técnica de TCZ que motivó el ingreso hospitalario y requirió tratamiento para la resolución de la sepsis originada. Tras un año desde el cuadro asociado al fármaco, no ha vuelto a manifestar más episodios de diverticulitis aun en tratamiento con corticoides a dosis bajas. Se han notificado casos poco frecuentes asociados al uso de TCZ en este contexto3, y ningún caso para la indicación de arteritis de células gigantes.
El empleo de TCZ para el tratamiento del SLC originado por el SARS-Cov19, supuso un aumento de su uso siendo importante perfilar el historial de infecciones crónicas/recurrentes. Así, un estudio en EE.UU. que evalúa su empleo en un total de 74 pacientes con COVID-19 ingresados en medicina intensiva manifiesta un aumento de las reacciones adversas asociadas a infecciones tras la administración (23% vs 8%) respecto a los pacientes que no recibieron TCZ (p=0.013), se registró aumento de transaminasas, neutropenia e hipertensión, pero, no hubo casos de perforación intestinal ni agravamiento de las diverticulitis4. Sería interesante conocer los antecedentes previos de diverticulitis de los pacientes para valorar si existe relación o no entre la administración de TCZ y perforaciones intestinales en ese grupo de pacientes. Los autores concluyen reiterando la necesidad de sopesar cuidadosamente el potencial de infecciones y toxicidades relacionadas con el TCZ al considerar su uso.
El estudio observacional de Strangelf et al. sí evalúa el riesgo de perforación intestinal en un grupo de 13.310 pacientes afectos de artritis reumatoide (AR) bajo tratamiento biológico en base a las notificaciones registradas, y describe una incidencia de perforaciones intestinales superior para TCZ que para el resto de tratamientos biológicos para AR. Se advierte, además que los síntomas pueden ser leves y estar enmascarados por no existir elevación de los valores PCR. La incidencia encontrada de perforaciones intestinales con tocilizumab es de 2,7/1.000 pacientes/año, muy superior a los 0,2-0,6/1.000 pacientes/año en el resto de terapias3. La edad, las dosis de glucocorticoides y AINEs previos también se relacionan con el riesgo de perforación intestinal5.
Parece evidente la relación entre TCZ y la aparición de perforaciones intestinales en pacientes con historial previo de diverticulitis pese a la baja incidencia. No obstante, se desconoce la influencia de la inhibición de la IL-6 en el desarrollo del cuadro. Respecto a la medicación concomitante, aunque algunos estudios manifiestan el empleo de corticoides y AINEs como factores de riesgo en el desarrollo, la paciente fue tratada con corticoides previos a uso de TCZ para la patología en cuestión, lo que pudo agravar la predisposición. Sin embargo, el uso de corticoides posteriores al cuadro (prednisona 2.5 mg y 1.25 mg), así como metotrexato a largo plazo no ha ocasionado más episodios de diverticulitis.
Del caso expuesto, se concluye con la necesidad de conocer todas las advertencias de manejo de los fármacos y considerar, por infrecuentes que sean, todas las reacciones adversas descritas, valorar la relación beneficio-riesgo de forma individualizada y no iniciar el tratamiento en casos que puedan suponer riesgo de aparición de reacciones graves. En los pacientes candidatos a recibir TCZ, en cualquier vía y a cualquier dosis, es fundamental valorar antecedentes de diverticulitis y/o infecciones crónicas/recurrentes.
El presente caso fue notificado al Centro de Farmacovigilancia correspondiente.
Conflicto de intereses: La autora declara no tener conflicto de intereses.
BIBLIOGRAFÍA
1. Bifimed: Buscador de la información sobre la situacion de financiación de los medicamentos – Nomenclator de JULIO – 2022. Disponible en: https:// www.sanidad.gob.es/profesionales/medicamentos.do?metodo=verDetalle&cn=661936. Visto el 12 de Julio de 2022.
2. Ficha técnica de Roactemra® 162 mg solución inyectable en pluma precargada. Disponible en: https://cima.aemps.es/cima/dochtml/ft/108492009/FT_ 108492009.html. Acceso el 15 de febrero de 2021.
3. Gout T, Ostör AJ, Nisar MK. Lower gastrointestinal perforation in rheumatoid arthritis patients treated with conventional DMARDs or tocilizumab: a systematic literature review. Clin Rheumatol. 2011 Nov;30(11):1471-4. doi: 10.1007 /s10067-011-1827-x. Epub 2011 Aug 11. PMID: 21833686.
4. Pettit NN, Nguyen CT, Mutlu GM, Wu D, Kimmig L, Pitrak D, Pursell K. Late onset infectious complications and safety of tocilizumab in the management of COVID-19. J Med Virol. 2021 Mar;93(3):1459-1464. doi: 10.1002/jmv.26429. Epub 2020 Aug 21. PMID: 32790075; PMCID: PMC7436682.
5. Strangfeld A, Richter A, Siegmund B, Herzer P, Rockwitz K, Demary W, Aringer M, Meißner Y, Zink A, Listing J. Risk for lower intestinal perforations in patients with rheumatoid arthritis treated with tocilizumab in comparison to treatment with other biologic or conventional synthetic DMARDs. Ann Rheum Dis. 2017 Mar; 76(3):504-510. doi: 10.1136/annrheumdis-2016-209773. Epub 2016 Jul 12. PMID: 27405509; PMCID: PMC5445993.
____
