Castañeda Hernández S1,3, De la Cruz Durán H1,3, García López IE2, Pérez Morales ME1, Sánchez Palacio JL1
1 Facultad Ciencias Químicas e Ingeniería. Universidad Autónoma de Baja California. Tijuana B.C. (México)
2 Derpartamento de Dermatología Hospital Infantil de las Californias. Tijuana B.C. (México)
3 Departamento de Farmacia. Hospital Infantil de las Californias. Tijuana B.C. (México)
____
Rev. OFIL 2016, 26;4:322-329
Fecha de recepción: 08/01/2016 – Fecha de aceptación: 25/10/2016
____
Correspondencia:
Saúl Castañeda Hernández
C/Piedra Luna, 1
Fracc. Eco-chumá
21440 Tecate B.C (México)
Correo electrónico: saulcashe@gmail.com
____
Resumen
Los hemangiomas infantiles son los tumores vasculares más frecuentes de la infancia, y se presentan en un 5 al 10% de los niños menores de un año. Pueden estar localizados en cualquier parte de la superficie corporal. Propranolol un β-bloqueador utilizado para tratamiento de la hipertensión y otros padecimientos cardiovasculares, recientemente se ha reportado su uso en la reducción de los tumores vasculares de la infancia, mostrando efectos superiores a los obtenidos con otros fármacos.
El propósito de esta revisión sistemática fue analizar estudios del efecto de propranolol en pacientes con este padecimiento, publicados a nivel mundial de 2010 a 2016.
En esta revisión se analizaron 15 estudios sobre el efecto farmacológico de propranolol en pacientes con hemangioma infantil; en los que se comparan dosis, inicio de la terapia, efecto terapéutico y efectos secundarios al tratamiento. En el 92% de los estudios el efecto del propranolol ha sido satisfactorio con la mínima incidencia de efectos secundarios.
Palabras clave: Propranolol, hemangioma infantil, efecto propranolol.
____
Introducción
Los hemangiomas infantiles (HI) son los tumores vasculares benignos más frecuentes de la infancia, con una incidencia al año de edad del 5-10%. Tienen una mayor frecuencia en raza blanca y en niños prematuros de peso inferior a 2 kg, con una predominancia tres veces mayor en pacientes femeninos que en masculinos. Pueden estar localizados en cualquier parte de la superficie corporal1.
Los HI se pueden clasificar de acuerdo a la profundidad en: superficiales (60%), profundos (15%) y mixtos (25%). Los hemangiomas superficiales afectan la dermis papilar, los profundos se encuentran dentro de la piel, y los mixtos, una combinación de los anteriores2. En la mayoría de los casos los HI afectan a la cabeza y cuello. Otras áreas comprometidas en orden de frecuencia son tronco, miembros inferiores y miembros superiores, mucosas orales y genitales. Según su distribución corporal los HI se dividen en: focales (70%), segmentarios e indeterminados (30%)3.
En su historia natural los HI constan de tres etapas. La etapa de proliferación se inicia durante las primeras semanas de vida, aquí los hemangiomas entran en una fase de crecimiento rápido que suele durar habitualmente de 3 a 6 meses; ésta se caracteriza por un aumento de volumen y la formación de una placa rojiza. Al final del primer año de vida suele iniciarse la fase de meseta, cuya duración es variable, en la que se observa una pérdida de la intensidad del color de las lesiones, y una pérdida evidente de volumen. Por último se inicia la etapa de involución que sucede lentamente y se caracteriza por la desaparición del HI. La duración puede ser de hasta cinco años4,5.
La causa de aparición de los hemangiomas no es conocida, existen diversas teorías sobre su etiología; varios descubrimientos han avanzado en el conocimiento de los HI, se identificó al transportador de Glucosa1 (GLUT-1) como marcador inmunohistoquímico expresado en los HI, con independencia de la etapa, GLUT-1 no se expresa en otros tumores y malformaciones vasculares, por lo que es un marcador especifico y útil para identificación de los HI6.
Storch y Hoeger (2010) plantearon hipótesis en cuanto a la formación de los HI:
Factores de crecimiento: existe un aumento de Factor de crecimiento endotelial vascular (VEGF) y el Factor de crecimiento de fibroblastos básico (bFGF) los cuales estimulan la señalización de la angiogénesis, y la formación de nuevos vasos sanguíneos, lo que produce el crecimiento del hemangioma.
La mayoría de los HI se presentan sin complicaciones, aun así más del 30% de los casos requieren de intervención médica. Las indicaciones para el tratamiento varían desde las complicaciones en vías respiratorias potencialmente mortales, ulceración, riesgo periorbital o la existencia de algún peligro en la función de algún órgano. Por lo tanto, los objetivos del tratamiento y los puntos finales difieren dependiendo de la indicación y el sitio de la participación del HI (por ejemplo, reducción de volumen o indicación para un HI ulcerado)8.
Entre los tratamientos farmacológicos utilizados se encuentran: corticoides intralesionales y tópicos, corticosteroides orales, β-bloqueadores orales, β-bloqueadores tópicos, Imiquimod tópico, interferón-α y ciclofosfamida10.
Para aquellos casos en los que no es posible el uso de medicamentos se describen otros procedimientos como: láser pulsante, cirugía y la no-intervención activa9.
Uso de propranolol en el tratamiento de hemangiomas Infantiles
Los β-bloqueadores orales, como propranolol, se consideran desde su primera publicación en el año 2008 como una opción más en el tratamiento de los HI cuando Léauté-Labréze y colaboradores observaron de forma incidental la notoria eficacia del propranolol en el tratamiento de los hemangiomas infantiles, previamente desconocida14. El mecanismo de cómo el propranolol realiza la disminución del HI aun no es claro. Varios mecanismos de acción han sido sugeridos.
1.- La vasoconstricción: se atribuye a una disminución de la liberación de óxido nítrico, β-bloqueadores tales como propranolol, inhiben la vasodilatación mediada por adrenalina, provocando la contracción de los capilares, y reduciendo el flujo de sangre al hemangioma.
2.- La disminución de la expresión de genes proangiogénicos: propranolol reduce la expresión del factor de crecimiento endotelial vascular (VEGF), e inhibe la tubulogénesis, lo que impide la angiogénesis de las células endoteliales micro vasculares; retrasando el crecimiento del HI.
3.- La activación de la apoptosis: la regresión del tumor producido por células endoteliales no diferenciadas se produce principalmente durante la fase de involución y se acelera por el bloqueo β-adrenérgico7,11. Otros posibles mecanismos de acción incluyen la inhibición de la matriz metaloproteinasas, la baja regulación de la interleucina-6 y modulación de la diferenciación de células madre12,13.
En la mayoría de los centros se indican como el tratamiento de primera elección, superando la respuesta farmacológica óptima de los corticosteroides, con una menor cantidad de efectos adversos en pacientes pediátricos15. Estos resultados se han ido confirmando en posteriores series clínicas y en estudios analizados en revisiones anteriores16. Hay numerosas publicaciones que muestran la seguridad de propranolol en la edad infantil, sin que se hayan constatado complicaciones graves, incluso en prematuros tratados por otras causas. Tampoco hay hasta la fecha ninguna complicación grave en niños con HI tratados con β-bloqueadores por lo que puede afirmarse que es un fármaco seguro para esta población17.
El propósito de esta revisión sistemática fue analizar estudios del efecto de propranolol en pacientes con hemangioma infantil, publicados a nivel mundial en las bases de datos de MEDLINE/Pub-Med, SciELO, EBSCO y Elsevier de 2010 a 2016.
Metodología
Se revisaron todos los artículos originales encontrados en inglés y español publicados en las bases de datos MEDLINE/Pub-Med, SciELO, EBSCO y Elsevier de 2010 a 2016.
Los criterios de inclusión fueron: estudios retrospectivos, prospectivos, o estudios clínicos en idioma inglés y español, sobre el efecto farmacológico de propranolol en pacientes pediátricos con hemangioma infantil, administrado vía oral. Se realizó una búsqueda con palabras clave: “propranolol”, “efecto de propranolol”, “infantile hemangioma”, “propranolol in infantile hemangioma”, “adverse effect of propranolol in hemangioma”, “side effects of propranolol”.
Los criterios de exclusión fueron: efecto farmacológico de propranolol en otras patologías. Estudios con una cantidad menor a 10 pacientes, terapia combinada de propranolol con otro beta-bloqueador o corticosteroides. Propranolol administrado por vía tópica.
Descripción de los estudios
Entre los estudios más recientes referentes a propranolol se encuentran Léauté-Labréze et al. (2015). Realizaron un estudio multicéntrico, aleatorizado, doble ciego, que evaluó la eficacia y seguridad de una solución propranolol oral en pacientes pediátricos con HI, en diferentes poblaciones pediátricas. La dosis fue de 3 mg/kg/día. Fueron tratados 460 pacientes en un periodo de 6 meses, la eficacia se demostró en el 88% de los pacientes. 10% de los niños tratados tuvieron un rebrote después de la suspensión del tratamiento. 12% de los pacientes presentaron efectos secundarios, principalmente hipoglucemia, hipotensión y broncoespasmo41.
Castaneda S. et al. (2015). Realizaron un estudio prospectivo abierto en pacientes mexicanos con HI tratados de manera ambulatoria con propranolol vía oral con dosis de 0,5-2,5 mg/kg/día, mediante una formulación extemporánea en forma de jarabe elaborado en el Servicio de Farmacia del hospital. En un periodo de 20 meses fueron tratados 31 pacientes con edades de 3 a 12 meses, el 64% fue del sexo femenino, el 96% de los pacientes respondió satisfactoriamente al tratamiento, con una disminución del tamaño y coloración del HI. En promedio la terapia tuvo una duración de 10,5 meses. El 16% de los pacientes presentaron algún efecto adverso en los primeros meses de terapia, los cuales fueron de carácter leve. Durante el estudio, el tratamiento con propranolol demostró ser eficaz y seguro, en este grupo de pacientes mexicanos, a una dosis promedio de 1,5 mg/kg/día, reduciendo el tamaño y coloración de los hemangiomas en los pacientes pediátricos tratados; con una mínima incidencia de efectos adversos39.
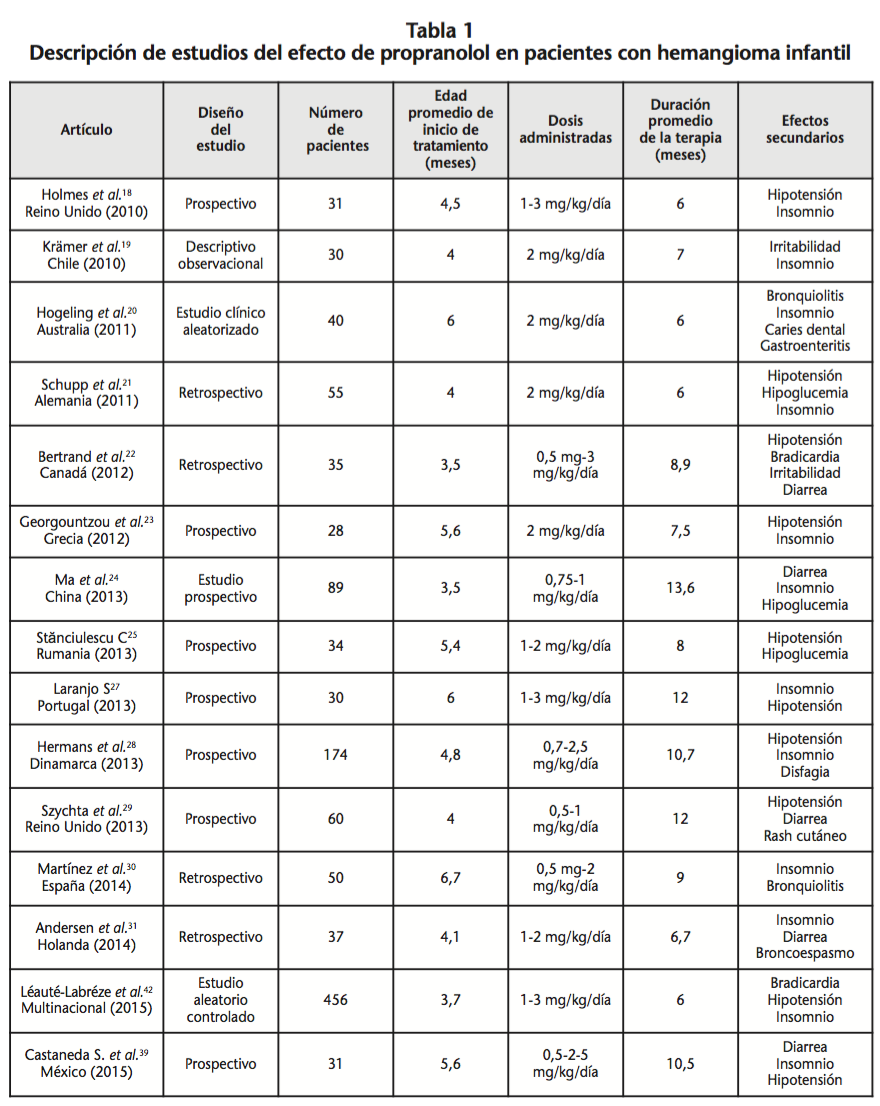
Las características generales de los estudios se describen en la tabla 1. Los estudios son heterogéneos, difieren en varios aspectos, incluyendo dosis, intervalo de dosificación, duración del tratamiento y forma farmacéutica administrada. Aun así permiten conocer el efecto terapéutico de propranolol en las diferentes poblaciones pediátricas a nivel mundial, datos demográficos, tipos de hemangiomas tratados y efectos secundarios presentados.
Resultados y discusión
En la búsqueda electrónica se encontraron 585 artículos relacionados. Con el límite de fecha de publicación del 2010 al 2016 y aplicando los criterios de exclusión, se seleccionaron 41 artículos potenciales, los cuales fueron leídos y analizados; eliminando 26 artículos que no cumplían con los criterios. Finalmente fueron incluidos 15 estudios que cumplían con los requisitos para su revisión sistemática (Figura 1).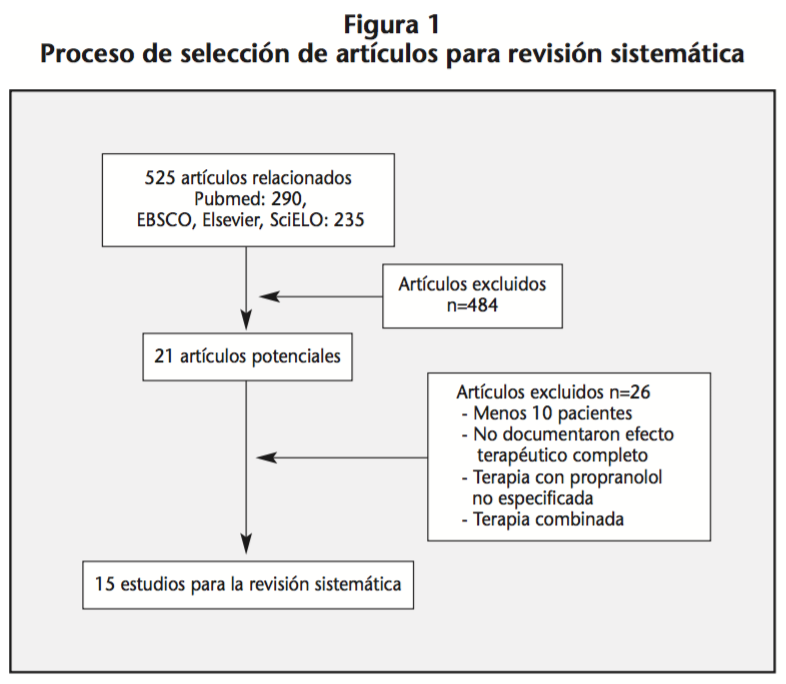
Desde el descubrimiento de propranolol en el tratamiento de los HI en 2008, más de 200 artículos se han publicado al respecto. En esta revisión sistemática se incluyen estudios realizados con un mínimo de 28 pacientes a un máximo de 17428. Las características generales de los estudios se describen en la tabla 1. Los estudios son heterogéneos, difieren en varios aspectos, incluyendo dosis, intervalo de dosificación, duración del tratamiento y forma farmacéutica administrada. Aun así permiten conocer el efecto terapéutico de propranolol en las diferentes poblaciones pediátricas a nivel mundial, datos demográficos, tipos de hemangiomas tratados y efectos secundarios presentados.
Información de los pacientes
El 71% de los pacientes tratados fueron del sexo femenino, 29% masculino. La edad promedio de los pacientes fue de 5,6 meses de edad. La aparición del HI se registró en las primeras cuatro semanas de vida del paciente.
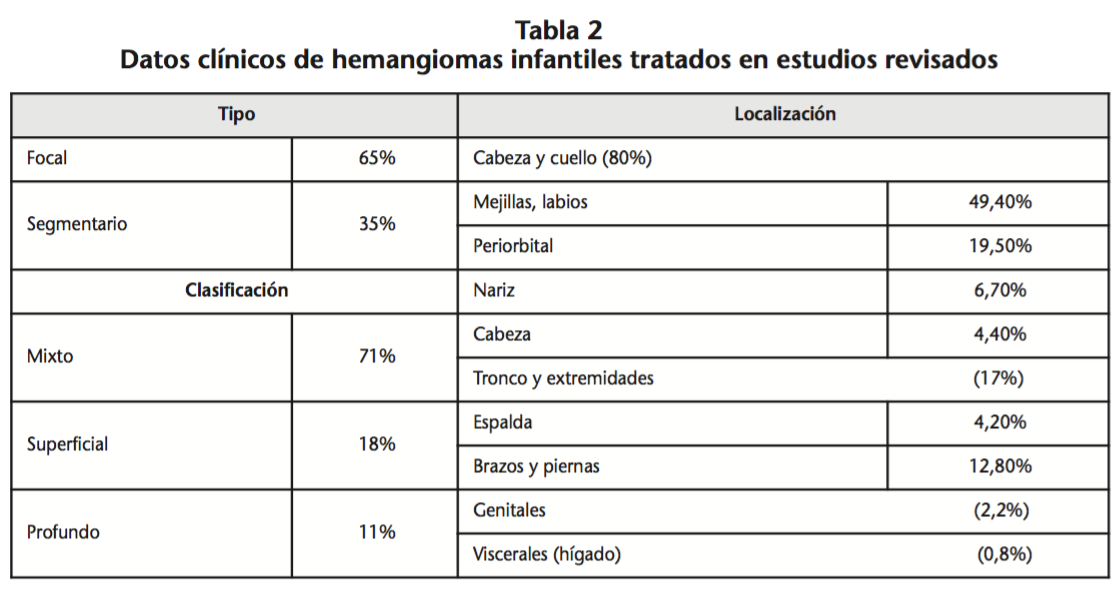
Las indicaciones principales para el tratamiento fueron riesgo de desfiguración, deterioro funcional, y ulceración. Otras indicaciones especificadas incluyen rápido crecimiento, complicaciones potencialmente mortales, estrés psicosocial, insuficiencia de corticosteroides sistémicos, y evitar procedimientos quirúrgicos21-24,30. Los datos clínicos de los HI tratados en los estudios se indican en la tabla 2.
Parámetros de tratamiento
Solo Martínez et al.30, Szychta et al.29, Hogeling et al.20 mencionaron la forma farmacéutica (solución oral de propranolol 1 mg/ml) utilizada durante el periodo de estudio. La vía de administración fue exclusivamente oral en todos los estudios.
El intervalo de la dosis de tratamiento de propranolol utilizado va desde 0,5 mg/kg/día22 hasta 3 mg/kg/día18 con una dosis media de 2 mg/kg/día, con poca variabilidad entre los estudios. Szychta et al.29 describieron la utilización de escalada de dosificación, en la que se va aumentando la dosis gradualmente hasta observar el efecto terapéutico deseado. En el estudio de Andersen et al.31 la dosificación se realizó solo al aumento de peso del niño. En cuanto al manejo de los pacientes, Hogeling et al.20, El Ezzi et al.33 manejaron terapia con hospitalización en un lapso de 48 horas, en las que se monitorizó a los pacientes para cualquier efecto grave que impidiera el tratamiento. En el estudio realizado por Krämer et al.19 la terapia fue de manera ambulatoria desde el inicio de la prescripción. Los protocolos descritos por la mayoría de los autores, como Ma et al.24 en el que indican que antes del inicio del tratamiento deben realizarse estudios básicos como electrocardiogramas, presión sanguínea, glucosa capilar y radiografía de tórax, para descartar contraindicaciones durante la terapia26.
La medicación se inicia a una media de 5,5 meses de edad en la que el HI la mayoría de las veces está muy avanzado. A pesar de esto, la alta tasa de respuesta apoya aún más las publicaciones previas que han documentado la eficacia de propranolol en el tratamiento de HI más allá de la fase proliferativa31,36. El protocolo y uso de propranolol se describe en la figura 2.

Respuesta al tratamiento
El 92% de los pacientes que recibieron propranolol durante los estudios analizados respondieron satisfactoriamente al tratamiento, con una disminución significativa de la coloración, densidad y tamaño del hemangioma.
En general, sólo el 2% de los pacientes en los estudios analizados en esta revisión fueron considerados con una respuesta inadecuada al propranolol. Estas estadísticas incluyen casos donde los autores mencionan respuesta lenta, pobre o nula24,27,30. Martínez et al.30 describieron cuatro casos de pacientes a los que se les aumentó la dosis, y no hubo respuesta adecuada, considerando que se debe al tipo de hemangioma y a la edad de inicio de la terapia.
Las fotografías seriadas del HI fueron adoptadas por todos los autores para evaluar el efecto terapéutico y la regresión del HI. Otros métodos para determinar la respuesta fue medición de los hemangiomas, mediante una cinta de grado médico, la cual presenta un sesgo de error, pero es mencionado como un método estándar para determinar el área y volumen de los HI37. Stănciulescu et al.25 llevaron un control de medidas con cinta métrica en una muestra de sus pacientes, con el cual observó la disminución y la relación con el tiempo de tratamiento. El ultrasonido en escala de grises y color combinado de ecografía Doppler es otro método para calcular el volumen de HI con mayor exactitud. Szychta et al.28 determinaron el volumen del HI antes y después del tratamiento, correlacionando el tiempo de tratamiento con la disminución del hemangioma; este tipo de medición es más exacta pero solo se reserva para los casos de hemangiomas internos ubicados en el hígado23,31.
La buena respuesta de los pacientes fue determinada cuando el crecimiento del hemangioma se detuvo y permaneció invariable durante un cierto tiempo. Una buena respuesta consistió en una mejora significativa de la lesión, con una reducción de más del 50% del volumen inicial, y una disminución del color o su desaparición completa39.
La edad de inicio de tratamiento fue mencionado por Andersen et al.27 como un factor importante para la respuesta a la terapia. Aquellos pacientes que inician antes de los 5 meses de edad tienen una alta probabilidad de una buena respuesta y menor porcentaje de un rebrote del tumor, en comparación con aquellos que inician después de los 6 meses, ya que el HI infantil está más desarrollado y necesitará de más tiempo e incluso incrementos de dosis.
La duración del tratamiento aun no queda establecida, en esta revisión el promedio fue de 8,5 meses. En el estudio realizado por Schupp et al.21 la duración de la terapia fue de 6 meses, mientras en el estudio de Ma et al.24 fue de 13,6 meses. El tiempo de tratamiento es un dato que los estudios aun no establecen, esto debido a varios factores determinantes, incluyendo la edad en que se inicia la medicación, el tamaño y la profundidad del HI, y la continuidad del paciente al tratamiento. Estos factores son importantes para definir el tiempo y dosificación adecuados de la terapia17,38.
Rebrote del HI
Un recrecimiento de la lesión, incluyendo cambios en su color o el volumen, la presencia de deterioro funcional, y/o ulceración 3 meses posteriores a la terminación del tratamiento con propranolol en los casos en que anteriormente habían respondido se considera una recurrencia35. Aproximadamente el 3% de los pacientes tratados presentan un rebote después de la suspensión de la terapia. Este efecto se puede observar dentro de los primeros 2 meses después del término de la medicación29. Andersen et al.31 mencionan en su estudio el caso de cuatro pacientes, en los que después de la cesación del tratamiento presentaron un rebrote del HI considerable, asociado a la edad de inicio de tratamiento o la falta de tratamiento continúo de la terapia, estos pacientes requirieron terapia con propranolol por siete meses más.
Efectos secundarios
Otro punto importante en la revisión de estos estudios, más allá del efecto terapéutico, es la documentación de los efectos secundarios que presentaron los pacientes en terapia con propranolol. Algunos de los efectos ya conocidos en pacientes pediátricos son hipotensión, hipoglucemia, bradicardia.
En esta revisión el 29% de los pacientes tratados con propranolol presentaron efectos secundarios. El más común que se observa son los trastornos del sueño, o insomnio en el 21% de los casos, mencionado en la mayoría de los estudios18-22,24,28. El papel del propranolol en la alteración del sueño puede deberse al hecho de que el receptor β-1 adrenérgico en la glándula pineal desempeña un papel importante en la estimulación de la melatonina. El bloqueo de este receptor se ha asociado con la disminución de los niveles de melatonina y la interrupción del ritmo circadiano32.
Se presenta hipotensión en el 20% de los casos, hipoglucemia 18% y bradicardia 15%. Otros efectos secundarios comunes reportados son: irritabilidad, diarrea, complicaciones gastrointestinales, broncoespasmo, extremidades frías y caries dental18,20,27,33.
Georgountzou et al.23 describen que estos efectos se presentan en los pacientes a los cuales se les aumenta drásticamente la dosis, y pueden ser reversibles al ajustar la posología de acuerdo al peso y edad, con un monitoreo adecuado de la presión arterial y glucosa capilar.
Entre los efectos adversos al tratamiento se menciona el caso de pacientes que presentaron taquipnea, infecciones respiratorias, asma18,22,34. De los pacientes que presentaron efectos adversos, el 2% tuvo que abandonar el tratamiento debido a que tuvieron que recibir tratamiento secundario. No hubo muertes atribuidas al tratamiento con propranolol.
El papel del farmacéutico clínico en la terapia
En la actualidad existen dos estudios publicados en los que se reporte la contribución directa del farmacéutico en el tratamiento de pacientes con hemangioma infantil, y su intervención se limita a la dispensación, en uno la participación se limita a la dispensación de la solución oral de propranolol (Hemangiol®) Martinez M30 y en el estuidio de Castaneda S y col.43 se enfatiza la participación e intervención del farmacéutico dentro del equipo de salud; basando su intervención en la educación de los familiares de los pacientes, preparación del jarabe extemporáneo de propranolol y en su seguimiento farmacoterapéutico.
Además el autor destaca que con estas intervenciones del farmacéutico se optimiza la terapia y aumenta a adherencia de los pacientes. Se menciona también que este tipo de preparaciones contribuye a un ahorro económico de los pacientes, ya que los costos son 30 veces menores a los de la formulación patentada.
Una de las estrategias que se discute en este estudio y que fue utilizada por el farmacéutico para mejorar la terapia fue la educación continua a los padres y familiares de los pacientes, orientándolos acerca del padecimiento del niño, y el manejo y administración de la formulación de propranolol, esto se realizó a través de entrevistas, folletos informativos y platicas educativas continuas con el fin de implicarlos más en el cumplimiento del tratamiento. El uso de estas estrategias se reflejó con los resultados satisfactorios obtenidos.
La importancia del farmacéutico clínico en estudios clínicos en pacientes pediátricos tiene un papel muy importante, especialmente en el uso de medicamentos de nuevas aplicaciones terapéuticas, sus intervenciones facilitan la adherencia al tratamiento con resultados satisfactorios, además de colaborar en el equipo de salud para mejorar la calidad de vida de los pacientes43.
Limitaciones
La falta de estudios en los que se cuantifiquen concentraciones plasmáticas que correlacionen el efecto terapéutico con las dosis y duración del tratamiento, serían de gran importancia para responder algunas preguntas como la duración ideal del tratamiento, cuando disminuir gradualmente la dosis de propranolol, que aún son desconocidos, y como se relacionan con el tamaño, la ubicación, y el subtipo de HI que está siendo tratado.
La presencia de un profesional farmacéutico que apoye al equipo médico en la terapia de este tipo de pacientes, es de importancia para mejorar la adherencia y el efecto terapéutico en los pacientes con HI. Estudios recientes hacen énfasis en el cuidado que se debe tener en la terapia, y la importancia del equipo multidisciplinario.
Propranolol fue aprobado por la FDA para el tratamiento de hemangiomas infantiles40, pero el protocolo de tratamiento óptimo no se conoce todavía. En 2015 fue publicado un estudio multicentrico a nivel mundial, en el que se evaluó el uso de una solución de propranolol comercial, donde se comprueba su efecto superior al placebo y otros fármacos utilizados anteriormente, y el cuidado que se debe tener para evitar los efectos adversos graves41.
Conclusiones
Propranolol es un β-bloqueador utilizado por más de 40 años en pacientes pediátricos para tratamiento de hipertensión arterial sin efectos secundarios significativos, ha revolucionado el campo de la dermatología, desplazando a fármacos como corticosteroides en el tratamiento de los tumores vasculares de la infancia.
Las publicaciones actuales realizadas a nivel mundial demuestran que propranolol es el fármaco de primera elección en pacientes con diferentes tipos de hemangioma infantil desde la etapa inicial hasta la proliferativa; con un efecto terapéutico significativo sobre la disminución del tamaño y coloración del hemangioma en el 92% de los pacientes tratados a una dosis promedio de 2 mg/kg/día, y una duración promedio de tratamiento de 9 meses; y una mínima incidencia de efectos adversos.
Se considera que el rol que juega el farmacéutico en este tipo de padecimientos en pacientes pediátricos es de suma importancia para la adherencia en el tratamiento, seguridad y eficacia terapéutica.
Conflicto de intereses: Los autores declaran no tener conflictos de intereses.
Bibliografía
1. Klauss Wolff. Dermatología en Medicina General. 7ª Ed. Argentina. Editorial panamericana; 2010 pág. 1164.
2. Bolognia Jean. Dermatología. 1a Ed. España. Editorial Elsevier; 2003, p. 1585.
3. Guzmán M, Kizlansky V. Hemangiomas infantiles. Arch Argent Dermatología. 2013;63:36-44.
4. Haggstrom AN, Drolet BA, Baselga E, et al. Prospective study of infantile hemangiomas: demographic, prenatal, and perinatal characteristics. J Pediatr. 2007; 150:291-294.
5. Phung T, Hochman M, Mihm M. Current knowledge of the pathogenesis of infantile hemangiomas. Arch Facial Plast Surg. 2005;7:319-321.
6. Chen T, Eichenfield L, Fallon S. Infantile Hemangiomas: An Update on Pathogenesis and Therapy. Pediatrics. 2013;131:99-106.
7. Storch CH, Hoeger PH. Propranolol for infantile Hemangiomas: insights into the molecular mechanisms of action. Br J Dermatology. 2010;163:269-274.
8. Sánchez I, Ruiz R, López J. Propranolol en hemangiomas infantiles: eficacia clínica, riesgos y recomendaciones. Actas Dermosifiliogr. 2011;102:766-779.
9. González M, Ramos L, Yáñez J. Uso sistémico de Propranolol en el tratamiento de hemangiomas infantiles. Revista Mexicana de Oftalmología. 2011;85(4):205-214.
10. Uriarte B. Víctor, Trejo F. Sergio. Farmacología Clínica. 1a Ed. México. Editorial Trillas; 2003, p. 309.
11. Bingham M, Saltzman B, Perkins JA, et al. Propranolol reduces infantile hemangioma volume and vessel density. Otolaryngol Head Neck Surg. 2012;147:338-44.
12. Greenberger S, Bischoff J. Infantile Hemangioma Mechanism(s) of Drug Action on a Vascular Tumor. Cold Spring Harb Perspect Med. 2011;1:a006460.
13. Sommers S, Smith D. Beta blockade induces apoptosis in cultured capillary endothelial cells. In Vitro Cell Dev Biol Anim. 2002;38:298-304.
14. Léauté-Labrèze C, Dumas de la Roque E, Hubiche T, Boralevi F, et al. Propranolol for severe Hemangiomas of infancy. N Engl J Med. 2008;358:2649-2651.
15. Price CJ, Lattouf C, Baum B, McLeod M, Schachner LA, Duarte AM, et al. Propranolol vs corticosteroids for infantile hemangiomas: a multicenter retrospective analysis. Arch Dermatol. 2011;147:1371-1376.
16. Zimmermann AP, Wiegand S, Werner JA, et al. Propranolol therapy for infantile hemangiomas: Review of the literature. Int J Pediatr Otorhinolaryngol. 2010; 74:338-342.
17. Beth A, Peter C. Initiation and Use of Propranolol for Infantile Hemangioma: Report of a Consensus Conference. Pediatrics. 2013;131:128-140.
18. Holmes WJ, Mishra A, Gorst C, Liew SH. Propranolol as first-line treatment for rapidly proliferating infantile Hemangiomas. J Plast Reconstr Aesthet Surg. 2011; 64:445-51.
19. Krämer D, Muñoz P, Alfaro P. Propranolol en el Tratamiento de los Hemangiomas de la Infancia. Rev Chil Pediatr. 2010;81(6):523-530.
20. Hogeling M, Adams S, Wargon O. A randomized controlled trial of propranolol for infantile hemangiomas. Pediatrics. 2011;128(2):259-266.
21. Schupp CJ, Kleber J-B, Gunther P, et al. Propranolol therapy in 55 infants with infantile hemangioma: dosage, duration, adverse effects, and outcome. Pediatr Dermatol. 2011;28:640-644.
22. Bertrand J, Sammour R, McCuaig C, et al. Propranolol in the treatment of problematic infantile hemangioma: review of 35 consecutive patients from a vascular anomalies clinic. J Cutan Med Surg. 2012;16:115-121.
23. Georgountzou A, Karavitakis E. Propranolol treatment for severe infantile hemangiomas: a single-centre 3-year experience. Acta Paediatr. 2012;101:469-474.
24. Ma X, Zhao T, Xiao Y, et al Preliminary experience on treatment of infantile hemangioma with low-dose propranolol in China. Eur J Pediatr. 2013;172(5):653-659.
25. Stãnciulescu C, Popoiu CM, Popoiu A. Propranolol Treatment of Infantile Hemangioma: Our Preliminary Results, Jurnalul Pediatrului. 2013;16:61-67.
26. Schiestl C, Neuhaus K, Zoller S, et al. Efficacy and safety of propranolol as first-line treatment for infantile hemangiomas. Eur J Pediatr. 2011;170:493-501.
27. Laranjo S, Costa G, Paramés F. The role of propranolol in the treatment of infantile hemangioma. Rev Port Cardiol. 2014;33(5):289-295.
28. Hermans DJ, Bauland CG, Zweegers J et al. Propranolol in a case series of 174 patients with complicated infantile haemangioma: indications, safety and future directions. Br J Dermatol. 2013;168(4):837-843.
29. Szychta P, Stewart K, Anderson W. Treatment of infantile hemangiomas with propranolol: clinical guidelines. Plast Reconstr Surg. 2014;133(4):852-862.
30. Martínez C, Rodríguez M, et al. Oral propranolol in the treatment of infantile hemangioma: a case series of 50 infants. Eur. J. Pediat. Dermatol. 2014;24:86-90.
31. Andersen I, Rechnitzer C, Charabi, B. Effectiveness of propranolol for treatment of infantile haemangioma. Dan Med J. 2014;61(2):A4776.
32. Stoschitzky K, Sakotnik A, Lercher P, et al. Influence of beta-blockers on melatonin release. Eur J Clin Pharmacol. 1999;55:111-115.
33. El Ezzi O, Hohlfeld J, De Buys Roessingh A. Propranolol in infantile haemangioma: simplifying pretreatment monitoring. Swiss Med Wkly. 2014;7:144-159.
34. Hassan BA, Shreef K. Propranolol in treatment of huge and complicated infantile hemangiomas in Egyptian children. Dermatology Research and Practice. 2014; 8:115-120.
35. Shehata N, Powell J, Dubois J, et al. Late rebound of infantile hemangioma after cessation of oral propranolol. Pediatr Dermatol. 2013;30:587-591.
36. Orozco L, García E, Sáez M, et al. Características clínicas y demográficas en una cohorte de niños mestizos mexicanos con hemangioma infantil. Dermatol Rev Mex. 2014;58:215-224.
37. Sans V, De la RoqueBerk D, Berk, BA, Bruckner A. A Novel Method for Calculating the Volume of Hemangiomas, Pediatric Dermatology. 2011;28(4):478-482.
38. Zhang L, Mai H, Zheng J, et al. Preliminary study on plasma RPN concentration of patients with infantile hemangioma treated with Propranolol. Int J Clin Exp Med. 2013;6(5):342-345.
39. Castaneda S, Garcia E, De la Cruz H, Ramirez O, Melendez S, Sanchez-Palacio J. Therapeutic Effect of Propranolol in Mexican Patients with Infantile Hemangioma. Drugs – Real World Outcomes. 2015; DOI 10.1007/ s40801-015-0052-3
40. Talaat A, Elbasiouny M, Elgendy D, Elwakil T. Propranolol treatment of infantile hemangioma: clinical and radiologic evaluations. J Pediatr Surg. 2012;47:707-714.
41. Food drug and administration EUA. Aprobación de propranolol en el tratamiento de hemangiomas infantiles. http://www.accessdata.fda.gov/scripts/cder/drug
satfda/index.cfm?fuseaction=Search.DrugDetails [Acceso 26-Agosto-2014].
42. Léauté-Labrèze C. Hoeger P, Mazereeuw-Hautie J, et al. A Randomized, Controlled Trial of Oral Propranolol in Infantile Hemangioma. N Engl J Med 2015; 372:735-740.
43. Castaneda S, Melendez-Lopez S, Garcia E, De la Cruz H, & Sanchez-Palacio J. (2016). The Role of the Pharmacist in the Treatment of Patients with Infantile Hemangioma Using Propranolol. Advances in Therapy, 33(10),1831-1839.
____
Descargar artículo en PDF: Uso de propranolol en el tratamiento clínico de hemangiomas infantiles. Revisión sistemática
